查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:兰州大学第二医院 武国德
01
—
临床资料
一般资料
青年女性,21岁,本科学历。
主诉:因“四肢无力19年余”。
现病史:入院前19年无明显诱因出现双下肢走路无力,下蹲后起立费力,需借助扶持起身,症状缓慢加重;双上肢无力主要表现为持重物不能,抬举无力,间断手震颤,写字及握拳不受影响,无四肢麻木等感觉异常,无疲劳性无力及肌肉酸痛,无明显肌肉萎缩及肉跳等。
既往史、个人史:无特殊药物服用史及毒物接触史。本科毕业,无不良嗜好。
家族史:父母为近亲结婚(堂兄妹),父母及兄妹体健。
查体
内科查体:无异常。神经科查体:主动体位,高级皮层功能正常。颅神经(-)。双上肢近端肌容积轻度减少,远端正常,双上肢近端肌力4级,远端肌力4级+,双下肢近端肌容积明显减少,双下肢近端肌力3级+,远端肌力4级,四肢肌张力正常,双侧腱反射减弱,深浅感觉对称存在,双侧病理征阴性。双侧平衡共济(-)。颈软无抵抗,脑膜刺激征阴性。
实验室检查:血常规、生化、甲状腺功能全套、贫血、肿瘤全套、皮质醇测定、血气分析、血浆氨、常规止凝血等均未见明显异常。脑脊液常规、生化及压力均正常范围。
辅助检查
胸部正位X线片,心脏彩超均未见明显异常;腹部B超提示慢性胆囊炎改变。肌电图:广泛神经元损害(慢性),累及颈、胸、腰骶段支配肌,脊髓前角病变多考虑。神经源性病变:运动波幅增加70%,轻收缩时限增加20%,多相波增加,重收缩减少型(单纯相);鉴别肌源性病变:时限下降、波幅下降,多相波增加;运动波幅越高提示慢性化的表现。
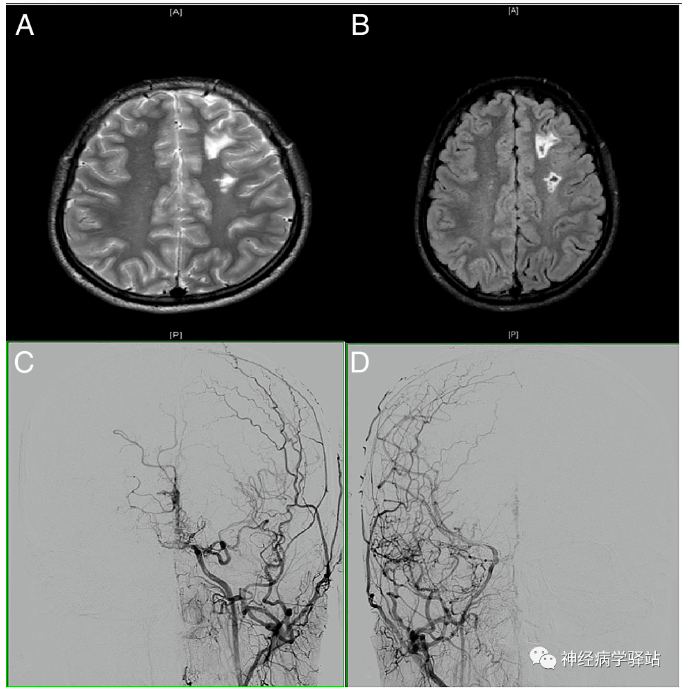
头部MR检查:如下图。
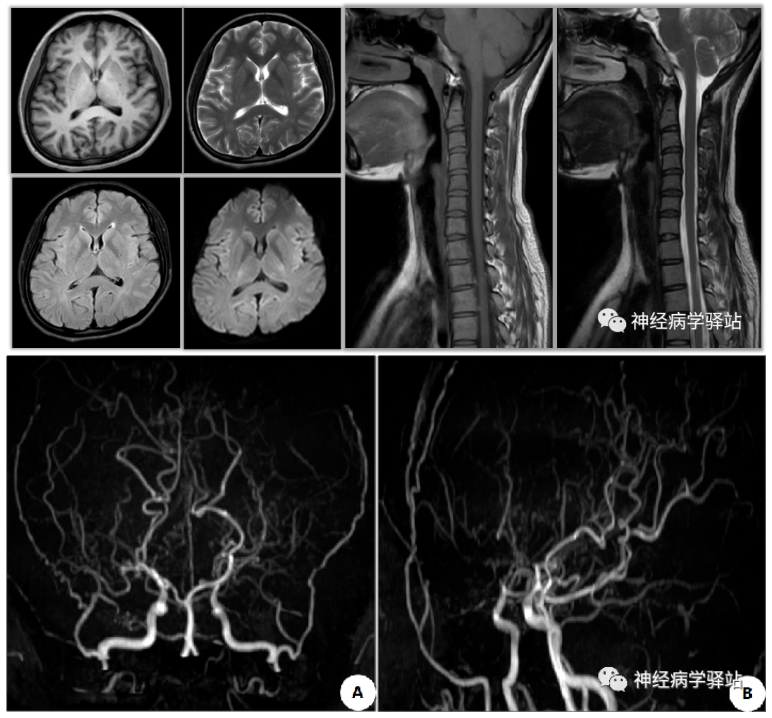
基因检测结果
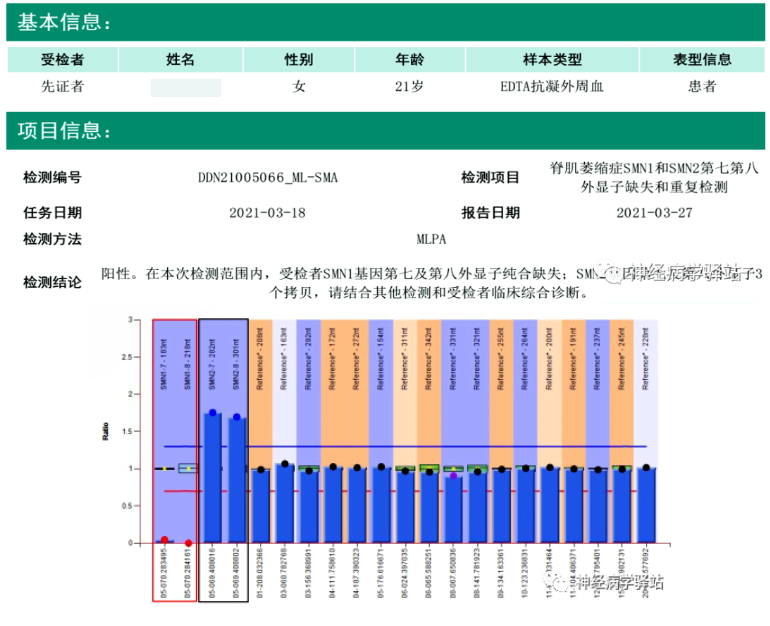
02
—
最后诊断
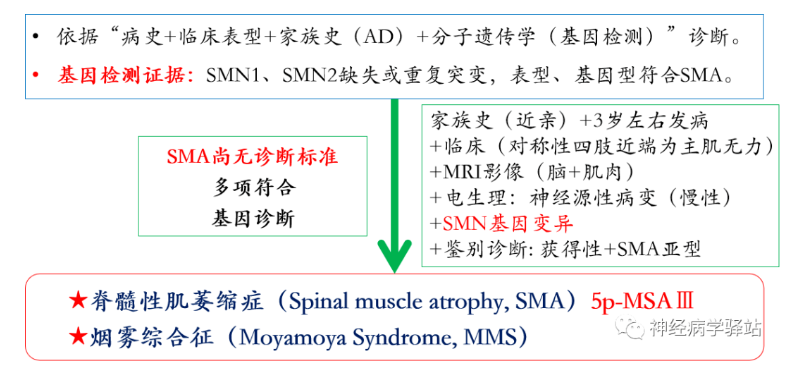
03
—
SMA和MMS,相关还是共病?
1. 罕见表现集于同一个患者,更可能具有相关性。
Puri等人报道过一例先天性颈部黑素细胞痣,双手、臂肌肉萎缩和DSA提示烟雾综合征的患者,作者认为这种“平山病+皮肤神经综合征”可能是一种未知的疾病谱系,三种征象:平山病,黑痣,烟雾病/烟雾综合征(MMD/MMS),孰主孰从,抑或是未知疾病的表现,不得而知,但作者的一句话笔者颇为认同:一个患者同时患有几种罕见疾病,可能更多提示它们之间具有相关性而不是巧合(The co-occurrence of rare diseases in a patient may hint more towards a correlation than a co-incidence.)!
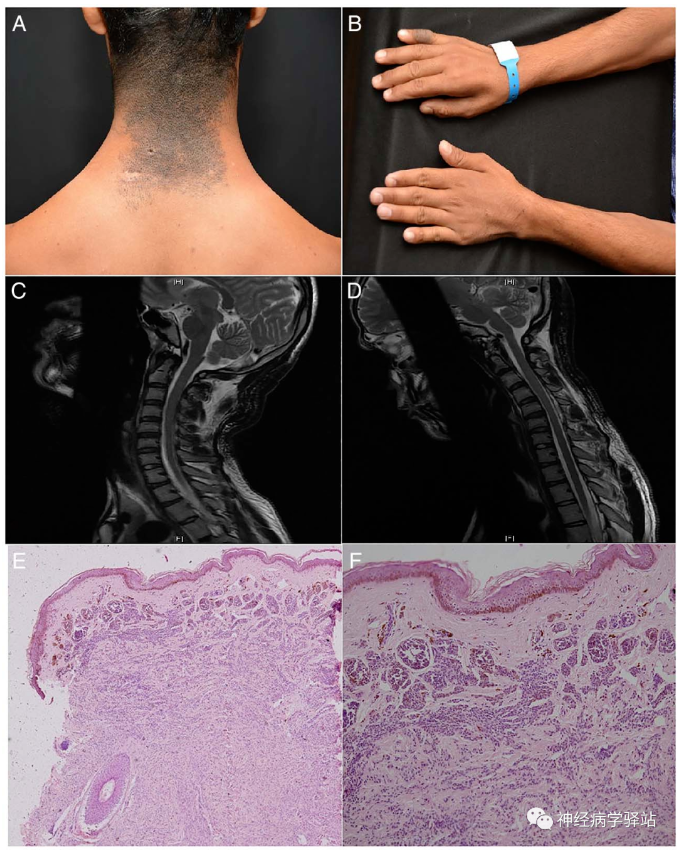
三种征象:平山病,黑痣,MMD/MMS
2. SMA与MMS可能也是一样的!
SMA是一种常染色体隐性遗传的神经肌肉疾病,以脊髓前角或脑干运动核α运动神经元变性和丢失为特征,主要临床特点为进行性、对称性四肢和躯干的肌无力和肌萎缩,近端重于远端,下肢重于上肢,有时可见舌肌纤颤、手震颤等,其发病率为1/10000~1/6000,符合罕见病有关发病率的诊断标准,属于罕见病,2019年我国第一批罕见病目录收录的121种疾病中就有SMA,所以SMA属于罕见病。
SMA的遗传学研究取得了很大进展,目前定位的基因有3个,其中5q13.1区域的SMN基因,含8个外显子,是主要功能基因,该区域还有NAIP基因,有16个外显子,与SMA协发病相关。部分成人型SMA与儿童型SMA有相似的基因改变,大部分患者基因定位尚不确定,SMN蛋白水平低下是如何导致运动神经元变性的机制亦不清除。SMN在中枢神经系统、自主神经系统、脉管系统等均有广泛表达。研究显示SMA患者可继发性丘脑的病变,大鼠的SMA模型可诱发海马病变(Ito, Y. et al)。动物研究已经证实,SMA小鼠模型中SMN蛋白水平的降低会导致围产期小鼠的大脑发育损伤;对SMA和野生型小鼠海马组织的比较蛋白质组学分析表明,当SMN蛋白水平降低时,调节细胞增殖、迁移和发育的蛋白表达水平发生显著改变,证实SMN蛋白在大脑发育中起着至关重要的作用(Wishart, T.M. et al)。SMN突变可能影响脑发育和血管的正常结构,理论上SMA出现脑血管病变是可能的,机制是否与SMN突变所致血管结构异常有关,需要进一步研究。
文献检索发现,目前还没有SMA伴发MMD/MMS的报道,SMA患者及动物研究提示SMN基因突变会影响血管的正常结构。SMN突变可能影响脑发育和血管的正常结构,理论上SMA出现脑血管病变是可能的,机制是否与SMN突变所致血管结构异常有关,需要进一步研究。结合Puri Inder等的观点,我们也推测SMA合并MMD/MMS可能也是与SMA遗传异质性相关的继发性脑血管病变,因此该患者最后诊断:SMA IIIb型,MMS/MMD,是SMA相关的MMS,亦或MMD的病因之一,有探讨的必要。日本学者Takeuchi和Shimizu于1957年首次对MMD进行描述:MMD一种慢性闭塞性脑血管病,特征性表现是DSA可见双侧ICA虹吸段和ACA、MCA起始段血管严重狭窄或闭塞,侧枝动脉代偿性增生,在颅底形成异常血管网。MMD病理(如下图,文献截图):管壁平滑肌增生,管腔闭塞,腔内血栓形成(Scott RM et al)。
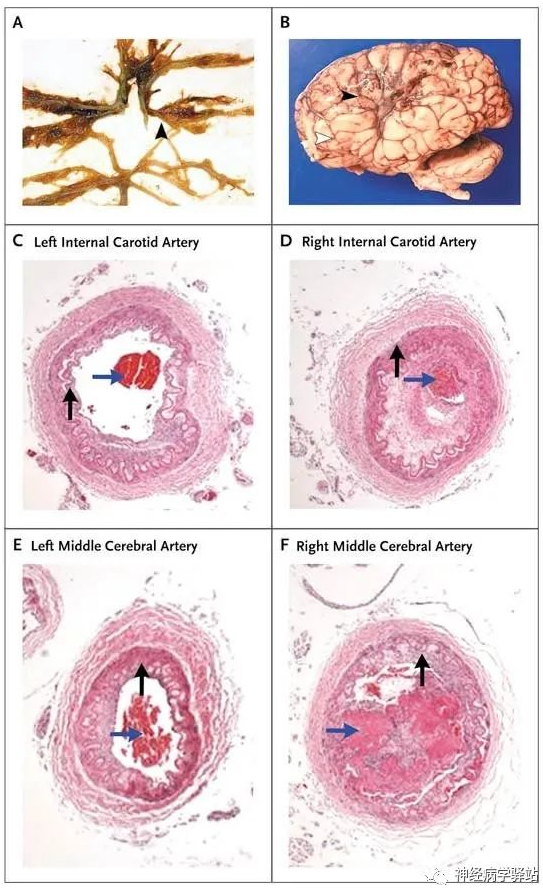
MMD的病理机制:遗传机制可能在MMD发病中起主要作用,在遗传因素的基础上,环境因素促发了易感人群的发病。全基因组连锁分析证实,17q25位点与MMD相关,其中17q25.3的环指蛋白213(RNF213)是MMD的易感基因,p.R4810K错义变异增加东亚人群对MMD的易感性。一些遗传病如唐氏综合征、镰状细胞病患者患MMD的风险较大。血管内皮生长因子(VEGF)和激酶插入域受体(KDR)多态性也被报道影响血管侧支血管的形成。烟雾病越来越被认为是儿童和成人卒中的一个病因。(Hishikawa T, et al)。

Suzukiʼs grading system(铃木分级)
MMS又称准烟雾病,是指与一种或以上基础疾病相关的准烟雾病,是由其他全身性疾病引起的继发性脑血管病(Li, et al)。很多疾病可以引起MMS,遗传病如NF1、Down综合征等,感染性疾病如结核性血管炎、EB病毒感染等,炎症性疾病如SLE、干燥综合征等,血液病如镰状细胞贫血、球形细胞增多症等,代谢性疾病、创伤、药物或吸毒等也可以引起MMS。
该SMA患者基本排除了其他可能的原因,具体是SMA或MMD的遗传多态性或是某种新的疾病表型,目前仍不得而知。随着SMN基因研究的深入,发现SMN蛋白分布非常广泛,SMN1表达异常既会影响脊髓前角细胞的功能,还会累及多部位、多脏器(Besse, et al),有国外学者甚至认为应该把SMA从MND中剔除。Nash等(Nash, et al)系统总结了SMN蛋白在消化系统、神经系统、内分泌系统、生殖系统、骨骼系统和血管系统中的表达情况,表明SMN表达异常可能导致相应脏器出现临床或亚临床表现。Somers等人的研究也发现SMA转基因小鼠脊髓血管床密度显著降低,SMN1缺失或突变可能导致外周和脊髓血管发育缺陷,但对颅内血管的影响尚不清楚(Somers, et al)。
该患者的胆囊病变、脑血管病变可能与SMN1缺失有关。基于此,我们推测SMN蛋白水平在SMA患者中的低表达可能通过影响引起发育障碍大脑中血管内皮细胞和平滑肌细胞的生长、分裂和迁移,最终发生了进行性血管狭窄甚至闭塞等MMD样异常变化。
SMA与烟雾现象共存的情况比较罕见,该SMA患者基本排除了其他可能的原因,从临床角度看,MMS很可能是先天性的,但具体是SMA或MMD的遗传多态性或是某种新的疾病表型,目前仍不得而知。我们推测可能与SMN蛋白功能障碍有关,功能缺陷的SMN蛋白导致颅内血管内皮细胞和平滑肌细胞的增殖、分化或调节异常,最后导致MMD/MMS。
所以,对于本文中涉及的两个问题:SMA与MMD/MMS之间
(1) 有无相关性?
(2) 如果有,可能的遗传机制是什么呢?
基于已有的认知,SMA与MMD/MMS之间的关系,仅限推测,依然无解!
来源:神经病学驿站
罕见病诊疗指南——抗 LGI1 抗体相关脑炎【神经系统罕见病】
《中国卒中学会关于无症状性颈动脉狭窄筛查的科学声明》在线发布
ISC 2022前沿速递|应用西洛他唑双联抗血小板治疗对卒中二级预防影响的性别差异
ISC 2022|续写新篇章 —— “替奈普酶”精彩继续……
血栓预防及血栓形成的治疗推荐丨2022 AHA/ASA自发性脑出血患者管理指南
院前和初始医疗系统的推荐丨2022 AHA/ASA自发性脑出血患者管理指南
Lancet:静脉溶栓替奈普酶(0.25 mg/kg) VS 阿替普酶
查看更多