查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






作者:中国医科大学附属第一医院 刘鹤 李玉姝 单忠艳 张浩 张义侠 李亚明 滕卫平
甲状腺癌(TC)在女性中发病率越来越高,最新报道显示甲状腺癌发病率位居女性高发肿瘤的第三位。甲状腺癌最常见的病理类型是乳头状癌(PTC),占所有甲状腺癌的80%~85%,其次是滤泡癌(FTC),占10%~15%。PTC和FTC均属于分化型甲状腺癌(DTC),虽然一般来说两者分期和预后相似,但在生物学特性及分子标志物等方面仍有其各自特点。例如,PTC易发生局部淋巴结转移,而FTC易早期出现远隔转移。两种DTC同时发生在一个患者身上很少见。
本文介绍一例同时确诊PTC和FTC的老年女性患者,且分别表达不同的分子标志物:PTC带有BRAF V600E突变,FTC表达TERT和NRAS突变。患者的肺转移癌考虑为FTC所致。该患者的术后分期及分子标志物结果提示为复发高风险,且可能预后不良。作为内分泌专科和甲状腺专科医生,应及早确定甲状腺结节良恶性以及可能的病理类型,有条件情况下检测肿瘤的分子标志物,以确定恰当的手术和后续治疗方案,提高患者生存率,改善预后。
患者女,62岁,主因“体检发现甲状腺结节4年”就诊。
患者述4年前体检发现甲状腺结节,甲状腺超声报告左侧较大者约1.3 cm×0.9cm,边界清,内呈中等回声,可见丰富血流信号,左叶另见0.6 cm×0.5cm结节,形态不规整,内呈低回声伴少许强回声点;右叶内见多个结节,较大者约1.6 cm×1.2cm,边界欠清,内呈中等回声,右叶另见直径约0.3cm强回声团。未再复查。现颈部可触及鸭蛋大小肿物,遂于外院行甲状腺超声检查,怀疑恶性,患者为求进一步诊治来我院就诊。
患者既往体健,否认甲状腺疾病家族史。患者自述病来无心悸气短、怕热多汗症状,无发热、颈部疼痛及声音嘶哑,无饮水呛咳、吞咽困难及异物感,无体重减轻。
专科检查:颈部对称,气管居中;甲状腺Ⅱ度肿大、质韧、活动可,右侧叶下部触及结节,边界不清,质地中等,无压痛,左侧叶Ⅰ度肿大,质地中等,未触及结节;颈部未触及明确肿大淋巴结,颈部听诊未闻及明确血管杂音。
患者为老年女性,4年前体检初次发现甲状腺结节,但未进一步诊治和复查。近期发现颈部可触及鸭蛋大小肿物,于外院再行甲状腺超声检查怀疑甲状腺癌来我院就诊。需要明确结节性质及肿瘤临床分期分级,再决定下一步治疗方案,因此进一步完善甲状腺功能、一般生化化验、肿瘤标志物、甲状腺结节穿刺病理,颈部及肺部影像学检查等。
血离子、血常规、肝功、肾功、血糖均正常。游离甲状腺素(FT4)14.67 pmol/L (正常值范围9.01-19.05 pmol/L),游离三碘甲状腺原氨酸(FT3)5.04 pmol/L (正常值范围2.63-5.7 pmol/L),促甲状腺激素(TSH)0.8755 mIU/L (正常值范围0.35-4.94 mIU/L)。抗甲状腺过氧化物酶抗体(TPOAb)>1000 IU/mL (正常值范围0-5.61 IU/mL),抗甲状腺球蛋白抗体(TgAb)>1000 IU/mL (正常值范围0-4.11 IU/mL),甲状腺球蛋白(Tg)1.61 ng/mL (正常值范围1.6-59.9 ng/mL),癌胚抗原(CEA)2.30 ng/mL,血清甲状旁腺激素测定(PTH)4.38 pmol/L,降钙素(CAL)0.84 pmol/L。
甲状腺超声:甲状腺右叶大小约:横径约3.43cm,前后径约2.26cm,上下径约<5.5cm;甲状腺左叶大小约:横径约1.93cm,前后径约1.32cm,上下径约<5.5cm。甲状腺腺体回声不均匀网状,类结节样伴结节(图1a)。甲状腺右叶(图1b)相当于后1/2腺体及后方见低回声区,范围约5.12cm×1.97cm×3.56cm,分叶状,融合状,边界清晰,右侧缘位于颈总动脉旁,左侧缘位于气管前方大血管上方,其内见粗大强回声,后方有声影,其内见点条状血流,C-TIRADS为4c级;右叶另于上极偏后见结节,范围约1.89cm×1.29cm,呈等回声,内见无回声区,周边见血流环绕,右叶结节为腺瘤型,C-TIRADS 为3级。甲状腺左叶中部偏前被膜下见结节,大小约0.76cm×0.60cm,呈低回声,不典型垂直位,与被膜关系密切,边缘见少量血流,C-TIRADS为4b级;左叶另于下极偏前见结节(图1c),大小约1.26cm×1.05cm,呈等回声,内见无回声区,毛刺状,周边见血流环绕,C-TIRADS 为3级。甲状腺峡部约0.45cm,结节大小约0.71×0.37cm,边缘见血流,C-TIRADS 为3级。双颈部可见多发淋巴结回声,右侧大者约1.93×0.63cm,左侧大者约:1.28×0.32cm,以上淋巴结位于Ⅱ区,形态规整,可见门样结构,可见点状彩色血流,均为2级。
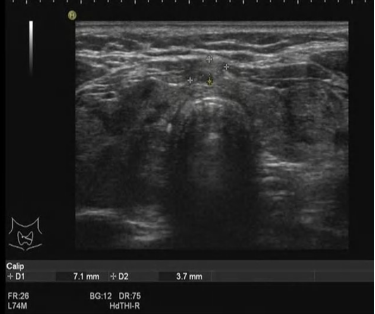
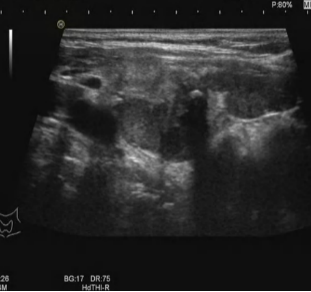
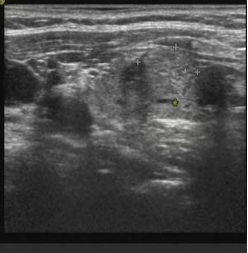
图1甲状腺超声 a 甲状腺腺体回声不均,右叶增大,双叶见多个结节;b 右叶低回声结节;c 左叶低回声结节
甲状腺增强CT(图2):右侧甲状腺增大,双侧甲状腺内可见数个大小不等的类圆形低密度影,大者位于右叶,大小约2.0cm×1.7cm,CT值34HU;增强扫描轻中度强化,CT值约143HU。右侧甲状腺内另可见点状致密影。甲状腺被膜完整,轮廓清晰。气管略受压,略有狭窄。胸骨后未见异常。双侧颈部未见肿大淋巴结。检查结论:双侧甲状腺多发结节性病变。
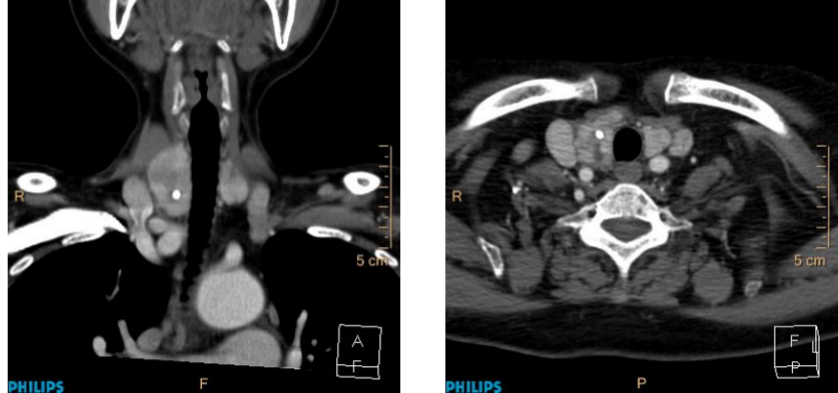
图2 甲状腺CT平扫+增强
肺CT平扫检查(图3):胸廓对称,左肺下叶可见结节(薄177),边缘光滑,大小约1.2cm×0.9cm,CT值约30HU,双肺可见多发微、小结节,大者位于左肺下叶(薄115),大小约0.6cm×0.5cm。双肺散在索条影,各级支气管通畅,无扩张与狭窄。双侧肺门不大,纵隔居中,其内未见肿大淋巴结。心脏大小正常,胸壁软组织未见异常。双侧胸膜局限性增厚伴右侧钙化。检查结论:双肺多发大小不等结节,转移瘤不除外,请结合临床病史。双肺及右侧胸膜陈旧性病变。
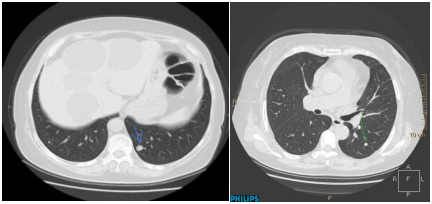
图3 肺CT平扫
超声引导下甲状腺右叶结节粗针穿刺活检:镜下所见:条形组织中见甲状腺滤泡上皮,非典型增生,排列密集,核稍大;免疫组化:CD56(-);CK19(局灶+);MC(-);galectin3(部分+)。病理诊断:可疑甲状腺癌,请结合临床。
完善患者相关检查,诊断患者甲状腺癌可能性大cN0M1,考虑患者为滤泡源性恶性肿瘤伴有远处转移,且没有手术禁忌证,应给予患者手术治疗,行全甲状腺切除,右侧VI区淋巴结清扫术。
手术病理:甲状腺右叶肿物(图4):组织大小5cm×2.5cm×1.5cm,切面见最大径0.7cm灰白质硬区域,距另见灰红质软结节两枚,最大径分别为1.6cm、0.5cm;免疫组化:CK19(±)、Galectin-3(±)、HBME-1(±);病理诊断:结合免疫组化及基因检测结果,符合滤泡癌,广泛侵犯型;分子病理: BRAF V600E、KRAS和HRAS 野生型, TERT (1-124C>T 1-146C>T)和 NRAS Exon3突变。甲状腺左叶肿物(图5):组织大小约3.5cm×1.5cm×1cm,切面见3处结节,其一最大径1.2cm灰红质软,其二最大径0.5cm灰黄质硬,其三最大径0.3cm灰白质稍韧;病理诊断:桥本病伴微小乳头状癌(约5mm),未见明确脉管,神经及被膜侵犯;分子病理:BRAF V600E突变,NRAS、 KRAS、 HRAS、TERT野生型。右侧Ⅵ区及喉前淋巴结:未见转移;分子病理:BRAFV600E野生型。
患者出院诊断为甲状腺滤泡癌伴微小乳头状癌(T1bN0M1 ⅣB期 高危组),肺转移,桥本病。予患者左甲状腺素(LT4)87.5µg每日一次口服,碳酸钙600 mg每日二次口服,一个月后复查甲状腺功能及相关抗体。
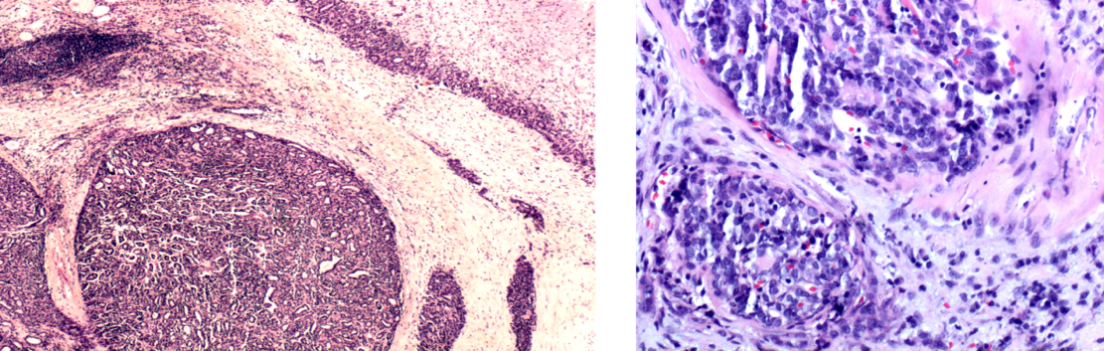
图4 甲状腺右叶术后病理
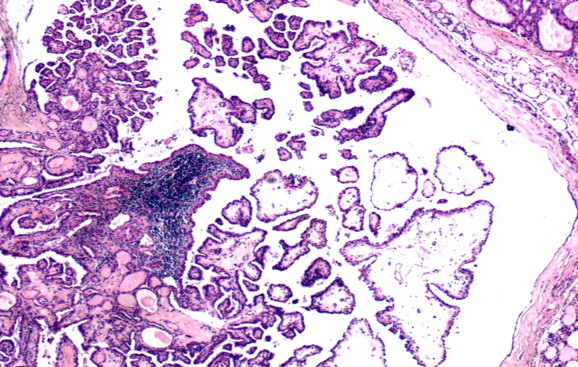
图5 甲状腺左叶术后病理
患者存在转移病灶,术后应给予清灶治疗。于术后一个月复查颈部CT和甲状腺静态显像均符合甲状腺术后改变。唾液腺动态显像:左侧腮腺摄取功能降低,酸刺激后有排泌。全身骨显像:第6胸椎显像剂分布略稀疏,恶性病变骨转移待除外。颅脑CT及肺通气功能及流速容量曲线未见异常。
嘱患者停用LT4待TSH升高,3周后复查。停药前后实验室检查结果如表1所示。
表1 不同LT4用量时期甲状腺功能及相关抗体

患者至核医学科行第1次131I清灶治疗,剂量为150mCi。131I治疗三天后全身碘显像(图6)及脏器断层显像:颈部甲状腺(图7)床区碘代谢增高,考虑残余腺体显影,双肺(图8)多发碘代谢增高,考虑转移灶显影。
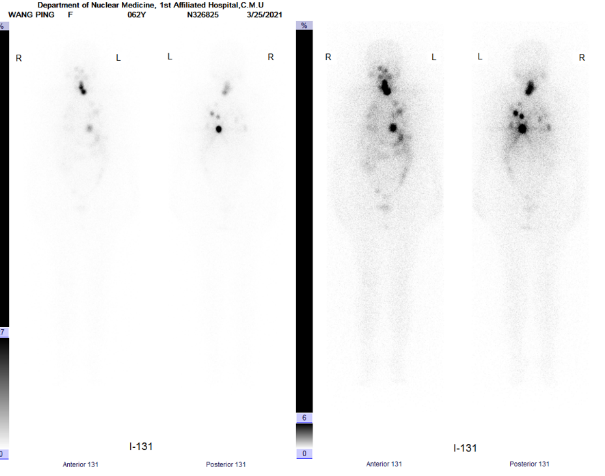
图6 131I治疗后全身碘显像
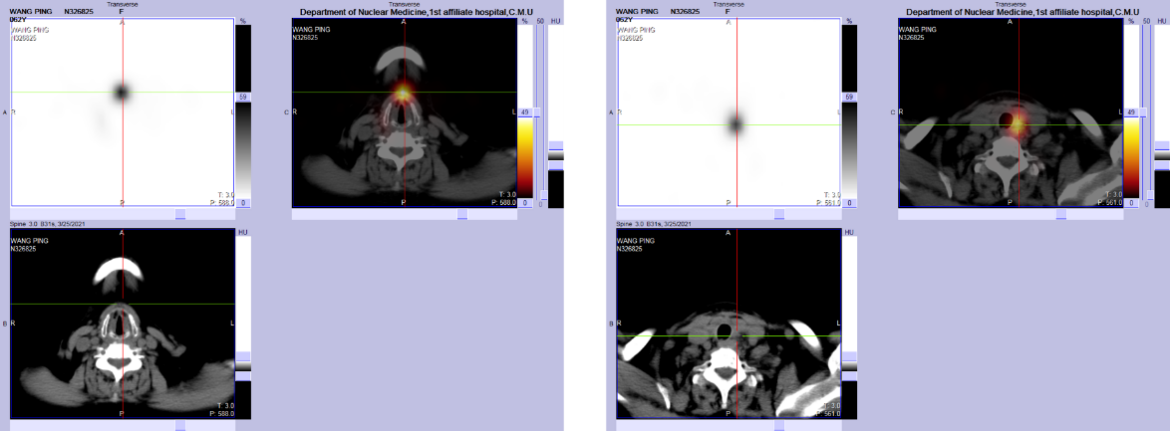
图7 脏器断层显像(甲状腺)
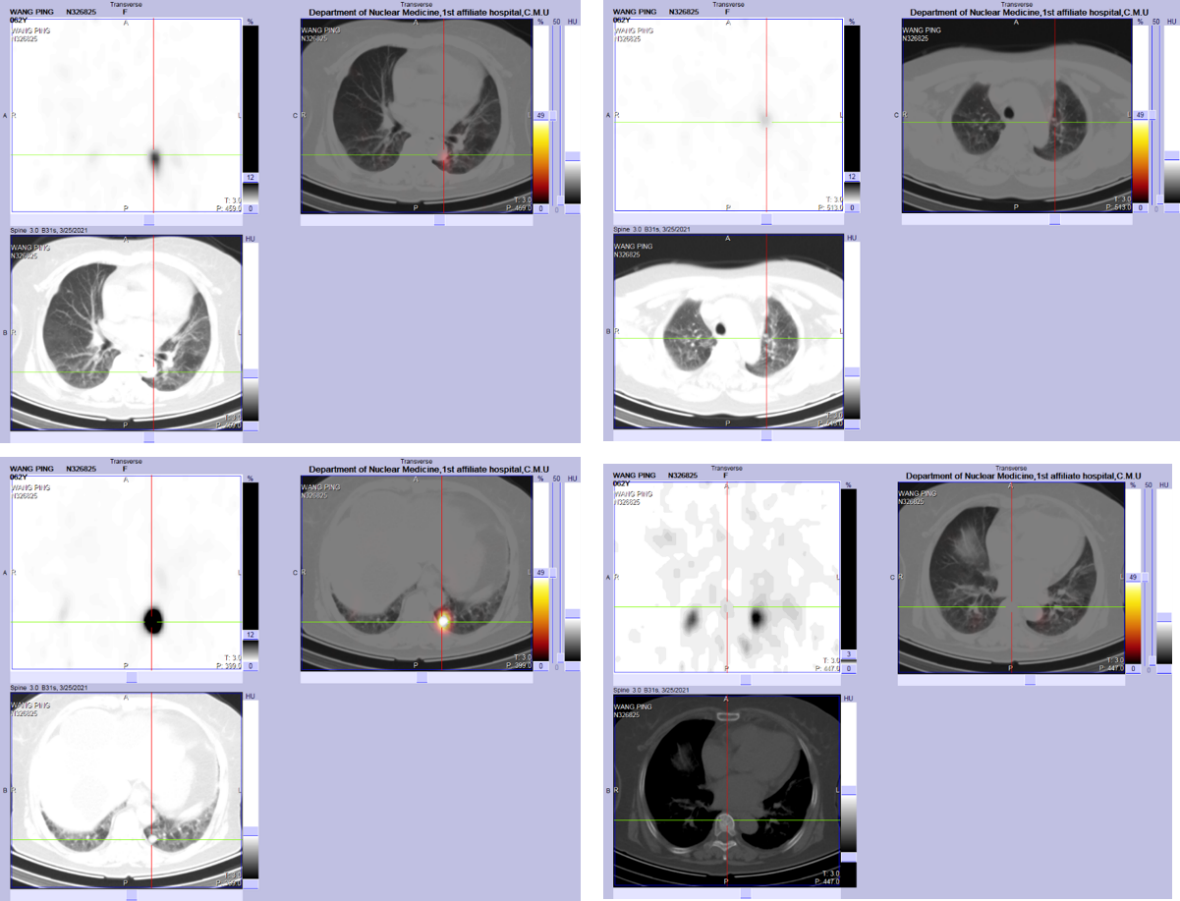
图8 脏器断层显像(肺)
继续给予口服LT4 87.5μg/d,早饭前60分钟日一次口服,调整LT4用量,TSH抑制目标0.1 mU/L以下,随访甲状腺功能及抗体相关检查结果如表1所示。补充钙(元素钙600mg/d)及维生素D3(1000单位/d)。患者骨密度正常,暂未给予其他抗骨质疏松药物。
虽然DTC是最常见的甲状腺恶性肿瘤,但在同一个患者甲状腺内同时独立地发生两种滤泡上皮细胞肿瘤:PTC和FTC,非常少见。黄韬教授团队利用SEER数据库(2004 – 2013),通过诊断代码检索FTC、PTC和PTC和FTC混合病理类型(MSTC)甲状腺癌,检索到分期和随访数据完整的甲状腺癌共有 98888 例,其中MSTC仅60例。分析MSTC的预后,发现MSTC的癌症特异性死亡率是每千人年28.823 (95% CI:12.949–64.156),而PTC是2.403 (95% CI: 2.252–2.564),FTC是6.509(95% CI: 5.598–7.569)。T4期在MSTC中比例显著高于FTC和PTC。MSTC、PTC和FTC的淋巴结转移率分别是27.6%、21.0%和3.0%,远处转移率分别是8.8%、1.2%和5.8%。该研究还发现PTC合并FTC本身并不是预后不良的因素,MSTC与同样分期、分级,接受同样手术术式和术后131I治疗的单纯PTC或FTC患者的预后相似。
本例患者左叶为PTMC,未发现淋巴结转移,右叶为FTC,没有淋巴结转移,但患者出现肺转移,考虑为FTC所致。因患者术前评估已发现肺转移灶,且双叶多发结节,因此应行甲状腺全切除术,以便彻底切除病灶,并为术后进行131I治疗奠定基础。患者一侧FTC伴肺转移,复发危险分层为高风险,术后应行131I清灶治疗。然后进行TSH抑制治疗,虽然为老年女性,但没有心血管疾病史,无骨质疏松和骨量减少,复发高危组,因此TSH抑制治疗目标为0.1mU/L以下。治疗期间给予充足的钙和维生素D预防骨质疏松。患者桥本病病史,TgAb显著升高,会干扰Tg免疫检测结果,应予以注意。观察TgAb的动态变化可能更有意义。
BRAF突变见于约50%的PTC中,大多为V600E多态性。滤泡性肿瘤中存在RAS基因突变,包括40% - 50%的滤泡性甲状腺癌、滤泡性腺瘤和具有乳头状核特征的非侵袭性滤泡肿瘤或NIFTP。BRAF和NRAS突变都改变了细胞增殖的MAPK通路。单独出现BRAF或RAS突变均不能提示肿瘤恶性程度高或复发风险高。如果BRAF或RAS合并其他突变如,TRET或TP50同时出现则提示预后不良。该患者FTC同时存在TERT和NRAS突变提示预后不良,该患者已经出现肺转移和可疑骨转移。应积极给予术后131I治疗和密切随访。第一次清灶治疗后6个月应再行全面评估,必要时再次行131I治疗。
妊娠甲状腺毒症合并分化型甲状腺癌

学习后,返回活动主页签到
累计签到4天,可获得一年期中国医学论坛报数字报
累计签到10天,可获得电子学习证书
中国医学论坛报版权所有
查看更多