查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者(点击查看大图):

来源:《中国卒中杂志》[2022,17(8):863-888]
点击阅读:
与冠状动脉狭窄的血管内治疗一样,球囊扩张/支架置入治疗后血管重度再狭窄是sICAS患者卒中复发及预后不良的独立危险因素。
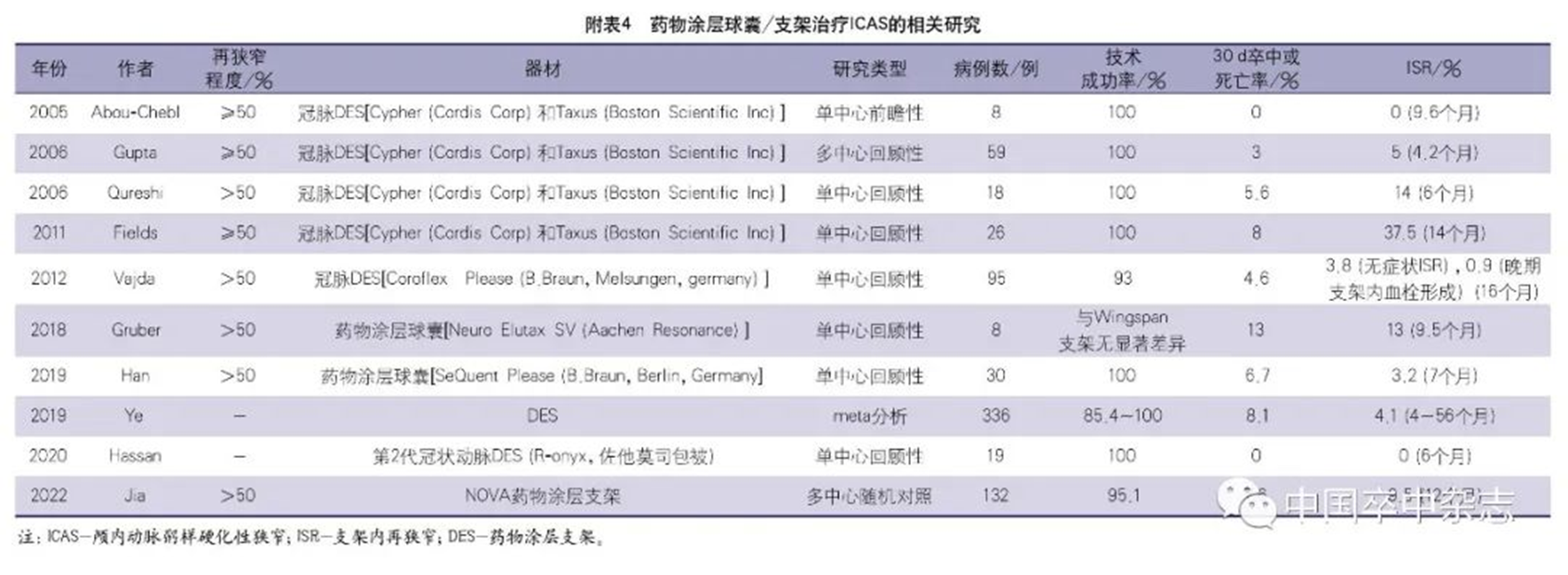
再狭窄的定义为支架内或相邻范围(5 mm内)狭窄率>50%,绝对管腔丢失>20%,其一直是困扰球囊扩张/支架置入治疗动脉狭窄的瓶颈问题,尤其是颅内血管重度再狭窄[支架内或相邻范围(5 mm内)狭窄率>70%,或较基线直径狭窄率增加>30%]与脑缺血症状及卒中复发相关。在心血管领域,较早就采用药物涂层球囊/支架来降低再狭窄的发生率,目前在脑血管领域也开始有这样的研究和临床应用。
sICAS血管内治疗后,症状性再狭窄与卒中复发关系密切,所以对术后再狭窄的随访和治疗也是sICAS血管内治疗的重点之一。球囊扩张/支架置入后再狭窄的准确机制尚不清楚,内膜增生是再狭窄的主要原因,可能与扩张创伤、支架置入后血栓形成以及血管壁对支架的炎症反应有关,其他的再狭窄危险因素还包括病变长度、治疗后的残余狭窄程度、患者年龄等。
不同研究中sICAS的治疗方式、随访时间及随访的影像设备不同,再狭窄发生率的报道结果有很大的差异。
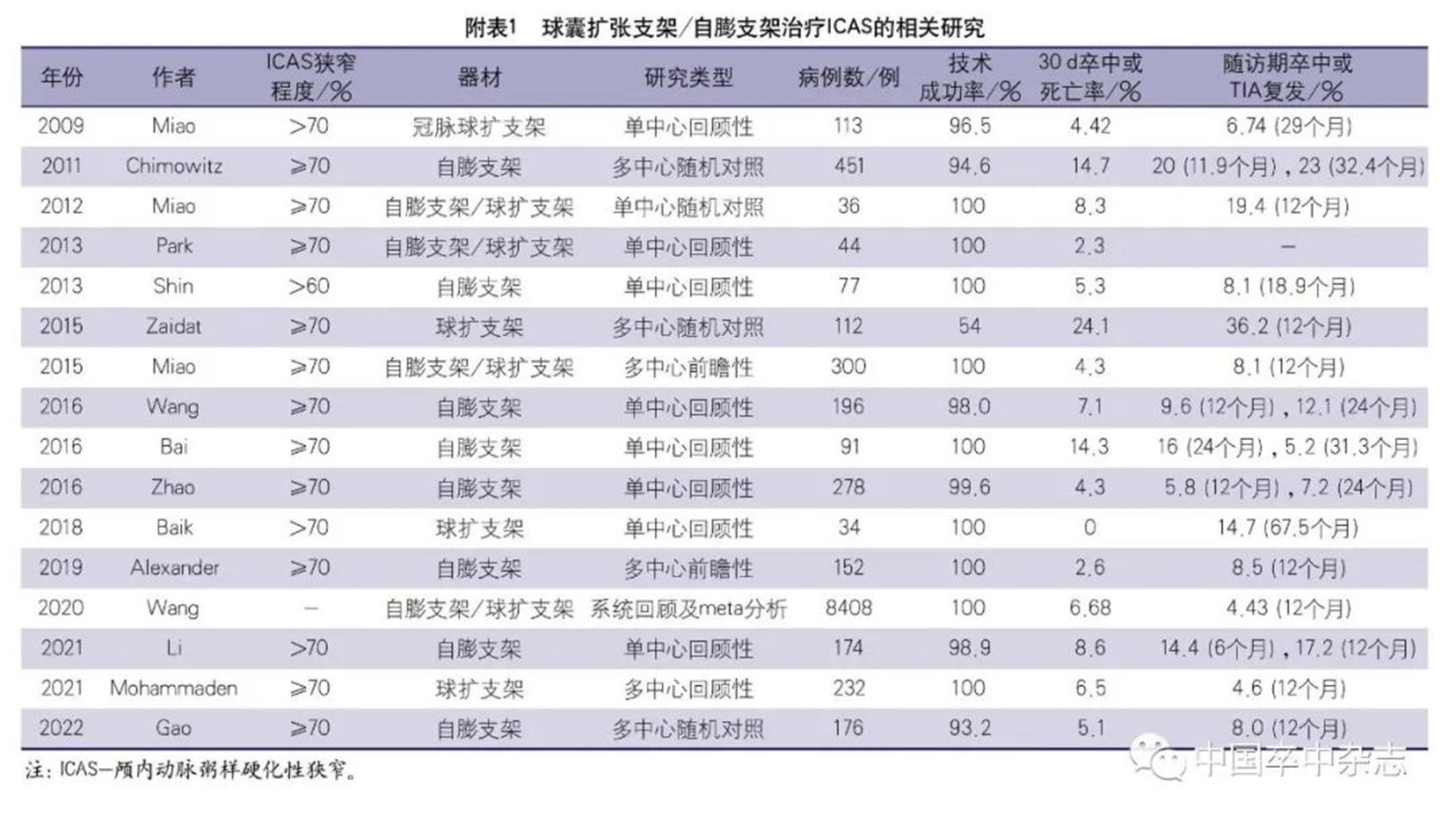
2004年,1项早期sICAS支架置入的研究发现球扩式支架有较高的技术成功率(95%)及较低的围手术期卒中发生率(1个月内6.6%),但6个月ISR的发生率高达35%。
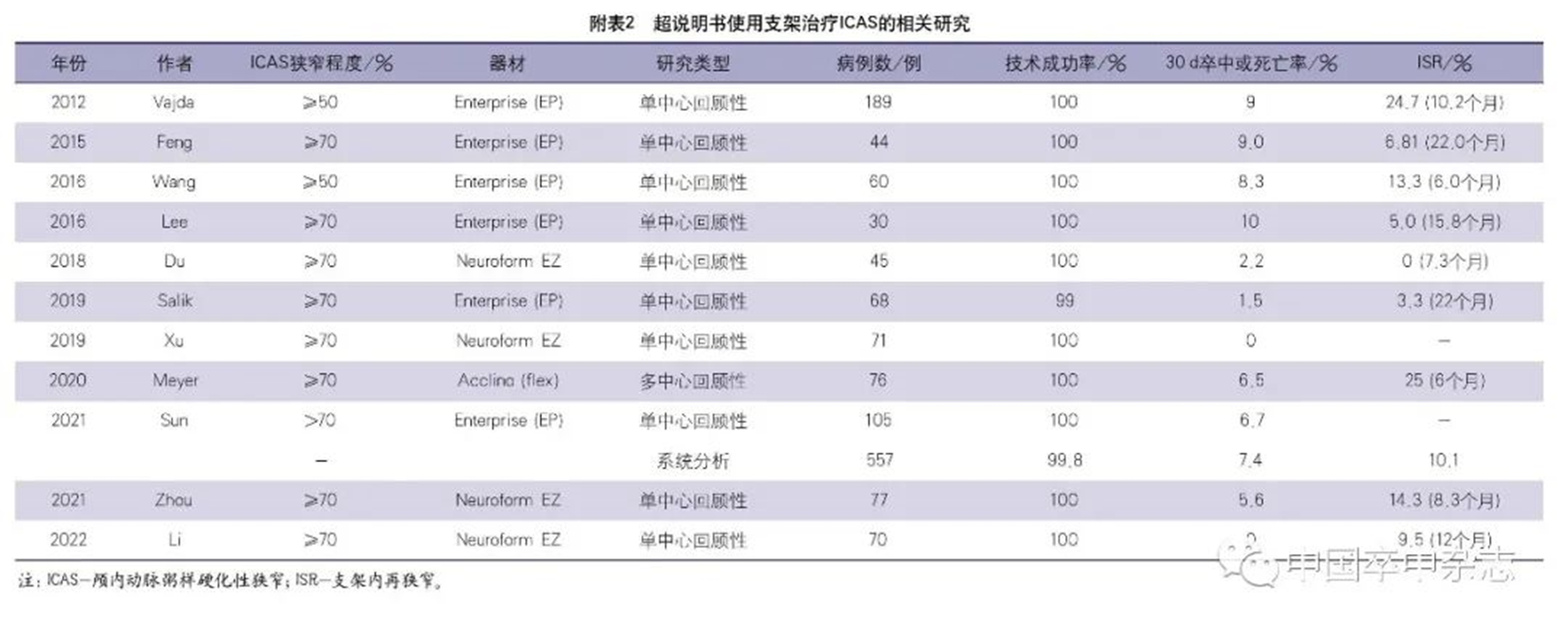
2007年,Levy等报道了应用Wingspan支架治疗78例(84个病变)sICAS患者的研究,在1.5~15.5个月的随访中,总体的ISR发生率为29.7%(25/84),症状性ISR为12%。
2008年,中国1项纳入了300例sICAS患者的多中心支架置入登记研究显示,12个月ISR(MRA/CTA证实狭窄≥50%)发生率为27.6%;球扩式支架与自膨式支架12个月ISR的发生率无显著差异(27.7% 对 27.5%,P=1.000);DSA证实的≥70%的ISR发生率为18.4%;78.9%的ISR是无症状性ISR。
2009年,1项系统分析纳入了31项研究,1134例支架置入治疗的sICAS患者,在中位随访时间(6个月)内,ISR的发生率为14.4%,其中症状性ISR占32.7%。自膨式支架与球扩式支架相比,ISR发生率显著升高(17.4% 对13.8%,P<0.001),但两者症状性ISR的发生率没有显著差异(41.6% 对 12.5%,P=0.080)。
2013年,Shin等报道了对内科治疗无效的77例sICAS患者行支架置入的单中心回顾性研究。在中位数为1年的影像随访期间,ISR的发生率为24.6%,其中17.6%为症状性ISR。快速球囊扩张及病变长度过长是支架置入后ISR的独立危险因素。
同年,Jin等报道了支架置入治疗sICAS的单中心前瞻性研究,其中1年ISR发生率为33.7%,症状性ISR为21.1%。研究同时还发现ISR组缺血性卒中的发生率显著高于无ISR组,提示ISR是支架置入后责任血管卒中复发的高危因素(21.1% 对8.5%,HR 2.94,95%CI 1.37~6.30,P=0.005)。
2017年,对SAMMPRIS研究中支架置入组的ISR发生情况再分析发现,未发生围手术期并发症的183例患者中,在35个月的中位随访期间,有27例发生了靶血管供血区的症状性梗死,16例出现了TIA。27例症状性梗死中有24例进行了充分影像学评估,ISR的发生率高达66.7%;16例TIA患者中有10例进行了充分影像学评估,ISR的发生率高达80%。1年、2年和3年随访ISR的发生率分别是9.6%、11.3%和14%。研究结果提示,在随访期间,至少每7例患者中就有1例会出现症状性ISR,症状性ISR主要发生在支架置入后第1年,是非围手术期缺血性卒中发生的重要原因。
2021年,针对WOVEN研究的1年影像(CTA/MAR/DSA)随访发现,ISR的发生率为17.6%。Haidegger等报道了115例sICAS患者支架置入治疗的单中心回顾性研究的结果,在11个月的平均随访期中,ISR的发生率33%,其中症状性ISR占11%。为找出预测ISR的生物学标志物,研究者分析了与动脉粥样硬化性硬化发展密切相关的CRP、中性粒细胞/淋巴细胞比例、血小板/淋巴细胞比例及平均血小板体积等指标,结果未发现这些生物学标志物与ISR的关联。
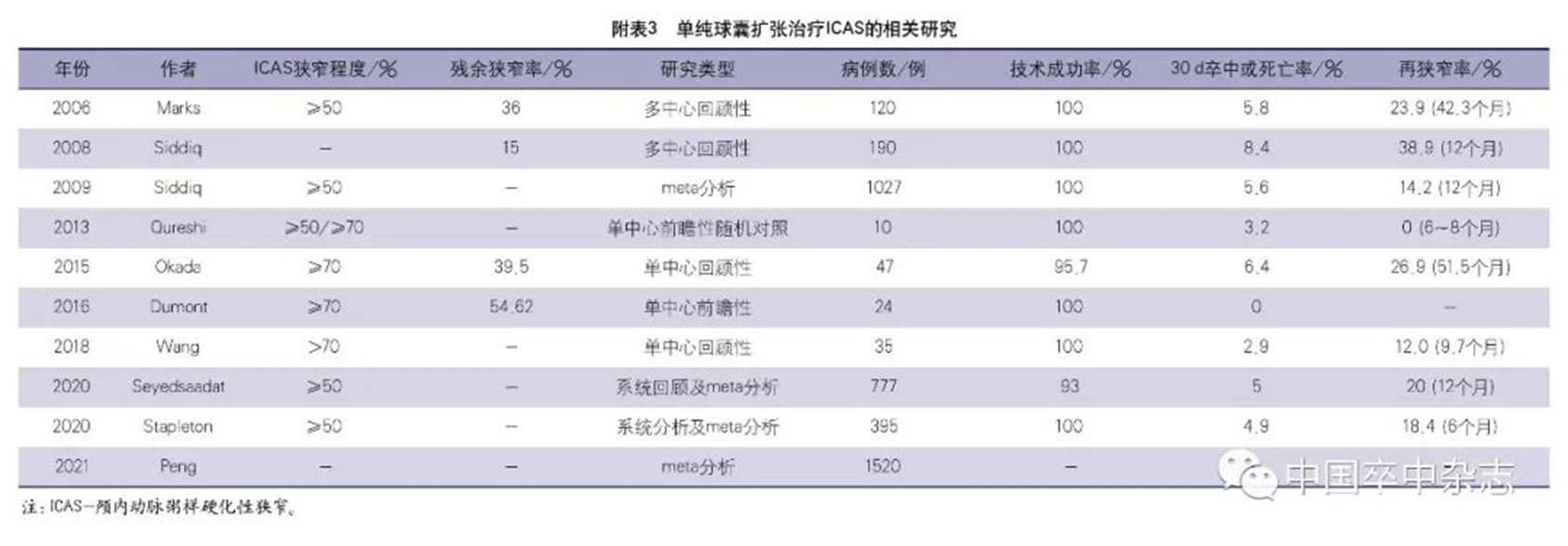
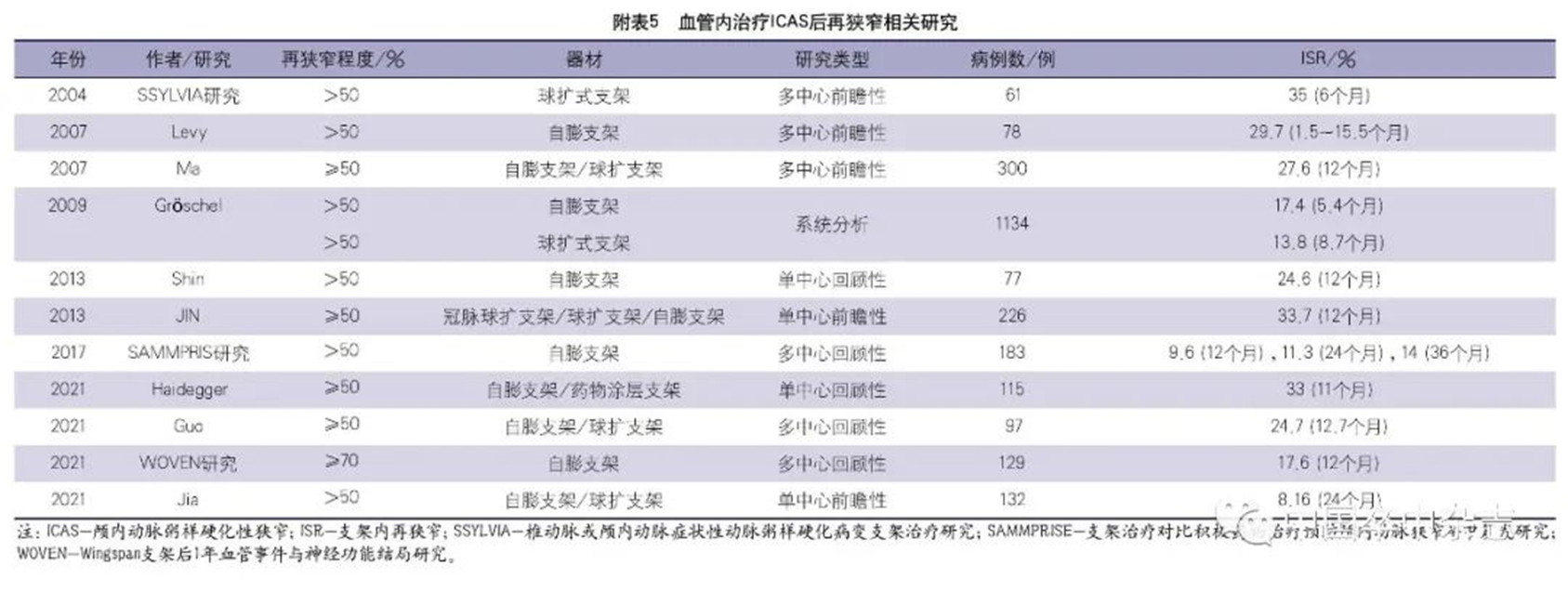
Guo等的1项来自中国的多中心回顾性研究发现,在平均12.7个月的影像学(CTA)随访中,≥50%的ISR发生率为24.7%,进一步分析发现hs-CRP是ISR的生物学标志物,回归分析发现支架长度、球扩式支架及局部麻醉是ISR的危险因素。Jia等报道了132例sICAS患者支架置入治疗的单中心前瞻性研究,结果表明随访2年的ISR发生率为8.16%。sICAS患者无论是接受支架置入治疗还是单纯球囊扩张治疗,治疗后6~12个月血管再狭窄的发生率在8.16%~35%,在卒中复发的患者中,再狭窄的发生率更高。再狭窄是导致卒中复发及预后不良的重要危险因素,应重视sICAS血管成形治疗后再狭窄的防治及监测。对本部分研究的汇总见附表5。
无症状再狭窄再发卒中风险相对较低,原则上推荐药物治疗下随访;对药物治疗无效的症状性重度再狭窄患者可以考虑通过血管介入的方式进行治疗(C-EO级证据,中等推荐)。
2012年,美国食品和药品管理局更新了Wingspan支架系统在ICAS患者中的适用范围,建议更严格地筛选患者,所以血管内治疗作为sICAS的治疗手段之一,应该在患者中选择性开展,只有通过严格的术前评估筛选的患者才能够通过手术获益。
术前评估包括:患者临床特点,手术时机,缺血性卒中病因分型,血管情况(狭窄率、位置、长度、形态、成角、斑块性质、钙化分级、血流分级、路径、远端导丝着陆区、病变与分支关系、合并其他血管病变等),脑侧支循环情况等。
与症状性颈动脉狭窄患者相似,导致缺血事件的严重sICAS短期内再发相同血管供血区域缺血事件的风险较高。但亚急性期责任血管斑块不稳定,术中操作易发生脱落导致远端栓塞等并发症。
1项有关ICAS血管内治疗时机的研究共纳入115例患者,41例患者接受早期支架治疗(发病2周内),74例患者接受晚期支架治疗(发病2周后),其中早期组有8例,晚期组有4例的再狭窄程度≥50%(P=0.018)。早期组有2例再狭窄程度≥70%,晚期组有3例再狭窄程度≥70%,差异无统计学意义。早期组中缺血性卒中、TIA、出血性卒中和死亡的总发生率高于晚期组(22.0% 对8.1%,P=0.035),单独缺血性卒中的复发率也高于晚期组(5/41 对 2/74,P=0.041)。两组TIA的发生率(1/41 对 3/74,P=0.651)、出血性卒中的发生率(1/41 对0/74,P=0.177)和死亡率(2/41 对 1/74,P=0.256)差异无统计学意义。
国内多项多中心、前瞻性研究也提示最近1次缺血性卒中距离血管内干预的时间间隔应>3周,但最佳时机仍未确定。综上,ICAS患者在急性缺血性卒中发生至少2周后行血管内治疗是比较合理的。
WASID研究的亚组分析提示脑侧支循环状态可能影响sICAS患者的卒中复发风险。对于动脉狭窄率在70%~99%的sICAS患者,具有良好的脑侧支循环的患者与较差和差的侧支循环患者相比,卒中再发风险较低,提示脑侧支循环的评估是筛选适合血管内治疗患者的重要依据之一。据此推测,经结构影像学和功能影像学方法评估脑侧支循环,并证实为血流动力学障碍引起的缺血症状发作的患者,可能更适合进行血管内治疗。
最近的1项多中心、前瞻性研究表明,远端灌注或血流受损的sICAS患者在药物治疗后卒中复发的风险更高。椎基底动脉血流评估及TIA和卒中风险(VERITAS)研究表明,在症状性椎基底动脉狭窄的患者中,远端血流受损是卒中复发的1个强有力的预测因子(HR 11.55,95%CI 1.88~71.00,P=0.008)。
另外1项单中心回顾性研究提示,对于波及颅内段颈内动脉或MCA近端的sICAS病变,最大达峰时间(Tmax)>6 s的延迟灌注区域≥15 mL的患者与<15 mL或无延迟灌注的患者相比,其卒中复发率更高。
国内的1项多中心研究纳入了167例侧支循环不良的ICAS患者,结果提示灌注不足或侧支循环不良的患者可能比那些来自穿支闭塞、动脉到动脉栓塞或隐源性卒中的患者从基于支架的再通中获益更多。该研究对侧支循环不良的定义为:与对侧半球相比,狭窄动脉区域的脑血流量下降了40%以上,或者美国介入和治疗神经放射学会/介入放射学会(ASITN/SIR)侧支血流量评分<3分。
同样,1项多中心研究纳入了300例侧支循环不良且随访超过1年的ICAS患者,结果提示低灌注或侧支循环不良的患者可能比其他发病机制(如穿支闭塞)的患者从血管内治疗中受益更多,该研究评估侧支循环不良的标准为术前2周内影像学检查确定责任动脉区域血流动力学障碍,采用以下任一标准:
①CTP显示前循环病变较对侧脑血流灌注下降≥30%,后循环病变较前循环灌注下降≥30%;
②基于DSA的ASITN/SIR评分<3分;
③MRI显示血流动力学缺血性病变;
④单光子发射CT显示低灌注;
⑤TCD显示责任血管的收缩期峰值速度≥200 cm/s,且可以探测到的侧支血管少于1支。
综上,血管内治疗的术前评估侧支循环非常重要的,侧支循环不良的ICAS患者可能会从血管内治疗中获益更多。
(1)手术时机:ICAS患者在急性缺血性卒中发生至少2周后行血管内治疗可能是安全的(进展性卒中除外)(C-LD级证据,中等推荐)。
(2)侧支循环:对ICAS的患者,进行术前的侧支循环评价对筛选合适的手术患者是有益的,术前影像学评估侧支循环较差的患者可能更适合血管内治疗(C-LD级证据,中等推荐)。
(3)针对ICAS患者的病因、狭窄部位的形态学分析选择个体化血管内治疗会有更好的获益(C-EO级证据,中等推荐)。
围手术期血压管理:多项多中心、前瞻性研究均建议将患者围手术期收缩压控制在100~120 mmHg,长期血压控制在收缩压<140 mmHg(糖尿病患者<130 mmHg)。急性、亚急性血栓形成是ICAS血管内治疗围手术期常见的并发症,并与抗栓药物的使用情况密切相关。
1项单中心研究提示预防性输注血小板膜糖蛋白Ⅱb/Ⅲa受体拮抗剂可以降低术中急性支架内血栓形成(AIST)的发生率,且不会增加围手术期脑出血的风险和30 d的总死亡率,然而在减少围手术期缺血事件方面没有优势。
该研究共选择分析236例匹配患者,其中替罗非班组和非替罗非班组各118例。接受替罗非班治疗的患者仅有1例发生AIST,而非替罗非班组AIST有8例。替罗非班组AIST的发生率显著低于非替罗非班组(0.8% 对 6.8%,P=0.039)。2组围手术期缺血事件(8.5% 对 5.1%,P=0.424)、颅内出血(4.2% 对 0.8%,P=0.219)和30 d总死亡率(3.4% 对 0,P=0.125)差异无统计学意义。
另1项单中心研究提示静脉滴注血小板糖蛋白膜Ⅱb/Ⅲa受体拮抗剂对ICAS支架置入期间的AIST是有效和安全的,且不增加出血并发症和死亡发生率。该研究共纳入194例患者,其中12例发生AIST,对于AIST的患者给予血小板糖蛋白膜Ⅱb/Ⅲa受体拮抗剂抢救治疗,所有患者均实现再通,无出血并发症或死亡。因此,血小板膜糖蛋白Ⅱb/Ⅲa受体拮抗剂预防性应用于ICAS患者血管内治疗的围手术期可能是获益的,但仍需多中心、前瞻性RCT进行临床验证。
(1)围手术期血压管理及抗血小板、抗凝治疗应用未更新,同2018版。
(2)围手术期麻醉方式、并发症管理未更新,同2018版。
(3)围手术期应用血小板膜糖蛋白Ⅱb/Ⅲa受体拮抗剂,在减少血栓并发症,尤其预防术中急性支架内血栓形成方面可能是获益的,但仍需高级别临床研究证据来证实(C-LD级证据,弱推荐)。
罕见病诊疗指南——抗 LGI1 抗体相关脑炎【神经系统罕见病】
《中国卒中学会关于无症状性颈动脉狭窄筛查的科学声明》在线发布
ISC 2022前沿速递|应用西洛他唑双联抗血小板治疗对卒中二级预防影响的性别差异
ISC 2022|续写新篇章 —— “替奈普酶”精彩继续……
查看更多