查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





骨髓增生异常综合征(MDS)是一组异质性疾病,其中,较高危(higher risk,HR-)[修订版国际预后积分系统(IPSS-R)评分>3.5分]MDS患者的预后差,传统疗法疗效有限1-3。在近期召开的2024年欧洲血液学学会(EHA)年会上,虽然发布了很多关于MDS的最新临床试验结果,但部分免疫治疗、靶向治疗在HR-MDS的研究以失败告终或未能达到主要终点4,5。
在MDS中,异柠檬酸脱氢酶(IDH)1/2突变的发生率为3.6%~10.2%6,7,IDH1/2突变在HR-MDS中比在较低风险(lower risk, LR)MDS中检出频率更高,这些患者更易进展为侵袭性的恶性肿瘤[如急性髓系白血病(AML)]8。如何改善IDH突变HR-MDS患者长期预后是临床亟待解决的一个瓶颈问题。2023年IDH1抑制剂艾伏尼布获得美国食品药物管理局(FDA)批准治疗难治/复发(R/R)MDS9,为HR-MDS患者带来了曙光。本期内容特邀中国医学科学院血液病医院(中国医学科学院血液学研究所)肖志坚教授,分享艾伏尼布在MDS中的最新进展,以飨读者。
MDS是一组起源于造血干/祖细胞(HPSC)的髓系恶性疾病,具有高风险向AML转化,HR-MDS患者接受目前药物治疗的疗效有限,异基因造血干细胞移植(allo-HSCT)是唯一可能治愈该病的方法,但是由于患者高龄和合并症以及供者等因素,接受移植的MDS 患者比例较低2。去甲基化药物(HMA)阿扎胞苷(AZA)和地西他滨仍是HR-MDS的标准一线治疗选择,但完全缓解(CR)率仅为10%~20%2,中位生存期仅1.5年3,HMA治疗失败的HR-MDS患者预后更差,中位生存期只有4.5个月2。在近期召开的2024年EHA年会上,免疫治疗等新型治疗方案是HR-MDS研究的热点,但取得的进展有限。
一项随机、双盲、多中心、III期试验(ENHANCE研究),共纳入了539例初治的HR-MDS患者,评估了CD47单抗莫洛利单抗(Magrolimab)联合AZA与安慰剂(PBO)联合AZA一线治疗HR-MDS患者的疗效和安全性,结果显示:莫洛利单抗(Magrolimab)联合AZA组与PBO联合AZA组的OS分别为15.9、18.6个月(P=0.13),CR率分别为21.3%、23.6%(P=0.52),研究未达到主要终点(OS和CR率),且≥3级治疗相关不良事件(TEAE)发生率更高4。
另一项随机、双盲、PBO对照、III期试验(STIMULUS-MDS2研究),共纳入了530例HR-MDS(N=492)或慢性粒单核细胞白血病(CMML)-2患者,评估了靶向TIM-3受体的单克隆抗体Sabatolimab(SABA)联合HAM对比PBO联合HAM一线治疗的疗效,结果显示:虽然SABA联合HAM在OS(22.31 vs 18.83个月,p=0.0825)、无进展生存期(PFS)(13.6 vs 10.1个月)、无白血病生存期(LFS)(19.4 vs 13.7个月)、和CR率(19.6% vs 14.3%)方面有更好的趋势,但却未达到主要终点(OS)5。因此,临床需进一步探索HR-MDS的有效治疗方案。
艾伏尼布是一种口服靶向IDH1突变的小分子抑制剂,已被中国国家药品监督管理局(NMPA)批准用于治疗IDH1突变的成年人R/R AML,同时FDA批准联合AZA治疗IDH1突变初诊AML10。一项在我国开展的AG120-C-001桥接研究首次评估了艾伏尼布治疗成年人R/R AML患者的效果与安全性。研究结果显示,艾伏尼布单药治疗CR/完全缓解伴部分血液学恢复(CRh)率为36.7%,CR/CRh患者的中位缓解持续时间为19.7个月11。
AG120-C-001研究中,还纳入了18名R/R MDS患者,根据IPSS-R评分,中等风险占比42.1%,高危和极高危患者分别占比15.8%,其亚组分析结果显示:CR+PR为38.9%,ORR为83.3%,Kaplan-Meier预估中位OS为35.7个月(95% CI, 13.1~NE);5/7(71.4%)和3/4(75%)在基线时分别依赖红细胞和血小板输注的患者,治疗之后脱离了血制品输注,9/11(81.8%)和14/14(100%)在基线时分别不依赖血红细胞和血小板输注的患者,在治疗之后仍然保持非输血依赖12。基于AG120-C-001研究结果,2023年FDA批准艾伏尼布用于治疗R/R MDS9。尽管该药尚未在我国获批R/R MDS适应症,但基于国外已有数据,中国临床肿瘤学会(CSCO)发布的《恶性血液病诊疗指南(2024)》推荐IDH1/2抑制剂联合AZA方案治疗复发、进展或无反应MDS患者(Ⅰ级推荐);推荐IDH1抑制剂单药治疗血清EPO浓度>500IU/L MDS患者(Ⅲ级推荐)(表1)13。此外,在最新更新的《美国国立综合癌症网络(NCCN)临床实践指南:MDS》中艾伏尼布单药治疗方案已被推荐用于中、高、极高危MDS患者的治疗(图1)14。
表1. CSCO指南基于预后(危险度)分层治疗建议
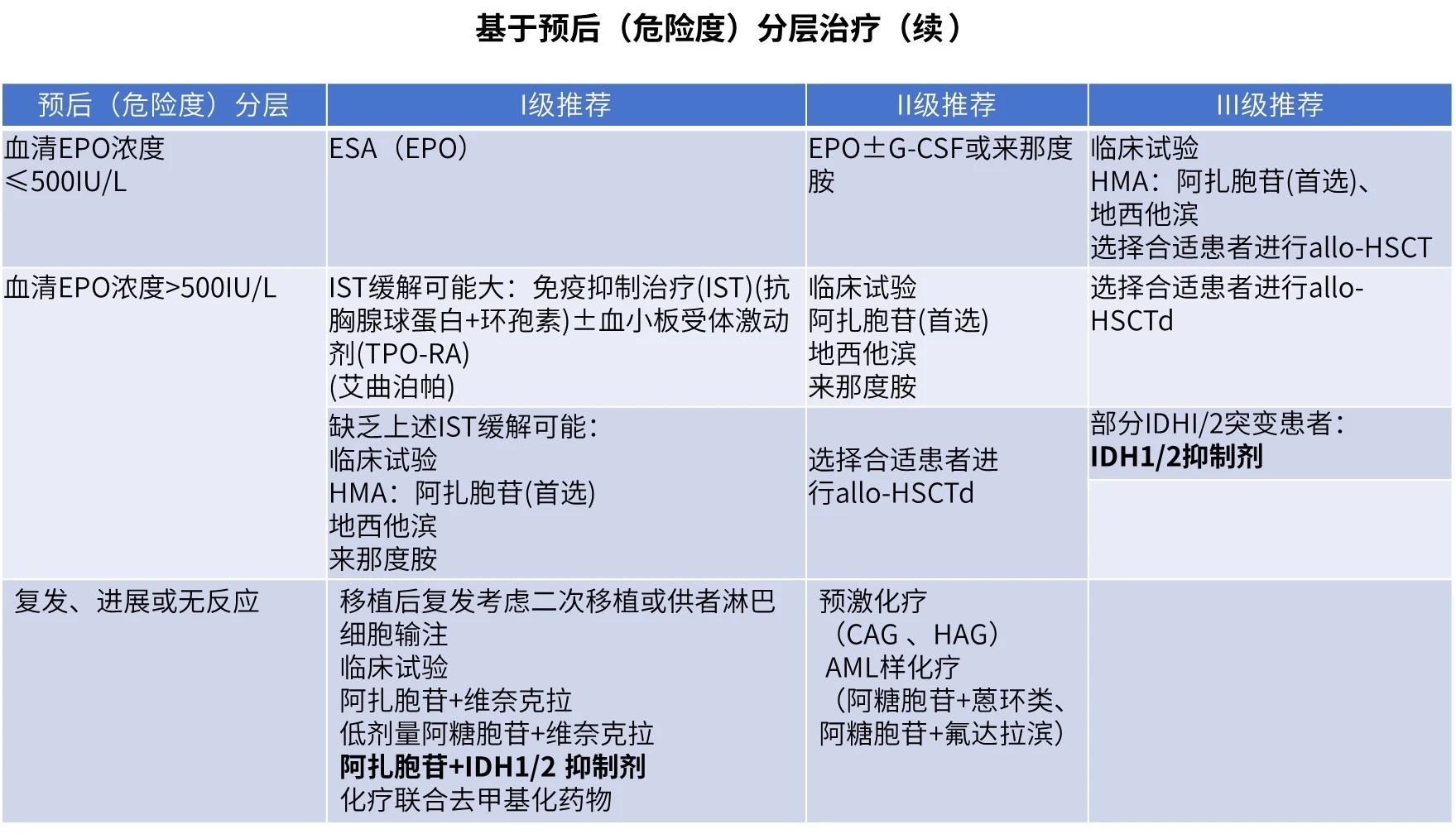
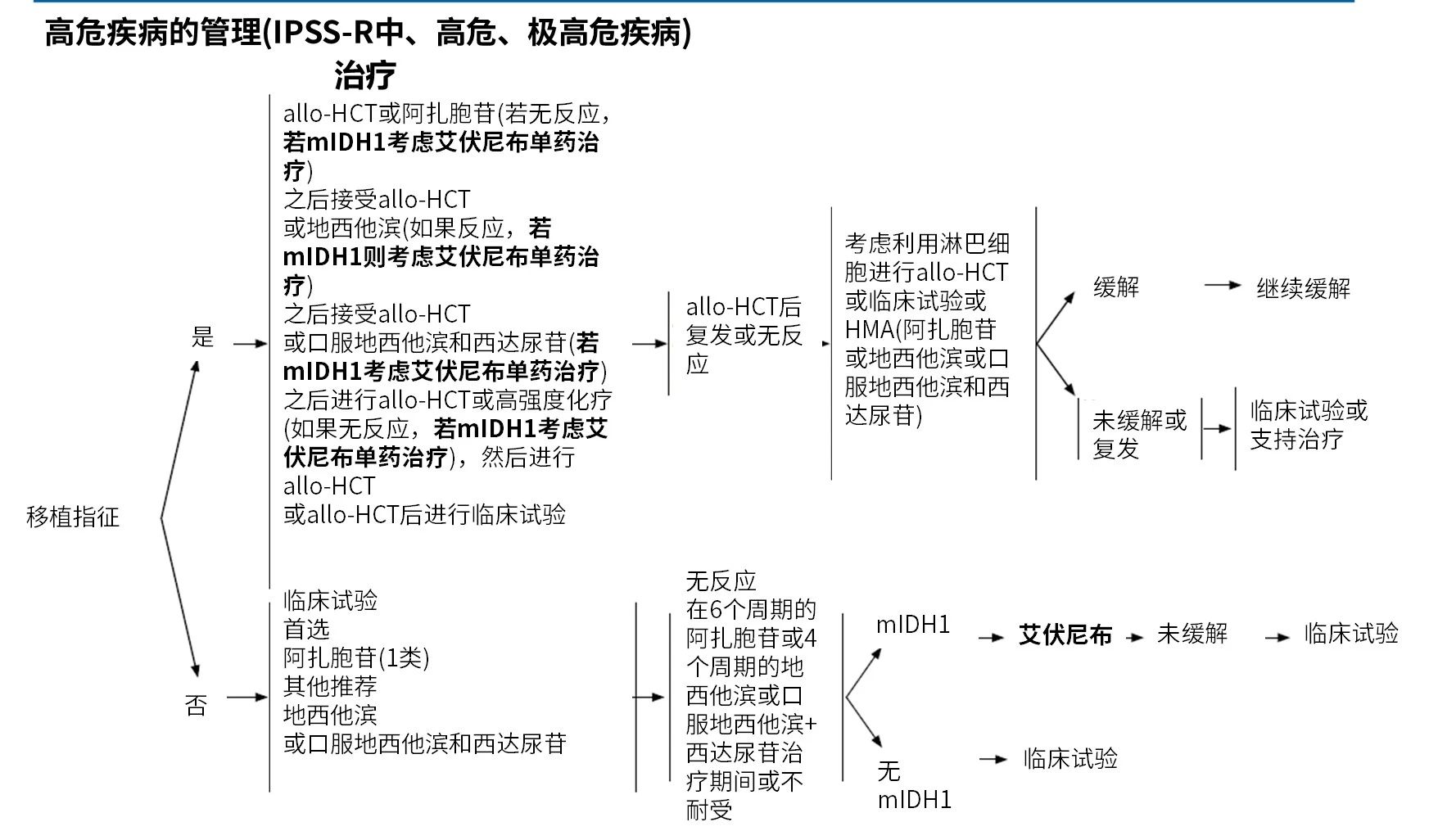
图1. NCCN指南关于高危患者的治疗建议
近日召开的2024EHA年会公布了艾伏尼布在IDH1突变MDS人群中开展的IDIOME研究的最终分析结果,为临床提供了重要参考。
IDIOME研究评估了艾伏尼布在3个MDS队列中的应用情况:A队列:HR-AZA治疗失败(R/R);B队列:一线治疗HR-MDS;C队列:LR-R/R EPO队列。研究目的是评估艾伏尼布在HR-MDS队列的ORR以及在LR-R/R EPO队列的安全性。
A、B、C队列受试者均接受连续28天的艾伏尼布500 mg(口服,一天一次)治疗。在B队列中,艾伏尼布治疗3个周期后,按IWG2006疗效标准评估未达缓解,则联合AZA(75 mg/m2/d x 7天,SC)治疗。主要终点:6个月内的总体血液学反应(OR);次要终点包括:安全性、反应持续时间(DOR)、OS期和评价生物标志物对反应作用的转化项目。
在2019年3月至2023年2月期间,共筛选了64例患者,其中48例患者纳入研究(A、B、C队列分别为22、23和3例),其中43例患者可评价主要终点。中位年龄76.5岁,50%为女性。根据世界卫生组织(WHO)2016诊断标准,MDS伴多系发育不良(-MLD)3例(6%),MDS伴原始细胞增多(MDS-EB)1型5例(10%),MDS-EB2型23例(48%),慢性粒单核细胞白血病(CMML)1例(2%),低原始细胞AML 16例(33%)。国际预后评分系统(IPSS-R)评分低、中、高、极高危分别有3例(6%)、12例(25%)、14例(29%)和19例(40%)(表2)。IDH1突变类型有p.R132C(60%),p.R132H(17%),p.R132S(13%),p.R132G(8%)以及p.R132L(2%)。筛查时骨髓IDH1突变的中位变异等位基因频率(VAF)为21%。
在队列A中,63.6%的患者在3个周期后达到ORR(图2),其中CR 3例(21%),PR 1例(7%),血液学指标改善(HI)10例(71%),中位DOR为4.8个月。截至数据截止日期(2023年9月),20例患者(主要因为疾病)死亡,2例治疗后仍存活(图3A)。中位OS为8.9个月,12个月OS率为15.2%。
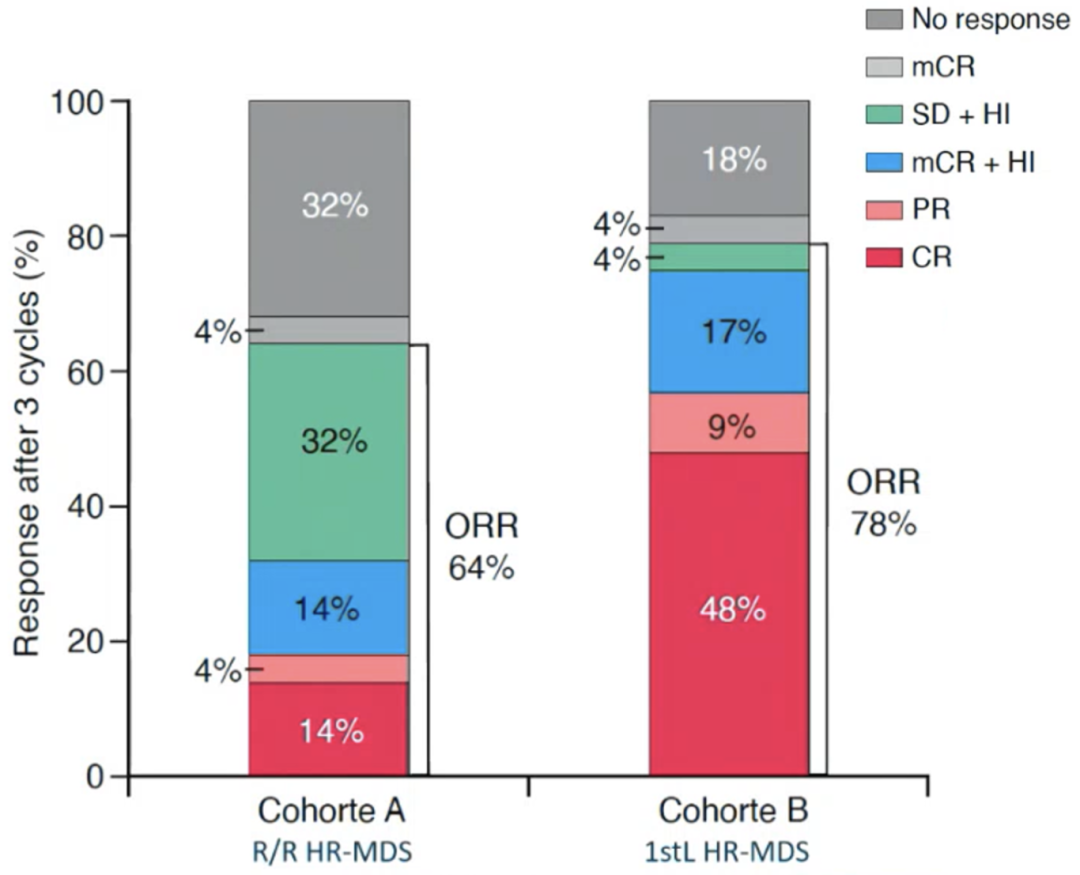
图2. 艾伏尼布单药治疗3个周期后队列A、B患者的缓解情况
在队列B中,78.3%的患者3个周期治疗后达到ORR(图2),其中CR 11例(61%),PR 2例(11%),HI 5例(28%)。仅3例患者在3、3、5个周期后联合AZA治疗,但未获得进一步缓解。5例患者已移植。截止数据时,8例患者已死亡,4例造血干细胞移植(HSCT)后CR仍存活,8例CR存活并且仍在接受治疗,2例进展后存活,1例CR仍存活(图3B),但第13周期后因校正的QT间期(QTc)延长停用艾伏尼布。中位随访25.2个月,中位OS和DOR均未达到,12个月OS率为91.3%。
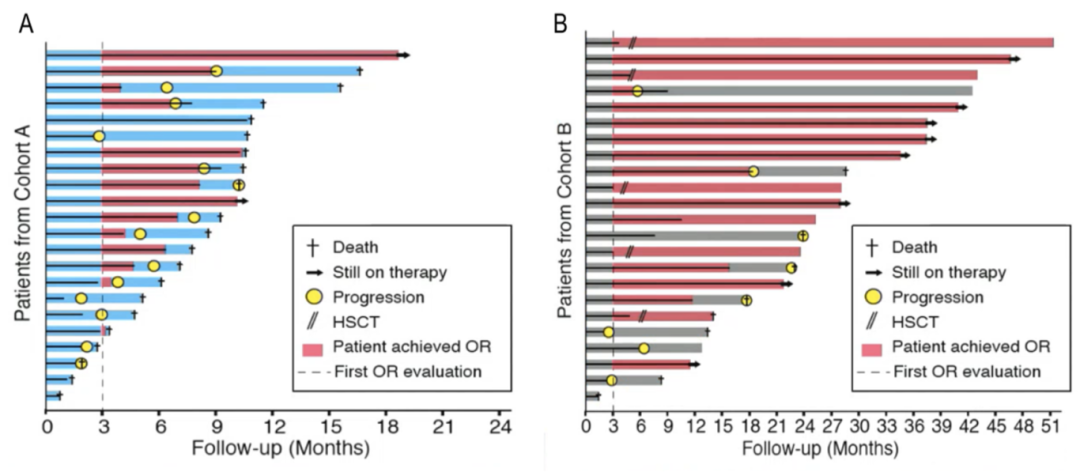
图3.(A)队列A和(B)队列B患者的治疗及生存情况
在队列C中,3例患者中2例分别在第3个和第9个治疗周期时获得CR。1例患者入组后共接受了13个周期治疗,DOR 10个月,并于入组2年后因疾病进展死亡。其余2例患者均为无进展生存,1例患者在治疗20周期后仍处于CR状态。
安全性:9例患者发生与治疗相关的不良事件(AE),主要是分化综合征,在所有病例中均可逆。
此研究提示,艾伏尼布单药治疗伴有IDH1突变MDS患者可实现较高的缓解率,且治疗相关的不良事件发生率低。在初治HR-MDS患者中观察到的高OR率和OS延长,表明艾伏尼布单药治疗可作为伴有IDH1突变HR-MDS患者包括HSCT候选者的一线治疗方案。
纵览2024年EHA年会关于MDS最新进展,免疫治疗、靶向治疗等新型治疗方案仍在积极探索中,艾伏尼布已获FDA批准用于IDH1突变的R/R MDS患者,而在其一线治疗HR-MDS患者的初步评估结果中,ORR达到78.3%,12个月OS率91.3%(包括HSCT候选者),期待HR-MDS患者的治疗迎来更多突破性进展。

肖志坚 教授
主任医师、教授、博士生导师
中国医学科学院血液病医院(血液学研究所)副院所长
中国医学科学院血液病医院MDS诊疗中心和病理中心主任
中华医学会血液学分会副主任委员
中华医学会血液学分会白血病淋巴瘤学组组长
主攻研究方向为髓系肿瘤,特别是骨髓增生异常综合征和骨髓增殖性肿瘤的发病分子机制和临床诊治新策略,在NEJM、Cancer Discov、Blood等杂志发表SCI论文一百余篇
获“新世纪百千万人才工程”国家级人选和“全国优秀科技工作者”等称号
《中华血液学杂志》、《国际输血及血液学杂志》和《白血病•淋巴瘤》杂志副主编,《Blood Review》《Gene,Chromosomes and Cancer》等杂志编委
参考文献:
1.Hochman MJ, et al. Clin Lymphoma Myeloma Leuk. 2024 Mar 18:S2152-2650(24)00113-7.
2.王红颜,邹兴立. 基于维奈克拉的联合治疗方案在较高危骨髓增生异常肿瘤患者治疗中的研究进展[J]. 国际输血及血液学杂志,2023,46(06):540-546.
3.刘柳,和凤,徐衍,等. 维奈克拉联合去甲基化药物治疗较高危骨髓增生异常综合征83例疗效与安全性分析. 中华血液学杂志,2024,45(03):277-283.
4.Sallman D, et al. 2024 EHA. Abstract: S181.
5.Zeidan AM, et al. 2024 EHA. Abstract: S180.
6.Lin J, et al. Ann Hematol. 2012 Apr;91(4):519-25.
7.佟红艳,胡超,余梦霞,等. 骨髓增生异常综合征患者IDH1和IDH2基因突变的临床意义. 中华医学杂志,2013,93(40):3180-3184.
8.王庚,田执梁.骨髓增生异常综合征治疗药物的研究进展[J].现代药物与临床,2022,37(02):433-438.
9.https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-ivosidenib-myelodysplastic-syndromes
10.中国临床肿瘤学会(CSCO)白血病专家委员会. 艾伏尼布治疗异柠檬酸脱氢酶1突变成年人急性髓系白血病临床应用指导原则(2023年版)[J]. 白血病·淋巴瘤,2023,32(11):641-646.
11.Sun M, et al. Blood Sci. 2024 Jun 20;6(3):e00196.
12.Final phase I substudy results of ivosidenib in patients with mutant IDH1 relapsed/refractory myelodysplastic syndrome
13.中国临床肿瘤学会指南工作委员会, 《中国临床肿瘤学会(CSCO)恶性血液病诊疗指南2024》
14.NCCN Myelodysplastic Syndromes Guideline. Version 2.2024
15.Sébert M, et al. 2024 EHA. Oral Presentation: S182.
审批号:M-TIBSO-CN-202407-00019
查看更多