查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






美国芝加哥当地时间5月31日~6月4日,第55届美国临床肿瘤学会(ASCO®)即将拉开帷幕。本届年会的主题为“为患医治,以患为师(Caring for Every Patient, Learning from Every Patient)”,我们由此可以充分体会,全世界临床肿瘤学家对于患者的关爱之情及谦卑之心。
作为临床肿瘤学界最负盛名的国际学术交流平台,来自全世界共约32,000名肿瘤学家,将汇聚于芝加哥麦考密克(McCormick)大厦,分享近一年来肿瘤学领域的最新进展,交流诊治经验。
本次年会将有超过2400篇研究在会议现场进行报告,《中国医学论坛报》记者,仍将一如既往奔赴会议现场,携手参会的中国专家代表,为您带来第一手的会议现场报道,精彩不容错过!

当地时间6月2日上午,“胃肠道肿瘤(非结直肠癌)”口头报告专场(Oral Presentation Session),将报告白蛋白紫杉醇联合吉西他滨对比吉西他滨,用于胰腺导管腺癌术后辅助化疗的国际 III 期、多中心、开放标签的随机临床研究(摘要号4000),本报特邀上海交通大学胰腺癌诊治中心、上海交通大学医学院附属仁济医院王理伟教授针对这项研究进行点评。

研究简介

APACT:白蛋白紫杉醇联合吉西他滨对比吉西他滨,用于胰腺导管腺癌术后辅助化疗的国际 III 期、多中心、开放标签的随机临床研究
背景
前期临床研究已证实在转移性胰腺癌中,白蛋白紫杉醇(nab-P)联合吉西他滨(G)治疗较单用吉西他滨,可延长患者总生存(OS)期。APACT 研究聚焦于白蛋白紫杉醇联合吉西他滨,在可手术切除的胰腺癌患者中,治疗的有效性和安全性。
方法
纳入标准:经组织学证实,肉眼完全切除且未接受过辅助治疗的胰腺癌患者,东部肿瘤协作组(ECOG)体力活动状态(PS)评分0/1分,肿瘤标志物CA19-9 <100 U / mL。分层因素:切除状态(R0/R1),淋巴结状态(LN +/-)和地理区域。术后12周内开始辅助治疗,患者分别在第1、8、15天接受白蛋白紫杉醇125mg/m2 + 吉西他滨1000mg/m2或G 1000mg/m2单药治疗,28 天/周期,共 6 周期。主要研究终点是独立评价员(IR)根据基线临床数据,评价无病生存(DFS)期,次要研究终点是总生存(OS)期和安全性。
结果
共866例患者随机入组,中位年龄为64岁(34~86岁);ECOG PS 0分患者占60%,LN阳性患者占72%,R0患者为76%。69%的患者完成了6周期的治疗(白蛋白紫杉醇联合吉西他滨组为66%,吉西他滨单药组为 71%)。OS的中位随访时间为38.5个月,IR评估的中位DFS(439例)在联合治疗组和单药组分别为19.4 个月对 18.8 个月(HR 0.88,95%CI,0.729~1.063,分层log-rank 检验P = 0.1824)。研究者评估的DFS(571例)在联合治疗组和单药组分别为16.6 个月对 13.7 个月(HR 0.82,95%CI,0.694~0.965,nominal P = 0.0168)。中期分析OS(427例),联合治疗组和单药组分别为40.5个月对 36.2个月(HR 0.82,95%CI,0.680~0.996,nominal P = 0.045)。3 级及以上治疗期间不良事件(TEAE)的发生率联合治疗组和单药组分别为86%和68%,最常见的3 级及以上血液学和非血液学TEAE分别是中性粒细胞减少症(联合治疗组和单药组分别为49%对43%)和疲劳(联合治疗组和单药组分别为10%对3%)。两组均出现了2例不良事件所致死亡。
结论
IR评估的联合治疗组DFS并没有显著性长于单药治疗组,单药组的中位DFS较历史资料更长。研究者(敏感性分析)评估的DFS和中期OS显示,联合治疗组优于单药治疗组(两者的HR均0.82)。对不适合FOLFIRINOX方案治疗的患者,白蛋白紫杉醇联合吉西他滨可能是辅助化疗的一种选择。
专家点评
APACT研究结果显示,白蛋白紫杉醇联合吉西他滨可能成为胰腺癌辅助化疗的可选方案,在探索“老药新用”的同时,我们也要继续开展新药研发,为胰腺癌患者的治疗带来新的希望。
胰腺癌一线治疗现状
FOLFIRINOX方案、白蛋白紫杉醇联合吉西他滨(AG)方案是目前胰腺癌一线治疗最常选择的治疗方案,两者均能显著改善晚期胰腺癌患者的生活质量和生存期。2018年ASCO大会报道、后续发表在新英格兰医学杂志(N Engl J Med)的PRODIGE 24/CCTG PA.6临床研究中,mFOLFIRINOX在胰腺癌辅助治疗中大放异彩,今年 AG 方案的中期结果也如期而至。mFOLFIRINOX(mOS为54.4个月)确实能使部分体能状况好、分期较早患者获益,但其较高的3~4级不良事件发生率(75.9%)也限制了其在临床上(尤其对亚洲人群)的应用。
APACT研究的意义
APACT是首个评估白蛋白紫杉醇在胰腺癌术后辅助治疗中疗效的大型III期临床研究,该研究选择DFS作为主要终点。尽管IR评估的DFS在两组中没有显著差异,研究者分析的DFS和OS,联合治疗组均优于吉西他滨单药治疗,提示白蛋白紫杉醇联合吉西他滨有可能成为胰腺癌辅助化疗的可选方案。
吉西他滨、吉西他滨联合替吉奥(5-Fu类)、AG方案和FOLFIRINOX是胰腺癌的一线用药,随着吉西他滨、吉西他滨联合替吉奥、吉西他滨联合卡培他滨在胰腺癌辅助治疗中的广泛应用,临床肿瘤学家开始探索同种药物或方案在不同治疗中的效果,尝试“老药新用”。目前胰腺癌的临床研究中“老药新用”的探索确实使部分患者获益,例如mFOLFIRINOX用于胰腺癌的辅助治疗。作为胰腺癌药物临床研究的一个新思路,“老药新用”更大程度地利用了现阶段为数不多的药物。在期待APACT研究最终结果的同时,我们也应该意识到,现阶段胰腺癌新药匮乏这一严峻现实,热门的免疫治疗在胰腺癌中疗效不容乐观,这促使我们反思,应结合胰腺癌发生发展机制的基础研究,多角度、多途径地开展转化和临床研究,研发更多新药,为胰腺癌的治疗带来新的突破。
附:近年来胰腺癌辅助化疗临床研究结果一览
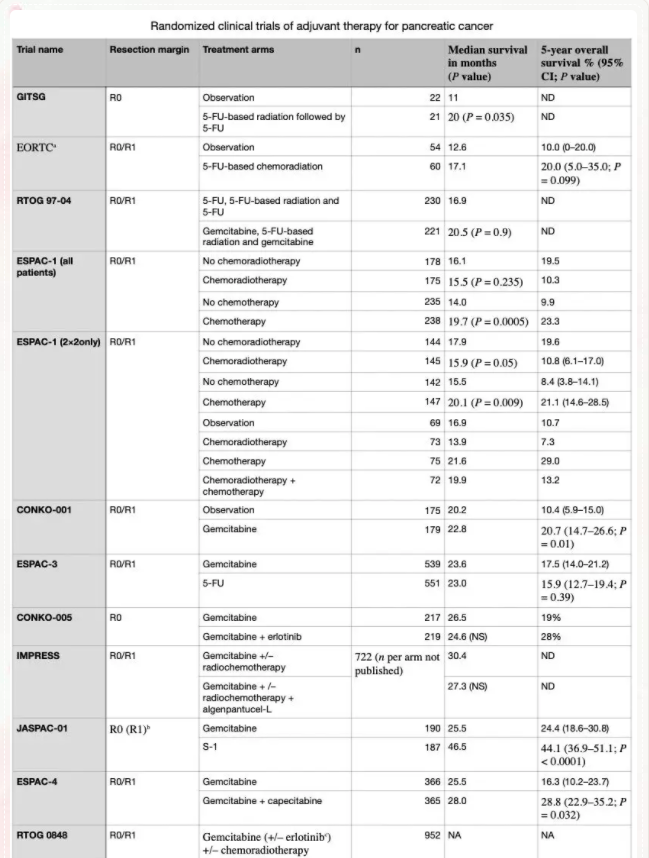

作者 | 毛铁波 崔玖洁 王理伟(上海交通大学胰腺癌诊治中心 上海交通大学医学院附属仁济医院)
编辑 | 刘婷(中国医学论坛报)
查看更多