查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





肠杆菌目细菌可引起呼吸道、泌尿道、血液等部位的感染,是引发医院感染的主要病原菌之一1。随着碳青霉烯类药物在临床的广泛使用,碳青霉烯类耐药肠杆菌目细菌(CRE)的检出率呈快速上升趋势,已成为当前临床面临的重大威胁2。2019年美国疾病预防与控制中心(CDC)公布的抗生素耐药威胁报告,将CRE列为紧急威胁级病原体3。

中国细菌耐药监测网(CHINET)数据显示,2005年-2024年,肺炎克雷伯菌对亚胺培南和美罗培南的耐药率分别从3.0%和2.9%上升到22.6%和23.4%,大肠埃希菌对亚胺培南和美罗培南的耐药率分别从1.1%和1.4%上升到2.0%和2.3%,总体耐药率呈现上升趋势4。
产碳青霉烯酶是CRE最常见、也是最危险的耐药机制1。2024 CHINET数据显示,临床分离出的碳青霉烯类耐药肺炎克雷伯菌(CRKP)以产肺炎克雷伯菌碳青霉烯酶(KPC)为主,而碳青霉烯类耐药大肠埃希菌(CR-ECO)和碳青霉烯类耐药阴沟肠杆菌(CR-ECL)以产金属β-内酰胺酶(MBL)为主(图1)5。一项中国多中心病例对照研究,对全国92家医院的4641例成人血液病患者进行的结果分析显示,在414株CRE分离株中,69.6%(288/414)的CRE菌株产碳青霉烯酶;其中新德里金属 β-内酰胺酶(NDM)是主要类型,占73.0%6。
图1 2024年CHINET 临床分离的CRE菌株碳青霉烯酶酶型分布5
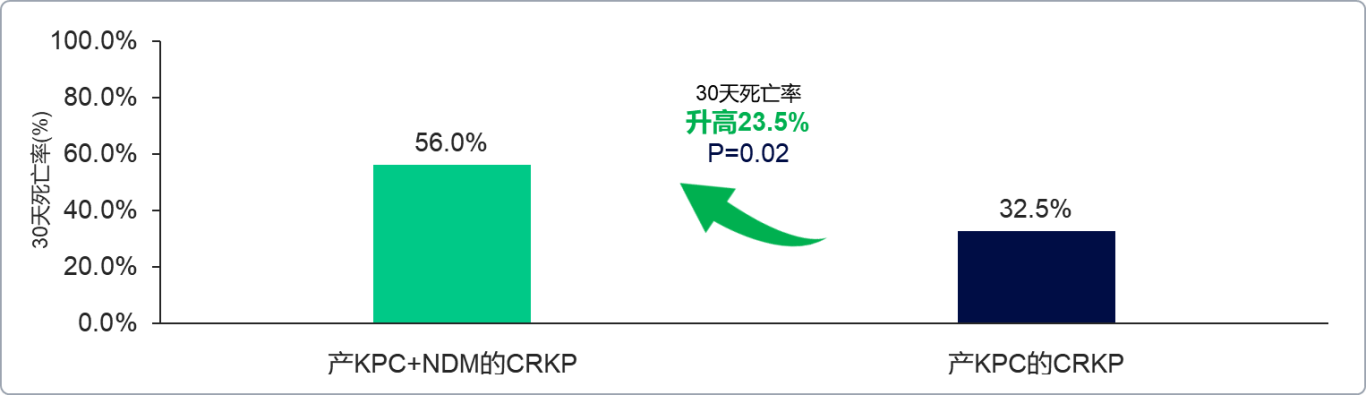
产MBL的细菌感染与不良临床结局相关7。一项中国回顾性研究显示,产KPC+NDM的CRKP所致血流感染(BSI)患者的30天死亡率较产KPC的CRKP高23.5%(56.0% VS 32.5%,P=0.02)(图2)8。MBL具有广泛的底物选择性,可催化水解包括青霉素类、头孢菌素类以及碳青霉烯类在内的双环β-内酰胺类抗菌药物9。目前,只有少数药物或药物组合可以有效克服MBL介导的耐药性,这使得MBL感染的治疗具有挑战性7。
氨曲南-阿维巴坦是目前中国上市的首个可单药治疗产MBL-CRE的新型β-内酰胺类/β-内酰胺酶抑制剂复方制剂10。氨曲南具有独特的单β-内酰胺环结构,使其不被MBL水解,与青霉素结合蛋白(PBP)结合后,可抑制细菌细胞壁肽聚糖合成,导致细菌细胞裂解和死亡11-13。产MBL的菌株可同时产超广谱β-内酰胺酶(ESBL)、C类β-内酰胺酶水解氨曲南12,而阿维巴坦可抑制这些酶,保护氨曲南不被水解12-14。在治疗多重耐药(MDR)革兰阴性菌感染的新型抗菌药物中,氨曲南-阿维巴坦可实现CRE全酶型覆盖15。
研究显示,氨曲南-阿维巴坦治疗肾功能正常、肾功能亢进、轻-中-重度肾功能损害的cIAI及院内肺炎(HAP/VAP)患者在首次给药间隔和稳态时的联合PTA均>90%(表1)16。
表1 氨曲南-阿维巴坦获批的成人剂量方案治疗不同肾功能成人患者的联合PTA16
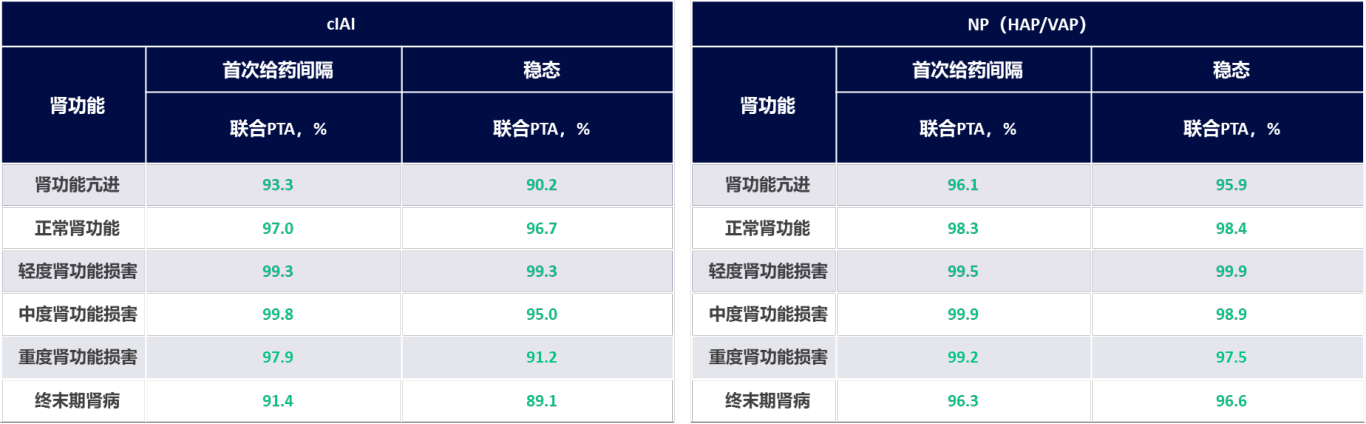
注:血浆暴露联合PTA靶值:氨曲南为60%fT>8mg/L、阿维巴坦为50%fT>2.5mg/L,二者同时达到;肌酐清除率(CrCL)值:肾功能亢进>150 mL/min,正常肾功能>80-≤150 mL/min,轻度肾功能损害>50-≤80 mL/min,中度肾功能损害>30-≤50 mL/min,重度肾功能损害>15-≤30 mL/min,终末期肾病<15 mL/min;PTA:药代动力学/药效学达标概率;cIAI:复杂性腹腔内感染;NP:院内肺炎;HAP:医院获得性肺炎;VAP:呼吸机相关性肺炎
全球Ⅲ期(REVISIT)研究结果显示,在意向治疗(ITT)分析集中,氨曲南-阿维巴坦±甲硝唑*治疗由革兰阴性菌(包含产MBL的MDR细菌)引起的cIAI和HAP/VAP的临床治愈率与美罗培南±黏菌素相当(cIAI:76.4% VS 74%,HAP/VAP:45.9% VS 41.7%),28天全因死亡率数值更低(cIAI:2% VS 3%,HAP/VAP:11% VS 19%),且氨曲南-阿维巴坦耐受性良好,报告的大多数不良事件(AE)均为轻中度17。多项共识推荐氨曲南-阿维巴坦用于治疗产MBL的CRE感染(表2)18-20。
注:±:联合或不联合;*治疗cIAI时,氨曲南-阿维巴坦联合甲硝唑;治疗HAP/VAP时,氨曲南-阿维巴坦不联合甲硝唑
表2 多项共识对氨曲南-阿维巴坦的推荐18-20

综上所述,中国CRE耐药率呈上升趋势,临床分离出的CRKP以产KPC为主,而CR-ECO和CR-ECL以产MBL为主4,5。产MBL的细菌感染常导致不良预后,且治疗选择有限,临床治疗具有挑战性7。氨曲南-阿维巴坦可实现CRE全酶型覆盖15,为CRE感染治疗带来新的突破。多项共识一致推荐氨曲南-阿维巴坦用于治疗产MBL的CRE感染18-20。
| 仅供医疗卫生专业人士阅读/参考
编辑丨梅文秀
1. 辛续丽,等.标记免疫分析与临床,2023,30(10):1695-1699+1800.
2. 全国细菌耐药监测网.中国感染与化疗杂志,2024,24(05):537-544.
3. CDC. Antibiotic Resistance Threats in the United States, 2019. Atlanta, GA: U.S. Department of health and human services, CDC; 2019.
4. CHINET数据云. Available at:https://www.chinets.com/Data/GermYear. Accessed on:2025-7-15.
5. CHINET2024年细菌耐药监测结果. Available at:https://www.chinets.com. Accessed on:2025-7-15.
6. Hu H, et al. Microbiol Spectr. 2024 Jul 2;12(7):e0429923.
7. Grabein B, et al. Infect Dis Ther. 2024 Nov;13(11):2423-2447.
8. Li J, et al. Infect Drug Resist. 2024 May 2;17:1685-1697.
9. Yang Y, et al.Trends Microbiol. 2023 Jul;31(7):735-748.
10. 中华医学会血液学分会,等.中华血液学杂志,2025,46(yufabiao) : 390-402.
11. Wright H,et al. Clin Microbiol Infect. 2017Oct;23(10):704-712.
12. Balaji,Veeraraghavan,et al. Indian journal of medical microbiology,2021,39(3):286-288.
13. 注射用氨曲南阿维巴坦钠说明书(最新版:2025年7月01日).
14. Chauzy A, et al. CPT Pharmacometrics Syst Pharmacol. 2019 Nov;8(11):815-824.
15. Nenad Macesic,et al. Lancet 2025; 405: 257–72.
16. Xie R, et al. Antimicrob Agents Chemother. 2025 Jun 18:e0195024.
17. Carmeli Y, et al. Lancet Infect Dis 2025;25(2):218-230.
18. 中国碳青霉烯耐药肠杆菌科细菌感染诊治与防控专家共识编写组, 等. 中华医学杂志, 2021,101(36): 2850-2860.
19. 胡付品,郭燕,王明贵,等. 细菌药物敏感试验执行标准和典型报告解读(第三版).上海:上海科学技术出版社[M], 2025.
20. 中华医学会血液学分会, 等.中华血液学杂志. 2025,46(6): 390-402.
查看更多