查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






患者,男性,66岁,因“右上腹痛2月”于2022年6月就诊。
现病史 患者于2月前无明显诱因出现右上腹间断性疼痛,无外伤表现,未伴恶心呕吐、头痛头晕、便血等症状。于当地医院东莞市第八人民医院就诊,予行腹部CT提示:1.胃癌肝弥漫性转移,门静脉主干及左右支癌栓,肝中静脉受侵,腹水;2.肝左叶囊肿。肝胆彩超提示:肝脏实质性占位。患者为求进一步系统诊治,于2022年6月拟“肝占位性病变查因”收入院。
既往史 既往有高血压、Ⅱ型糖尿病病史,平素服用“缬沙坦氨氯地平片”、“盐酸吡格列酮片”药物治疗。余无特殊。
个人史、婚育史、家族史 无特殊。
实验室检查 血常规:白细胞 6.76×109/L,血小板 276× 109/L,红细胞 3.92×1012/L,血红蛋白119g/L 。
肝功能:丙氨酸氨基转移酶/天冬氨酸氨基转移酶(ALT/AST)89/181U/L,白蛋白(ALB)35g/L,总胆红素(TBIL)43.2μmol/L。
肿瘤标志物:甲胎蛋白(AFP):299020ng/ml。
乙肝两对半:HBsAg(-)、HBsAb(+)、HBeAg(-)、 HBeAb(-)、HBcAb(+)。
乙肝病毒DNA:阴性。
影像学检查 彩超:肝脏增大,肝内回声改变考虑肝癌,门静脉癌栓形成。
胸部CT:未见明显肺部转移。
上腹部MRI:肝内多发占位,考虑原发性肝细胞癌并肝内多发转移;门静脉主干、左右支近端癌栓形成;腹腔积液。
胃镜 :胃窦前壁可见一溃疡 ,底部覆盖白苔,边界不清,触之易出 血 ,予以取4块送病理(图1)。
病理:(胃窦)低分化腺癌(图2)。
评分 Child-PughB级(7分);ECOG-PS 0分。
初步诊断 1.胃窦癌(中低分化腺癌);2.肝细胞癌?(BCLC C期;CNLC Ⅲ B期)。
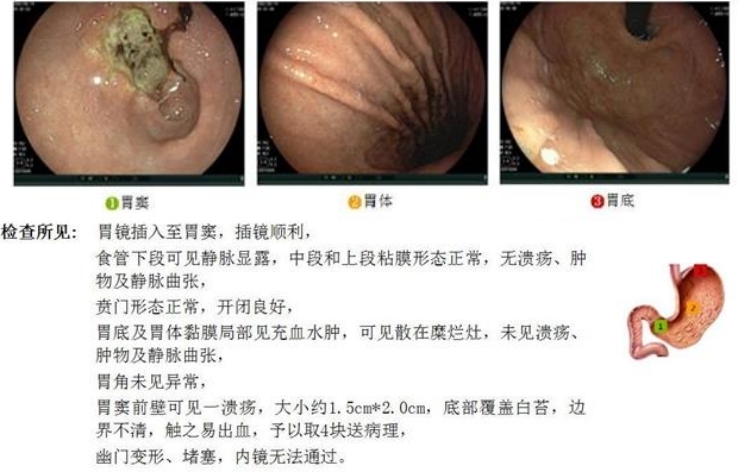
图1 内镜检查(胃窦腺癌)

图2 病理:(胃窦)中低分化腺癌
治疗方案: 肝动脉化疗灌注术(HAIC:氟尿嘧啶+亚叶酸钙+奥沙利铂)+仑伐替尼+替雷利珠单抗+淫羊藿素软胶囊。
疗效评估:
2个疗程治疗后:
肝功能:ALT/AST 36/40U/L,TBIL 15.3μmol/L。
AFP 21138ng/mL。
腹部彩超:门静脉主干约8mm,见侧支血管形成。
腹部MRI检查:肝癌并肝内多发转移瘤治疗后,肝内病灶较前略有缩小(图3)。
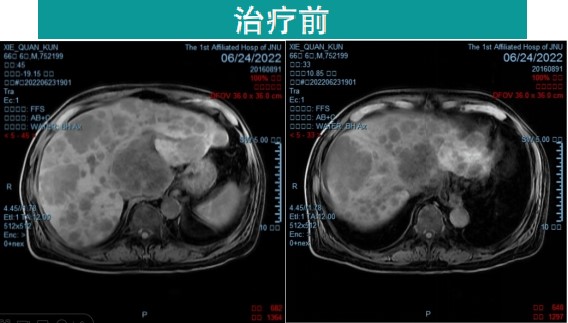
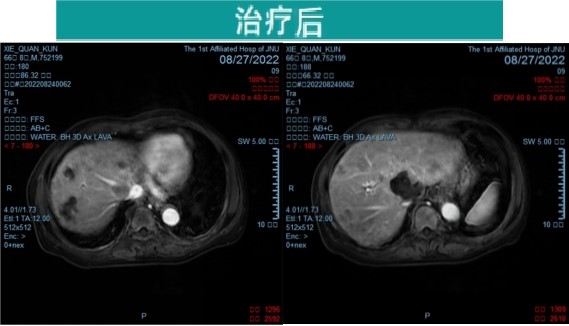
图3 治疗2个疗程前后腹部MRI对比
3个疗程治疗后:
病人感觉良好,心情愉悦,饮食、大小便正常,腹胀腹水消失,睡眠好,体重增加,活动有力。
AFP 10699ng/mL。
复查胃镜:治疗后幽门狭窄改善,且内镜可通过(图4)。
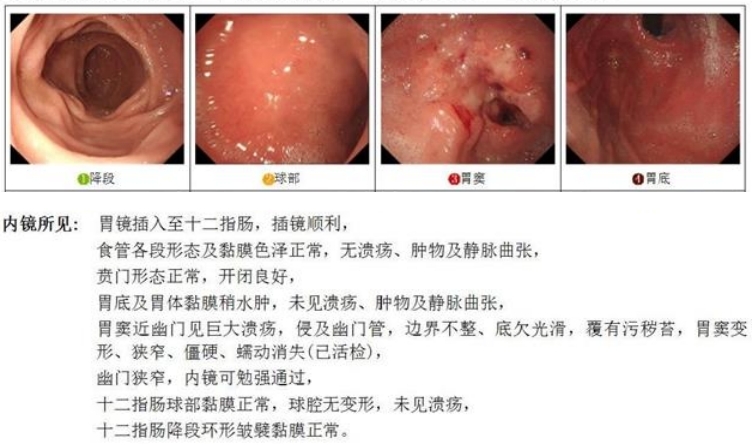
图4 治疗3个疗程后复查胃镜
浙江大学医学院附属邵逸夫医院 梁霄

本病例患者AFP显著升高,虽患者乙肝两对半及乙肝DNA检测均排除乙型病毒性肝炎病史,但结合上腹部MRI明确肝占位性病变,故有诊断为原发性肝癌可能。镜下病理诊断为胃腺癌,胃腺癌的临床表现亦有AFP升高,故在鉴别诊断中应鉴别胃腺癌肝转移可能,但患者拒绝肝脏穿刺以明确肝部病变病理诊断。根据临床经验,考虑采用FOLFOX-HAIC治疗,术后行全身系统抗肿瘤治疗。选用仑伐替尼+替雷利珠单抗+淫羊藿素软胶囊。连续用药3个周期后复查,AFP持续下降且患者感觉良好。同时,治疗后复查胃镜明确幽门狭窄改善,且内镜可通过。治疗后的检查结果及患者主观感受均表明本治疗方案明确有效,且未出现手足综合征、呕吐、疲倦等系统抗肿瘤治疗较为棘手的不良反应。
淫羊藿素软胶囊是创新小分子免疫调节剂,具有独特免疫调节机制。不同于细胞毒类抗肿瘤药物、靶向抗肿瘤药物以及免疫检查点抑制剂类,淫羊藿素软胶囊不单独针对某一分子或靶点,而是通过联合多重机制和靶点进行相互作用,进而通过免疫抑制等通路参与免疫调节,发挥抗肿瘤作用。一方面,淫羊藿素的作用机制是抑制IL-6/JAK2/STAT3信号通路和TLR-MyD88-IKK-NF-κB炎症通路,减少肿瘤坏死因子-α(TNF-α)及白细胞介素-6(IL-6)等炎性细胞因子的产生,改善炎性环境;另一方面,IL-6的减少也会反过来延缓JAK2信号通路的反应1-3。这两条信号通路并不是单独存在的,而是相辅相成,相互作用。此外,淫羊藿素软胶囊还会显著降低髓系来源抑制细胞等免疫抑制性细胞比例,抑制其表达程序性死亡蛋白-配体1(PD-L1),从而恢复T细胞肿瘤杀伤功能,进一步激活适应性免疫。综上,淫羊藿素软胶囊从机制上解读,具有良好的抗肿瘤特性,且与免疫抑制剂有协同增效的可能。本病例中患者应用FOLFOX-HAIC+仑伐替尼+替雷利珠单抗+淫羊藿素软胶囊的局部联合系统抗肿瘤治疗。连续用药3个周期复查后发现,治疗效果好,从临床疗效上再一次印证淫羊藿素联合靶免药物协同增效的可能性。
本病例患者在治疗过程中,未行肝癌穿刺病理诊断,既未明确是否为原发性肝癌合并胃腺癌,亦未明确是否胃腺癌肝转移,但明确其AFP检测呈异常升高。在联合药物治疗过程中,AFP从299020ng/mL骤降至21138ng/mL后继续降至 10699ng/mL,从AFP数值监测肿瘤情况,考虑抗肿瘤疗效显著。曾有研究报道,对235名接受PD-L1治疗的肝癌患者研究分析,AFP降低>50%的HCC患者无进展生存期显著高于AFP降低<50%的患者(P<0.05)4。这提示AFP可作为评估中晚期HCC患者预后的潜在生物标志物。结合淫羊藿素的基础研究报道,其可通过提高miR-620、miR-1236和miR-1270的表达水平从而降低AFP mRNA稳定性和翻译活性,进而降低AFP表达5,6。淫羊藿素软胶囊的Ⅲ期临床研究中,对于AFP>400 ng/mL的患者,其生存获益显著优于对照组。淫羊藿素软胶囊Ⅲ期临床研究数据报道≥3级不良反应发生率仅为12.1%,停药率仅为0.7%7,为患者长期用药提供更为安全的可能。总体而言,淫羊藿素软胶囊区别于传统的系统抗肿瘤治疗药物,是一个具有跨时代意义的创新类免疫小分子调节剂。结合对于癌症患者的长期全身治疗诉求,淫羊藿素软胶囊越早地用于肿瘤患者的系统性治疗,患者获益越长。
1. Liu K, et al. J Clin Med Res. 2016 Apr;8(4):297-302.
1. Bai L, et al. J Dig Dis. 2007 Aug;8(3):154-159.
2. Tan HL, et al. Front Pharmacol. 2016 Jun 29;7:191.
3. Alessandro Annibaldi, et al. Trends in Molecular Medicine. 2018.
4. Sun et al. BMC Cancer (2021) 21:775.
5. Li H, et al. BMC Cancer (2021) 21:318.
6. Zhang C, et al. Oncotarget (2016) 13;7(50):83755-83766.
7. CSCO 2021 Keynote Speech.
查看更多