查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





自2014年问世以来,以PD-1/PD-L1抑制剂为代表的肿瘤免疫治疗,极大地影响了肿瘤治疗的格局,在肿瘤治疗中显示出巨大的应用潜力。在免疫治疗药物研发方面,我国紧跟国际发展步伐,近年来取得了骄人成绩。近日,PD-1抑制剂斯鲁利单抗用于治疗广泛期小细胞肺癌(ES-SCLC)获得美国食品药品监督管理局(FDA)授予的孤儿药资格认定,同时相关适应症的上市注册申请也获得国家药品监督管理局(NMPA)受理。
PD-1抑制剂如何“杀伤”肿瘤?对于极具潜力的斯鲁利单抗而言,其药理特点又有哪些独特之处?本报特邀中山大学肿瘤防治中心李苏教授从临床药理学角度分享其看法及观点。

免疫检查点抑制剂开启新纪元
SCLC生存获益仍有限,亟需突破
PD-1是一种免疫检查点受体,主要表达于T细胞、B细胞、自然杀伤细胞,PD-1与其配体PD-L1在细胞表面的结合可触发抑制信号,向下调节免疫系统对人体细胞的反应,以及通过抑制T细胞炎症活动来调节免疫系统并促进自身耐受。这可以预防自身免疫疾病,但它也可以防止免疫系统杀死肿瘤细胞。
PD-1抑制剂或PD-L1抑制剂可阻断PD-1与PD-L1的结合,恢复T细胞杀伤肿瘤活性,而且一旦抗肿瘤免疫循环建立,可以产生持久的抗肿瘤效应[1]。因此,PD-1抑制剂成为治疗肿瘤的突破口,自全球首个PD-1抑制剂纳武利尤单抗(O药)上市至今,PD-1抑制剂研发热潮经久不衰,并不断创造出新的奇迹。以肺癌为例,2015年,纳武利尤单抗率先获批二线治疗肺鳞癌适应症,随后帕博利珠单抗(K药)、国产PD-1抑制剂等相继发布研究数据,获批适应症由二线前推到一线,极大提升了非小细胞肺癌(NSCLC)的生存预后。
相对NSCLC,PD-1抑制剂在小细胞肺癌(SCLC)中的研发进展迟缓。纳武利尤单抗和帕博利珠单抗在SCLC领域接连折戟,未使广泛期SCLC(ES-SCLC)患者真正获益。PD-1抑制剂斯鲁利单抗横空出世,打破这一窘态,或将成为全球首个一线治疗ES-SCLC的PD-1单抗。
剖析药理特性
斯鲁利单抗匠心巧构,攻守兼备
那么,在国内外已上市PD-1抑制剂不胜枚举的背景下,斯鲁利单抗又“创新”在何处呢?2021年12月,一项斯鲁利单抗的基础研究对其结构和作用特点进行了分析[2]。从药理学层面上来讲,斯鲁利单抗特点可总结为:结构稳定、抗体依赖的细胞毒性作用(ADCC)和补体依赖的细胞毒性作用(CDC)效应弱、有一定抗体依赖性细胞吞噬(ADCP)效应、结合表位面积大、亲和力高、解离慢、抑瘤活性强、免疫原性低。
结构稳定。斯鲁利单抗是一种重组人源化IgG4单克隆抗体(图1)。IgG4分子铰链区很短、二硫键不稳定,会经历Fab臂交换的过程,也就是IgG4特有的“半分子交换”现象,从而产生与抗肿瘤无关的IgG4分子。斯鲁利单抗将野生型IgG4亚类抗体的第228位丝氨酸替换为脯氨酸(S228P),S228P结构改造避免了“半分子交换”现象的发生,使得该药能够稳定发挥药效,避免了临床疗效的不可测性。
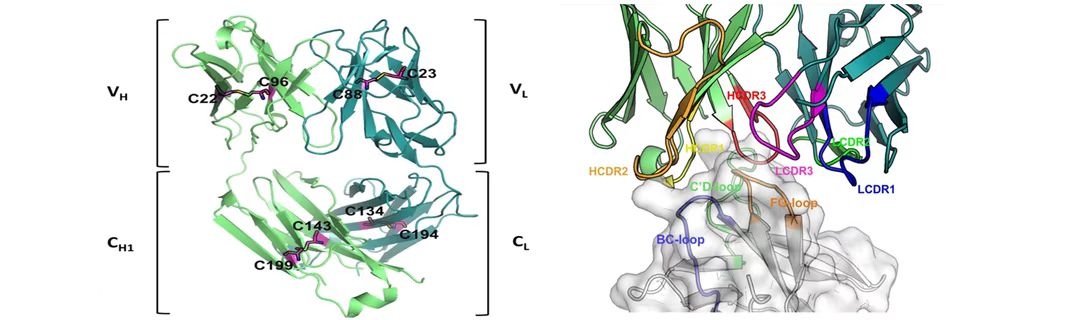
图1:斯鲁利单抗结构示意图
ADCC和CDC效应弱、有一定ADCP效应(图2)。在免疫单抗类药物之前,肿瘤抗体药物多选择IgG1亚型,与表达在靶细胞(肿瘤细胞)表面的抗体结合,借助其介导的ADCC或CDC效应杀伤肿瘤。但PD-1表达在T细胞表面,通过激活T细胞发挥抗肿瘤作用,因此ADCC或CDC效应的存在可能导致T细胞被杀伤。IgG中的IgG4亚型不易引起ADCC和CDC效应,是制备PD-1抗体的最佳类型,也是目前国际主流PD-1抑制剂的抗体类型。斯鲁利单抗为IgG4亚型抗体,ADCC、CDC、ADCP效应弱,有效避免靶细胞即活性T细胞被NK细胞、巨噬细胞等清除,从而保留T细胞对肿瘤细胞的杀伤能力,使斯鲁利单抗发挥更好的抗肿瘤作用。
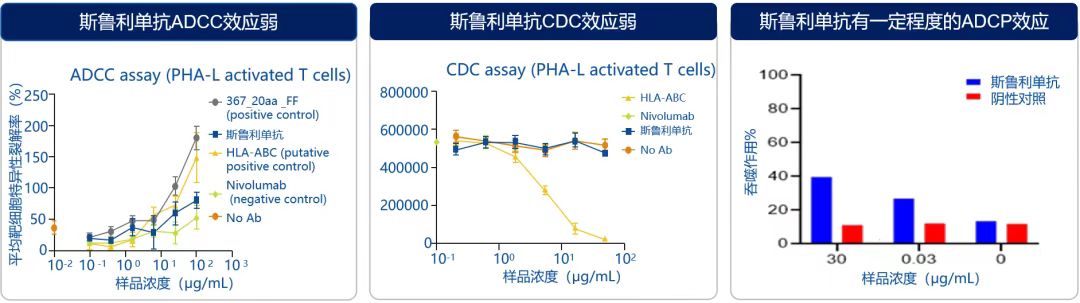
图2:斯鲁利单抗ADCC、CDC、ADCP效应弱
结合表位面积大(图3)。不同的PD-1抑制剂与PD-1分子结合的位点不同,这会导致不同PD-1抑制剂药效的差异。纳武利尤单抗结合的是PD-1分子上的N端环,与PD-L1的结合表位面积为27%;帕博利珠单抗结合的是C’D环,结合表位面积为60%。斯鲁利单抗结合的是PD-1分子上的C’D环和FG环,与帕博利珠单抗较为相似,结合表位面积达55%。
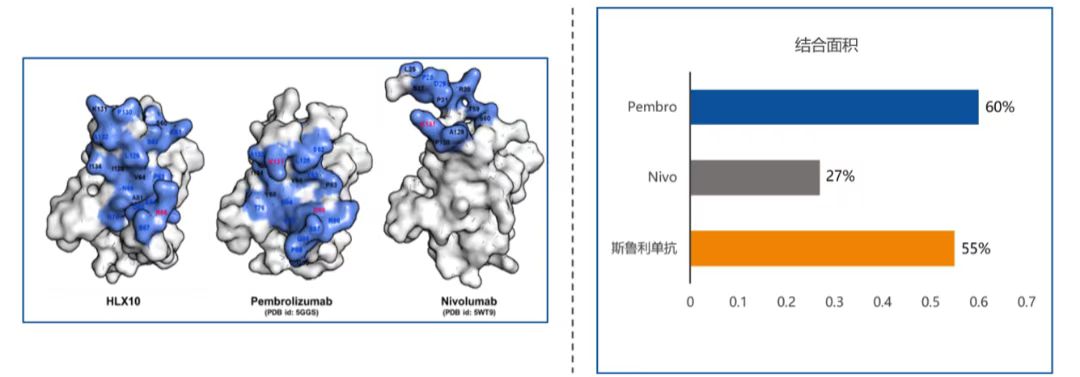
图3:斯鲁利单抗与PD-L1的结合位点、结合表位面积与K药相近
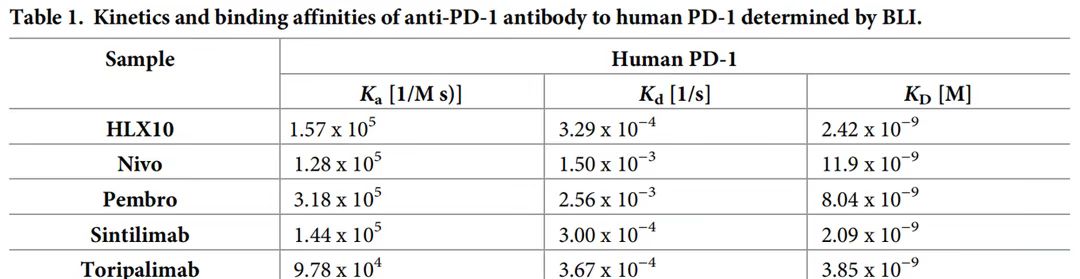
亲和力高,抑瘤活性强。亲和力是影响单抗类药物疗效、临床最佳剂量和部分毒副作用程度的重要因素之一,用平衡解离常数(KD)表征,KD值越小,亲和力越高、解离越慢。研究者通过生物膜层干涉技术(BLI)和表面等离子共振技术(SPR)测定了不同PD-1抑制剂与其靶标的亲和力,结果均证实了斯鲁利单抗与人PD-1结合的高亲和力。BLI检测结果见表1,斯鲁利单抗与人PD-1结合的KD值为2.42×10-9,远远低于纳武利尤单抗(11.9×10-9)或帕博利珠单抗(8.04×10-9)单抗;SPR检测结果显示斯鲁利单抗与人PD-1结合的亲和力比纳武利尤单抗高约10倍(KD:0.32nM vs 3.05nM)。
表1:BLI检测不同PD-1抑制剂与人PD-1的亲和力结果
这表明:斯鲁利单抗具有高亲和力,能够更牢固地结合T细胞上的PD-1,同时缓慢解离,达到恢复T细胞正常功能,阻止肿瘤逃逸的目的。T细胞共培养实验也显示,斯鲁利单抗能促进T细胞的增殖活化,诱导T细胞分泌更多的细胞因子如IL-2(图4),进一步佐证了斯鲁利单抗的抗肿瘤作用。
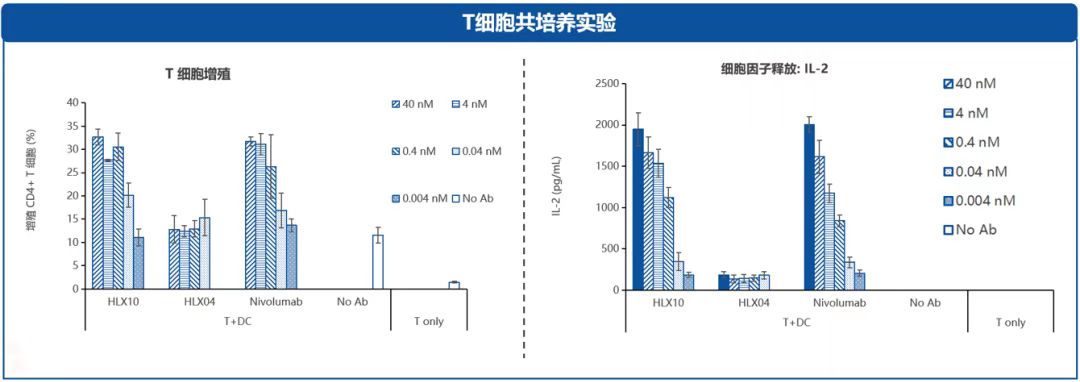
图4:T细胞共培养实验结果
免疫原性低。抗肿瘤药物产生的抗药物抗体(ADA)可能中和药物的生物学活性,或与内源性蛋白产生交叉反应,导致过敏反应甚至细胞因子释放综合征等不良事件,因此药物的免疫原性是其上市时安全性和有效性评审的重要内容。研究显示,斯鲁利单抗的ADA产生率为2.8%,与帕博利珠单抗1.7%相近,远低于其他同类药物,这是该药良好安全性的重要基础。
机制决定疗效
斯鲁利单抗临床数据优异,潜力无限
药物的作用机制是良好临床疗效的基础,斯鲁利单抗凭借独特稳定的药物结构,多维度匹配了理想的PD-1抑制剂模型,铸造了其持久且安全的疗效。2022年3月24日,斯鲁利单抗正式在我国获批上市,用于治疗不可切除或转移性微卫星高度不稳定(MSI-H)的成人晚期实体瘤经治患者。
在SCLC领域,斯鲁利单抗也捷报频传。其联合化疗一线治疗广泛期小细胞肺癌(ES-SCLC)的国际多中心随机对照Ⅲ期研究ASTRUM-005研究达到主要终点,中期分析数据显示,与安慰剂组相比,斯鲁利单抗组的中位OS显著延长(15.4 vs.10.9个月;HR= 0.63, 95% CI 0.49-0.82;P <0.001)。独立影像学评审委员会(IRRC)依据RECIST v1.1标准评估的中位PFS在斯鲁利单抗组显著长于安慰剂组(5.8 vs. 4.3个月;HR=0.47,95% CI 0.38-0.59;P < 0.001)。IRRC依据RECIST v1.1评估的ORR (80.2% vs. 70.4%)和DoR (5.6 vs. 3.2个月)也观察到疗效改善。安全性方面,斯鲁利单抗组和安慰剂组分别有33.2%和27.6%的患者报告了与药物相关的3级以上治疗相关不良事件(TEAE);斯鲁利单抗联合化疗显示出可控的安全性,研究期间未观察到新的安全信号。
凭借ASTRUM-005研究的成功,斯鲁利单抗成为首个在广泛期小细胞肺癌一线治疗获得成功的PD-1抑制剂。2022年4月7日,斯鲁利单抗治疗ES-SCLC获FDA孤儿药资格认证。2022年4月11日,斯鲁利单抗联合化疗一线治疗ES-SCLC的上市注册申请获得国家药监局受理。2022年4月23日,2022版《CSCO小细胞肺癌诊疗指南》公布更新要点,新增斯鲁利单抗联合化疗(EC)方案作为ES-SCLC一线治疗的Ⅲ级推荐1A类证据。
此外,非常值得关注的是,2022美国临床肿瘤学会(ASCO)年会日程近期公布,ASTRUM-005研究从众多研究中脱颖而出,将于北京时间6月5日22:57-23:09由Leading PI、吉林省肿瘤医院程颖教授做线上口头报告,将斯鲁利单抗的风采展现给全球的肿瘤学者,敬请关注。
与此同时,斯鲁利单抗还正在全球同步开展多项免疫联合疗法临床试验,广泛覆盖肺癌、食管癌、头颈癌、胃癌和肝癌等高发大瘤种。铅华褪尽留本色,大浪淘沙始见金,期待未来斯鲁利单抗能够斩获更多适应症,为更多肿瘤患者带来生命之光。
参考文献:
1.Chen Y,et al. Looking for the Optimal PD-1/PD-L1 Inhibitor in Cancer Treatment: A Comparison in Basic Structure, Function, and Clinical Practice. Front Immunol. 2020; 11: 1088.
2.Hassan Issafras et al. Structural basis of HLX10 PD-1 receptor recognition, a promising anti-PD-1 antibody clinical candidate for cancer immunotherapy. PLoS One. 2021 Dec 31;16(12):e0257972.
查看更多