查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





2021年11月6-7日,由中华医学会、中华医学会呼吸病学分会主办,中国医科大学附属第一医院协办的中华医学会第七届全国呼吸危重症学术会议采取“网络在线”的形式召开。本次会议邀请了国内呼吸领域的顶级专家,针对呼吸危重症相关的临床诊疗热点、难点开展全方位、多层次的深入探讨,为大家带来了内容丰富、贴近临床的学术盛宴。
11月6日,中国人民解放军第八医学中心解立新教授以“电阻抗成像(EIT)技术指导的呼气终末正压(PEEP)滴定:问题与展望”为题进行了精彩汇报。
解立新教授介绍,急性呼吸窘迫综合征(ARDS)在重症监护室里非常常见,是处理起来比较棘手的疾病。ARDS能通气的肺是“小”而且是“相对正常(解剖结构有损伤,通气功能正常)”的肺,叫作“婴儿肺(Baby lung)”,这时的治疗目标是抑制肺泡过度膨胀、维持正常通气,但患者同时还存在大面积肺泡萎陷和实变的问题,也要将萎陷的肺泡复张(RM),维持正常的通气-血流(V-Q)交换。
ARDS患者肺部表现的异质性很强,目前静态评估肺部状态变化的主要手段是肺部计算机体层摄影(CT),动态评估肺部状态变化的技术可以使用超声,但是肺部超声不是实时全维度的观察。有没有更好的方法去做个体化呼吸支持治疗是我们需要继续研究的问题。
正压机械通气会导致肺进一步损伤,我们称之为呼吸机相关性肺损伤。人体呼吸过程是负压通气,呼气是负压被动过程,吸气是负压主动过程,正压机械通气使吸气相和呼气相都为正压,必然会导致患者出现压力伤、容积伤、萎陷伤或生物伤等相应问题。进行正压机械通气治疗时,既要维持患者的氧合指数(P/F),又要避免正压机械通气导致的呼吸机相关性肺损伤的问题,这是治疗的根本宗旨。
目前最好的个体化呼吸支持治疗技术是PEEP滴定方法,PEEP滴定的主要方法见图1。

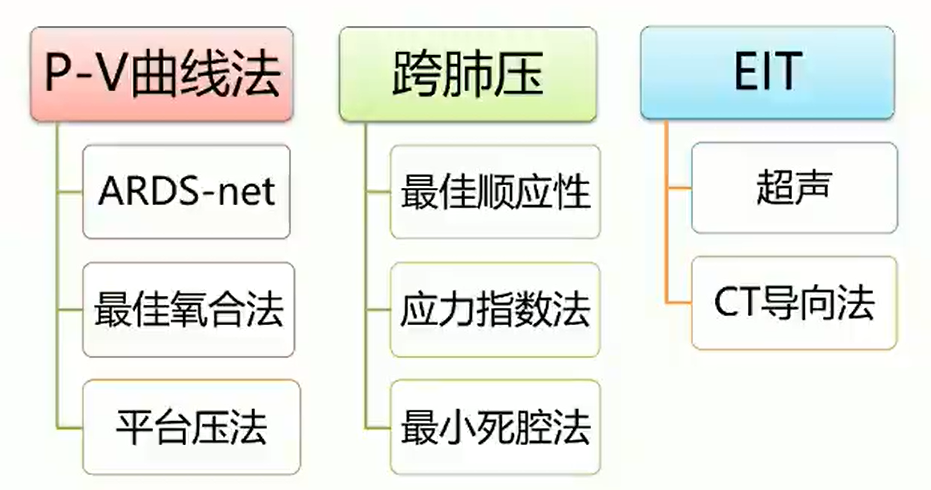
图1
在20世纪90年代,压力容积(P-V)曲线方法非常常用,最佳PEEP是呼气支最大曲率点(PMC)+2 cm H2O,能防止发生呼吸机导致的肺剪切伤。
跨肺压是吸气末或呼气末阻断时测量的肺泡与食道之间的压力差[跨肺压=气道压-食道压(胸膜腔内压平均值近似等于食道压力)]。呼吸机的辅助压监测接口可以连接食道球囊导管,测量食道下三分之一处的食道压。吸气末跨肺压≤25 cm H2O,可避免吸气末肺泡过度扩张,呼气末跨肺压应>0 cm H2O且<5 cm H2O,可维持肺泡开放状态,相关循证医学研究证明以上范围确实能改善患者的氧合情况,但目前并没有大样本、多中心的相关研究能够证明它能降低病死率。
P-V曲线方法和跨肺压方法都是单室模型,这导致它们不能有效反映肺部的异质性和不均一性以及多形性的改变。
EIT技术是指利用生物电阻抗与气体的良好相关性,通过测得胸部电阻抗数值,反映当时肺部的气体容量变化。空间上只能分辨气体和非气体,重在观察气体含量随时间变化而出现的变化,时间分辨率高。
EIT滴定PEEP,目前主要有三种测量指标。
(1)呼气末肺阻抗(EELI)趋势:EIT设备根据患者肺阻抗变化制作的连续线性图像,目前认为恒定的EELI相当于稳定的呼气末肺容积(EELV),也就是最合适患者的PEEP值。
(2)全局不均匀性(GI)指数是根据像素值差异计算的通气均匀性指标,GI越小说明肺通气越均匀。
(3)区域顺应性(Creg)估计过度膨胀和塌陷。
解立新教授提到,基于既往的治疗经验得出,使用Creg估计过度膨胀和塌陷指标进行PEEP时倾向于选择较低的PEEP,而GI指数和EELI趋势则倾向于选择较高的PEEP。
一项发表于2019年关于EIT(使用GI滴定PEEP)与P-V曲线的随机对照试验显示,对重症ARDS患者进行床旁PEEP滴定,与P-V曲线相比,EIT安全且方便,氧合、顺应性、驱动压等指标更好,撤机成功率更高;一项发表于今年关于EIT(使用Creg估计过度膨胀和塌陷滴定PEEP)与P-V曲线的随机对照试验显示,在中、重度ARDS患者中,与P-V曲线相比,EIT指导的PEEP滴定可降低驱动压和死亡率。但目前相关的研究均为小样本研究,仍需要大样本量的研究增强循证医学证据。
一项关于EIT与跨肺压的临床研究显示,在肺源性ARDS中,PEEPEIT引导测得的PEEP值比PEEP跨肺压引导的PEEP值要低;在肺外性的ARDS中,PEEPEIT建议使用更高的PEEP值,从而获得更好的腹侧通气分布,但呼吸系统压力和跨肺压略高。
使用不同方法滴定PEEP的不足见表1。

表1 使用不同方法滴定PEEP的限制

使用EIT滴定PEEP的问题主要有:① EIT单一胸带只能观察60%肺的变化;② 不能动态实时定量评估;③ 不能动态观察血流灌注改变。
为了能使用EIT动态观察肺灌注的改变,目前,临床上也在进行注射高渗盐水的研究。注射高渗盐水会导致血液中盐浓度一过性升高,胸部总阻抗会下降,在阻抗下降的这段时间内,灌注较差的区域(像素)血流量会比灌注正常的区域(像素)的血流量少,可以在一定程度上观察到患者肺的动态V-Q灌注变化,但后期图像处理有一定难度。一项发表于2021年的关于使用盐水造影肺电阻抗成像进行V-Q匹配预测ARDS患者预后的研究显示(50例患者,相对大样本研究),V-Q不匹配的比例越高,患者的死亡风险就越大。这也提示我们,临床中使用盐水造影肺电阻抗成像动态观察血流灌注改变十分有意义。
如果将呼吸机与EIT技术整合,实现实时监测肺通气和肺灌注后,是否可以自动调整至个体的最佳PEEP,目前已有呼吸机厂家对此进行升级,我们期待它的到来;EIT单一胸带只能观察60%肺的变化,因此,能否通过两条绑带实现实时全肺部的通气监测(将两条绑带的图像进行整合),我们联合厂家正在进行动物试验,期待明年能有好消息;我们与清华大学团队合作,将EIT电阻抗图像做成了三维图像,可以将动物的肺通气情况实时全部展现出来,下一步想实现V-Q的三维图像呈现,但要走的路还很长;如果不打高渗盐水,是否可以将EIT和全息投影技术接合,完成实时肺通气及肺灌注的监测,目前相关研究刚刚起步,我们还在不断完善。
最后,解立新教授总结道,在重症监护病房,我们需要建立床旁动态评估呼吸/循环功能的体系,实现异质性ARDS肺部应力/应变的个体化评估,提高我们对ARDS的救治能力。
《中国医学论坛报》整理,转载须授权
查看更多