查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






本期作者:郑方圆
上期话题,我们阐述了儿童慢性髓细胞性白血病(CML)患者的诊断及监测【☜点击可跳转阅读】,本期继续聊聊儿童CML的治疗。
如临床高度怀疑CML,在等待BCR-ABL1融合基因结果前,如患儿有高白细胞血症(白细胞计数>100×109/L),可短期使用羟基脲,用量为20~40 mg/(kg·d),分2~3次服用,以降低白细胞数量,待诊断明确后,可停用羟基脲并换用酪氨酸激酶抑制剂(TKI)。
应根据ELTS风险分层选择药物。对于低危患儿,一线首选伊马替尼治疗,初始剂量为260~340 mg/(m2·d)(总剂量≤600 mg/d)。
对于中、高危患儿,可选用伊马替尼,用法同低危患儿,此外,也可借鉴成人二代TKI一线治疗的经验选用二代TKI作为中、高危CML患儿的一线治疗药物,其中尼洛替尼剂量为230 mg/(m2·次),每12小时1次(单次剂量≤300 mg),达沙替尼剂量为60 mg/(m2·d)(总剂量≤100 mg/d)。
伊马替尼、达沙替尼、尼洛替尼的药物剂型为薄膜包衣片剂或胶囊剂型,因此对于不能吞服片剂或胶囊的CML患儿,可选择口服临时混悬液的方法,如服用伊马替尼或达沙替尼时,可用苹果汁溶解药物并立即服下。
服用尼洛替尼时,可打开胶囊,用苹果酱溶解内容物,空腹时服下。
(向下滑动查看更多)
Castagnetti、Millot等报道CML患儿接受一线伊马替尼治疗的5年无进展生存(PFS)率为92%,5年总生存(OS)率为97%。
Cai等发表的单中心数据显示一线伊马替尼治疗CML患儿的5年OS和无事件生存(EFS)率分别为95.5%和88.9%。
Shao等报道在3、6个月时达最佳反应的CML患儿,在12个月时获得了更高的主要分子学反应(MMR)率和完全细胞遗传学反应(CCyR)率以及4年EFS。
Dou等发表的多中心回顾性研究显示,我国接受一线伊马替尼治疗的CML患儿比成年人患者累积获得CCyR以及分子学反应(MR)4.5的比例更高。
在成人CML患者的随机对照研究中,相对于标准伊马替尼一线治疗,二代TKI一线治疗可更快地获得更深的分子学反应,减少疾病进展。
目前尚罕见在CML患儿中比较伊马替尼与二代TKI一线治疗的随机对照研究,但有研究显示,以二代TKI作为一线治疗的CML患儿获得的分子学反应率与成人相当。
一线使用二代TKI的CML患儿更少发生疾病进展。
CML患儿接受TKI治疗过程中的治疗反应评估包括血液学、细胞遗传学以及分子生物学分析,及时评估治疗反应以及检测早期复发对于优化CML治疗具有重要而积极的意义。
TKI治疗期间,可参考ELN 2020和NCCN的成人CML的疗效评估标准进行治疗反应的评估,并结合患儿耐受性,随时调整治疗方案(表1和表2)。
(点击可查看、保存大图)
▼表1 CML-CP患儿接受TKI治疗反应的定义
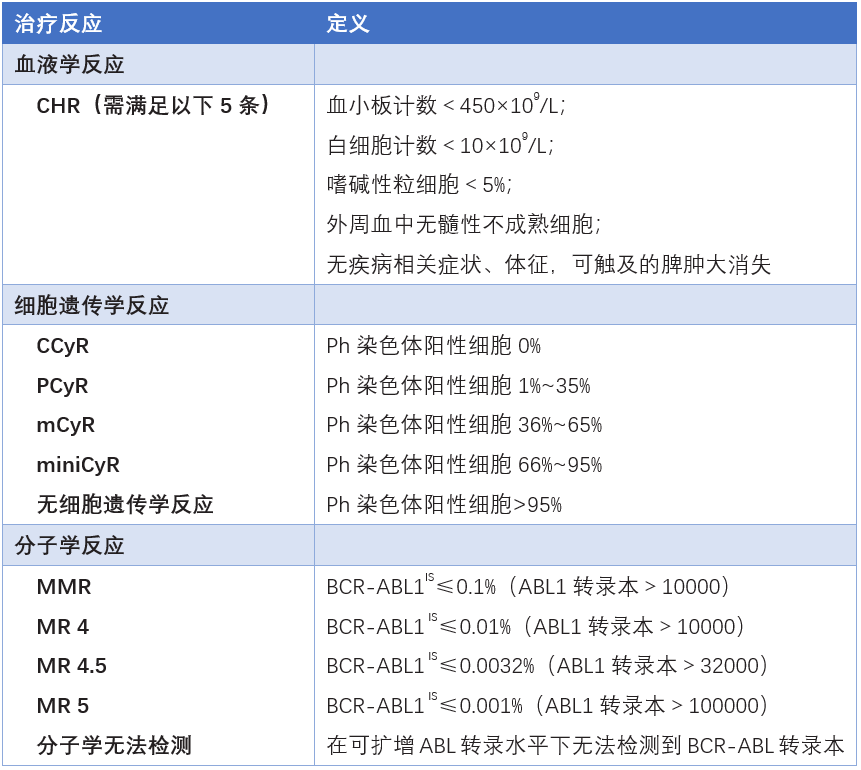
注:CML-CP为慢性髓性白血病慢性期;CHR为完全血液学反应;CCyR为完全细胞遗传学反应;PCyR为部分细胞遗传学反应;mCyR为次要细胞遗传学反应;miniCyR为微小细胞遗传学反应;MMR为主要分子学反应;MR 4为分子学反应4;MR 4.5为分子学反应4.5;MR 5为分子学反应5;IS为国际标准化
▼表3 CML-CP患儿接受TKI治疗反应评估标准(ELN 2020版)
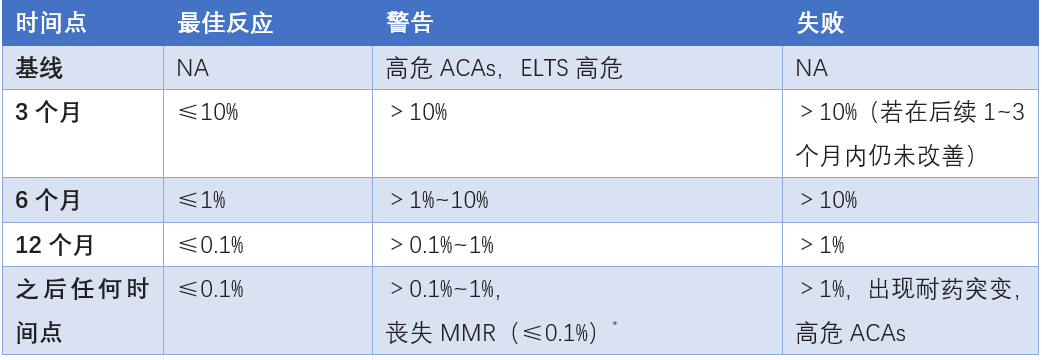
注:CML-CP为慢性髓性白血病慢性期;TKI为酪氨酸激酶抑制剂;NA为不适用;ACAs为附加染色体异常;ELTS为EUTOS长期生存评分;MMR为主要分子学反应;*TKI停药中丧失MMR(>0.1%)意味着治疗失败;表中所有数值均为国际标准化(IS)值
参照治疗反应标准
治疗方案调整建议如下
对于治疗反应处于失败的患儿,应寻找原因(如依从性差、耐药或药物不耐受),依据失败原因方案调整如下:
①对于因依从性差而导致失败的患儿,应采取相应措施提高依从性;
②对于因耐药而导致失败的患儿,应根据BCR-ABL1激酶突变检测结果选择TKI。如若检出F317L、F317V、F317I、F317C、V299L、T315A基因突变,宜采用尼洛替尼;若检出Y253H、E255K、E255V、F359C、F359V、F359I基因突变,宜采用达沙替尼;若检出T315I基因突变,宜考虑使用三代TKI、对T315I敏感的TKI、进入临床试验或进行造血干细胞移植(HSCT);
③对于药物不耐受而导致失败的患儿,应更换其他TKI。
Millot等报道初诊CML-AP和CML-BP患儿的5年OS分别为94%和74%。
借鉴成人研究结果,对初诊为CML-AP患儿,建议应用高剂量伊马替尼或二代TKI作为一线治疗,如果TKI治疗可以达到最佳治疗反应,可以在密切监测下维持原TKI治疗,如果没有达到最佳治疗反应,建议换用TKI,并考虑HSCT。
对于初诊CML-BP患儿,建议应用高剂量伊马替尼或二代TKI作为一线治疗,并根据免疫表型判断髓系或淋系急性变,辅以相应的诱导化疗。
如果初始治疗无效,应考虑选择合适的二代TKI治疗,如果二代TKI耐药(根据突变分析结果)和(或)药物不耐受,应考虑使用三代TKI或参加临床试验。
对于TKI治疗中进展为CML-AP的患儿,应基于BCR-ABL1激酶突变谱、前线治疗和合并症等因素,尽快转换TKI,并开始寻找HSCT供者。
对于所有初诊时为CML-BP或在TKI治疗中进展为CML-BP的患儿,都应在TKI或联合化疗回到CML-CP后尽快进行HSCT,并且HSCT前应密切监测药物治疗效果,建议在分子学反应达到MR 4前,每个月进行外周血分子学检测1次,之后每3个月检测1次。
CML患儿服用TKI后不良反应主要为血液学和非血液学不良反应,血液学不良反应为骨髓抑制,表现为中性粒细胞减少、贫血和血小板减少,多为1、2级,一般不需特殊干预。
伊马替尼导致非血液学不良反应中常见的为胃肠道症状,多可耐受,6%的患儿表现严重而需要停药,比例与成人患者相当。
CML患儿服用尼洛替尼的不良反应的发生率、类型和严重程度与成人相当,肝功能异常发生率略高于成人,但并未观察到明显的心血管事件,血糖升高较成人少见。
CML患儿服用达沙替尼常见的非血液学不良反应为恶心、头痛、腹泻、呕吐,也可见消化道出血、胸腔积液、心包积液、肺水肿或肺动脉高压。
CML患儿接受二代TKI治疗发生的严重不良事件少于成人患者,在成人中列为危险因素的动脉闭塞性疾病、肺动脉高压、心血管疾病、胰腺炎等合并症在儿童中虽然发生率低,但不可忽视。针对CML患儿TKI不良反应的处理可参考成年人。
此外,还需要关注长期TKI治疗对CML患儿生长发育的影响,如TKI可引起生长迟缓、骨代谢变化、甲状腺功能异常、青春期性腺发育延迟和成年人后生育力下降等。
Deng等研究发现,一线伊马替尼治疗CML患儿中,42.9%的患儿出现骨密度下降。
郑方圆等的多中心研究发现在接受伊马替尼治疗的CML-CP患儿中,71%出现身高增长减慢,青春期前服药者更为显著,并且服药初始年龄越小,服药时间越长,伊马替尼抑制身高增长越显著。
二代TKI对儿童生长的影响数据较少,但也观察到相似现象。


在TKI治疗的CML患儿中,治疗依从性差是导致疗效不佳和治疗失败的常见原因之一。
治疗时间长、同时服用多种药物和症状获得缓解等因素是服药依从性差的主要原因。
在CML患儿中多次忘记服药的发生率可达15%,有研究报道青少年CML的依从性更差,且多发生在治疗反应良好后的第1年。


关于TKI治疗期间CML患儿免疫功能的数据较少。TKI治疗有一定的免疫抑制作用,但未达到引起机会性感染的程度,因此不需要常规预防卡氏肺孢子菌肺炎。
大部分CML患儿在TKI治疗期间可以进行免疫接种,接种灭活疫苗通常是安全的,不推荐CML患儿在TKI治疗期间接种活疫苗。
对正在接受TKI治疗的CML患儿,无治疗缓解(TFR)具有非常大的吸引力,但CML患儿的停药研究较少,样本量较小,TFR成功率有待更多研究。建议儿童TKI停药仅可在临床试验中进行。
TKI治疗的CML患儿
健康相关的生活质量
Zheng等报道的一项横断面研究显示,女性、诊断CML时年龄较大、年龄较小、母亲文化程度较低以及存在TKI不良反应是导致CML患儿健康相关的生活质量(HRQoL)较差的显著相关因素。
此外,患儿更关注诊疗过程中的躯体感受以及对外貌的不满意,而父母更关注服药给患儿带来的胃肠道不适和对患儿未来的担忧。


TKI时代CML患儿HSCT的适用情况如下:
CML-CP对≥2 种TKI耐药,如果存在T315I基因突变,尝试对T315I基因突变有效的药物,但仅用于桥接HSCT,应尽快考虑HSCT;
初诊CML-AP,在首选高剂量伊马替尼或二代TKI治疗下,如果可以达最佳反应,暂不考虑HSCT。如果治疗失败,建议考虑HSCT;
初诊CML-BP,在首选二代TKI联合化疗下回到CML-CP后,应尽快接受HSCT;
TKI治疗中进展至CML-AP,根据ABL1激酶突变分析结果选择针对突变类型的二代TKI,并考虑HSCT;
TKI治疗中进展至CML-BP,根据ABL1激酶突变分析结果选择针对突变类型的二代TKI,回到第2次CML-CP后,尽快接受HSCT。

综上所述,儿童CML与成人在临床特征、诊治和结局存在差别,医生需要对CML患儿进行全面评估,在此基础上选择合适的TKI治疗,并进行规范监测。
此外,应重视TKI对儿童生长发育的影响,必要时通过多学科合作,全面提高我国儿童CML临床管理水平。




点击图片进入专题→
第一时间查看更新


儿童血液主治医师
国家血液系统疾病临床医学研究中心
北京大学人民医院
北京大学血液病研究所
查看更多