查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





在肿瘤治疗领域,精准医疗的理念正逐渐改变着临床实践的面貌。胆道恶性肿瘤(BTC)作为一种恶性程度高、预后极差的肿瘤类型,长期以来治疗选择有限,患者面临着严峻的生存挑战。近年来,随着对BTC分子特征的深入理解,HER2等治疗靶点取得了令人瞩目的突破,为该类患者带来了新的希望。本期我们将分享一例HER2阳性的晚期肝内胆管癌治疗案例,其二线治疗应用维迪西妥单抗为基础的联合治疗方案,快速控制疾病,疗效持续达PR,迄今已获得了超过11个月的PFS。让我们在解放军总医院第五医学中心谭招丽教授的分享及解放军总医院第七医学中心李晓松教授的专业点评之中,深入剖析其治疗经过,以期对HER2突变BTC的治疗策略提供更为深入的启示与思考。
病例分享

谭招丽 教授
医学博士,解放军总医院第五医学中心肿瘤内科主治医师
主要研究方向:结直肠癌、胃癌、食管癌等消化道肿瘤的精准治疗及免疫治疗。
负责国家自然科学基金项目1项,主要参与国家自然基金面上项目2项、北京市自然科学基金面上项目1项
一作或通讯作者发表SCI论文6篇,核心期刊4篇,单篇最高影响因子为14.919分,累计影响因子超40分
获国家发明专利1项
获军队专业技术人才岗位津贴
基本情况
男性,76岁,ECOG评分 0分,疼痛NRS 0分。因“上腹部疼痛不适”,于2023年4月17日就诊当地医院,相关检验、检查结果提示(肝右叶)肝内胆管细胞癌。2023-5-12于外院行肝癌切除术、胆囊切除术。2023-10-19在外院行腹部增强CT,提示肝右叶新发强化结节,考虑肿瘤复发。于2023-10-20开始行顺铂+吉西他滨+曲妥珠单抗治疗6周期,2024-04-6复查腹部增强CT提示肿瘤进展,遂至我院进一步诊治。
既往史
既往体健,否认高血压、糖尿病、冠心病等慢性病史,否认乙肝、结核等传染病史,否认外伤史、输血史、冶游史,否认食物药物过敏史,否认烟酒史,否认家族性遗传病史。
辅助检查
2023-4-17腹部彩超(外院):肝右叶大小约8.0 cm*5.8 cm的实性团块,周边及内部可见血流信号。
2023-4-22腹部增强CT(外院):肝右叶可见一外突稍低密度团块影,大小约8.6 cm*6.9 cm,增强扫描显示动脉期可见不均匀强化,门脉及延迟期呈稍低密度影。
2023-4-22甲胎蛋白(外院):4.6 ng/ml。
2023-5-12肝癌切除术、胆囊切除术后病理(外院):(肝右叶)肝内胆管细胞癌,中分化伴大量坏死,多发性,最大为11 cm*8 cm*5.5 cm,最小为1 cm。脉管内癌栓形成。免疫组化结果:HBsAg(-),Hepa(+),CK19(+),GPC-3(弱+),CD34(-),Ki67(+,>75%),EMA(-),CEA(-),GS(+),CDX-2(+),Arginase(-),AFP(-),P53(+),MUC-1(+),CK7(-),CK20(弱+),Syn(-),p40(-),EGFR(灶状+)。PD-L1(SP263)CPS2分,HER2(3+),MSH2(+),MSH6(+),MLH1(+),PMS2(+)。基因检测结果:CCNE1扩增,拷贝数27,CDK4扩增,拷贝数5,ERBB2扩增,拷贝数7,PALB2 13.44%,TP53 34.21%。
2023-10-19腹部增强CT(术后5个月,外院):肝右叶新发强化结节,直径约1.0 cm,考虑肿瘤复发可能。
2024-4-06腹部增强CT(一线治疗后5个月,外院):肝占位综合治疗术后改变,肝S3凝固性坏死;肝S8切缘周围及肝中静脉旁、S1下腔静脉旁多发、新发强化结节较前增大。考虑肿瘤进展。
2024-4-11肝脏CT(我院):
肝中静脉旁
S1下腔静脉旁多发、新发强化结节
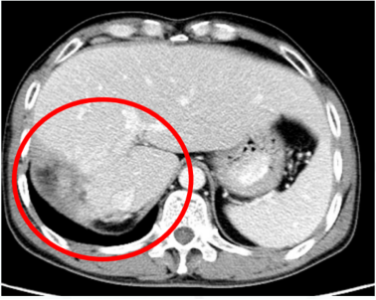
肝S8切缘周围
我院治疗经过
2024-04-12至今于我科行17周期维迪西妥单抗联合特瑞普利单抗治疗。
肿瘤评估:治疗期间,患者的靶病灶持续缩小。治疗11个多月后,患者的靶病灶较基线缩小42.3%,非靶灶稳定,未见新发病灶,综合评效PR。
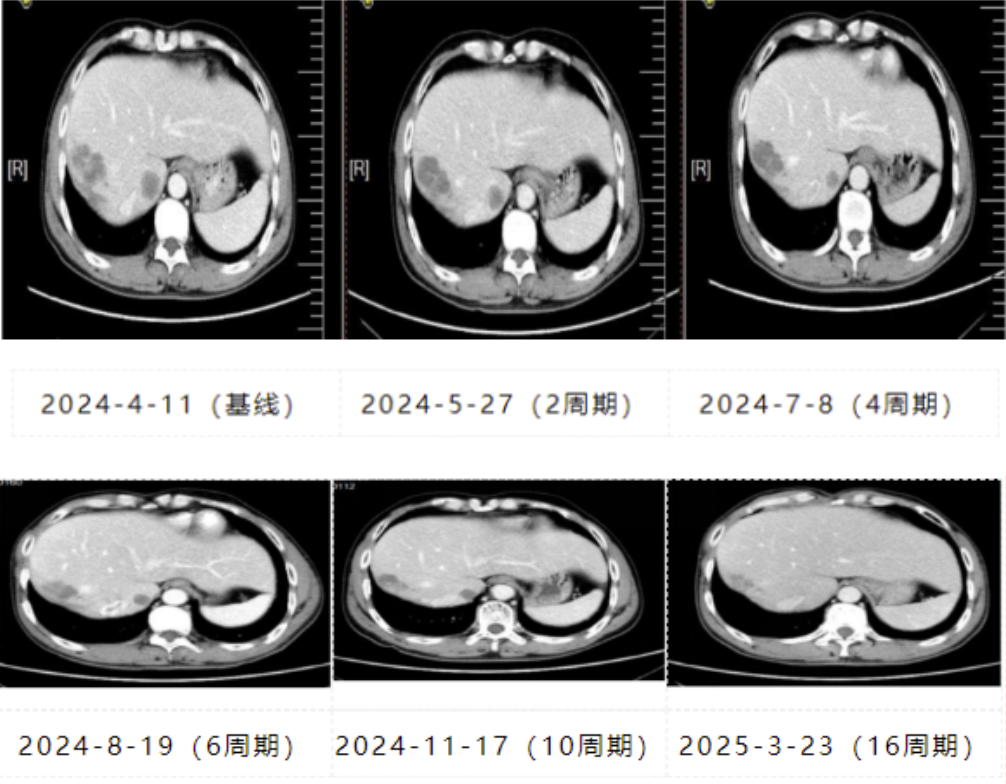
表1. 维迪西妥单抗联合特瑞普利单抗治疗期间靶病灶变化
不良反应评估:1级手足麻木、白细胞水平2度降低、中性粒细胞3度降低。以上不良反应均可管理。
诊疗体会
在面对该例晚期肝内胆管细胞癌患者时,我们深刻体会到了精准医疗在肿瘤治疗中的重要性。患者在外院行根治手术治疗后,就进行了基因检测,提示ERBB2扩增,HER2成为了后续治疗的重要靶点。该患者的病情相对复杂,术后不久便出现了肿瘤复发,并且在一线抗HER2联合化疗方案治疗5个月后,病情迅速进展。在为患者制定二线治疗方案时,我们仍延续了以维迪西妥单抗为基础的抗HER2联合免疫治疗方案。随着治疗的推进,我们欣喜地观察到患者的靶病灶持续缩小,截至最新的随访期(2025-3-23),患者的靶病灶较基线缩小42.3%,疗效评价持续达PR,获得了超过11个月的PFS,且耐受性可。目前,该患者仍遵医嘱接受维迪西妥单抗联合特瑞普利单抗方案治疗,且在严密的随访监测中。
病例点评

李晓松 教授
解放军总医院第七医学中心肿瘤科主任
中国人民解放军总医院肿瘤医学部 主任医师 教授 博士生导师
擅长常见恶性肿瘤的标准化诊疗,在肿瘤精准诊疗、生物靶向及免疫治疗方面具有丰富的临床经验
入选“北京市科技新星”、教育部“国家公派访问学者”
“首都优秀青年医生”、国家重点研发计划项目负责人
中国临床肿瘤学会老年肿瘤防治专家委员会委员
中国临床肿瘤学会肿瘤光动力治疗专家委员会常委
中华医学会激光医学分会委员兼副秘书长
国家自然科学基金、北京市自然科学基金评审专家
国家药品监督管理局医疗器械技术审评专家
国家肿瘤微创治疗产业技术创新战略联盟专委会委员
教育部学位与研究生教育发展中心评估专家
北京医学会医疗损害责任技术鉴定专家
解放军医学科技委员会生物技术专业委员会委员
解放军医学科技委员会激光医学专业委员会委员
BTC涵盖肝内胆管癌(iCCA)、肝外胆管癌(eCCA)、胆囊癌(GBC)和壶腹癌(AC)等多种亚型。其中,胆管癌(CCA)是仅次于肝细胞癌的第二种最常见的原发性肝脏恶性肿瘤,其发病率约占所有原发性肝脏肿瘤的10%~15%[1]。据统计,近数十年来CCA的死亡率呈不断上升的趋势,其中,与西方国家相比,亚洲地区的死亡率更高[2]。
由于其侵袭性本质和症状出现较晚,多数BTC患者在确诊时已处于晚期,肿瘤不可切除或已转移,导致预后不佳,5年总生存率(OS)低于20%。长期以来,晚期BTC的治疗主要依赖吉西他滨与顺铂联合化疗(GC方案)。近期,TOPAZ和KEYNOTE-966等临床试验结果显示,在传统治疗基础上联合免疫检查点抑制剂,可显著延长晚期BTC患者的生存期,因此免疫联合化疗已成为一线治疗方案。然而,仅有不到30%的BTC患者对免疫联合治疗有反应,且缺乏有效的预测免疫治疗反应的生物标志物评估,这可能导致部分患者错过最佳治疗时机和治疗方案。
因此,探索多样化的治疗方案仍是临床亟待解决的问题。在BTC管理中,与靶向治疗相关的靶点基因检测的重要性日益凸显。BTC常见的基因突变包括HER2、BRAF V600E、FGFR2融合以及IDH1/2等。其中,晚期BTC中HER2过表达和扩增约占13%[3]。研究显示,HER2在BTC中的过表达与患者的不良预后密切相关。抗HER2治疗以抑制HER2受体为中心,产生二聚化阻断、磷酸化抑制或细胞内细胞毒素表达,从而阻断下游信号通路(MAPK和PI3K),诱导细胞死亡。目前,已在BTC中报道了多种不同的HER2抑制剂研究,显示出了可观的客观缓解率(ORR,16%-47%)[4]。
本例患者最初因上腹部疼痛不适就诊,检查结果提示肝部占位,经评估后行肝癌切除术和胆囊切除术,术后病理显示(肝右叶)肝内胆管细胞癌,免疫组化结果显示HER2(3+),基因检测提示ERBB2扩增,为后续的治疗方案选择提供了重要的基础。不幸的是,该患者在术后5个月即出现肿瘤复发,一线治疗接受GC方案化疗联合曲妥珠单抗治疗6周期。在治疗5个多月后,复查腹部增强CT发现肝S3凝固性坏死,肝S8切缘周围及肝中静脉旁、S1下腔静脉旁多发新发强化结节较前增大,提示肿瘤进展,一线治疗失败。
《胆道恶性肿瘤HER2分子诊断与临床应用中国专家共识》[5]指出,HER2阳性经治不可切除BTC患者接受抗HER2治疗可显著改善OS和PFS。同时,考虑到患者在一线治疗时已接受双药化疗,身体机能通常受到打击,后续难以耐受高强度抗肿瘤治疗。因此,主治团队在二线治疗中选择了维迪西妥单抗进行HER2靶向治疗,同时联合特瑞普利单抗免疫治疗。
维迪西妥单抗是荣昌生物自主研发的一款ADC,同时是我国首个原创ADC,它可通过特异性结合HER2蛋白,将细胞毒性药物直接递送到肿瘤细胞内,从而提高治疗效果并减少对正常细胞的损害。其于2021年6月9日由国家药品监督管理局(NMPA)宣布上市,适应证为至少接受过 2 个系统化疗的HER2过表达局部晚期或转移性胃癌(包括胃食管结合部腺癌)的患者和既往接受过含铂化疗且HER2过表达局部晚期或转移性尿路上皮癌的患者。此外,它在广泛瘤种中也展现出了较强的抗肿瘤作用,包括肠癌、泌尿、乳腺、阴茎癌、乳房外paget等,相关成果接连在美国临床肿瘤学会(ASCO)、欧洲肿瘤内科学会(ESMO)、欧洲肿瘤内科学会亚洲会议(ESMO-ASIA)重磅会议及European Urology Oncology、European Journal of Cancer、Cancer Medicine等重磅期刊上亮相。
在维迪西妥单抗联合治疗方案下,患者的肝内病灶较前持续缩小,在超过11个月的规律随访中,靶病灶较基线缩小42.3%,非靶灶稳定,未见新发病灶,疗效评价持续达PR。截至最新的随访期(2025-3-23),患者已获得了超过11个月的PFS,且仍在规律治疗,持续获益中。同时,患者在用药期间发生的不良事件均可控,安全性和耐受性良好。
综上所述,从该病例展示了维迪西妥单抗联合方案在HER2阳性胆管癌二线治疗中的显著疗效和可管理的安全性,其为难治的晚期肝内胆管癌患者争取了更长的生存获益。未来,随着更多临床研究的开展和经验的积累,维迪西妥单抗联合治疗方案有望在HER2阳性胆管癌治疗中发挥更大的作用。
参考文献:
1. Banales JM, Marin JJG, Lamarca A, et al. Cholangiocarcinoma 2020: the next horizon in mechanisms and management. Nat Rev Gastroenterol Hepatol. 2020;17(9):557-588.
2. Ferlay J, Ervik M, Colombet M, et al. Global Cancer Observatory: Cancer Today. Lyon, France: International Agency for Research on Cancer. Published 2020. Accessed September 30, 2021.
3. Nam AR, Kim JW, Cha Y, et al. Therapeutic implication of HER2 in advanced biliary tract cancer. Oncotarget. 2016 Sep 6;7(36):58007-58021.
4. Ten Haaft BH, Pedregal M, Prato J, Klümpen HJ, Moreno V, Lamarca A. Revolutionizing anti-HER2 therapies for extrahepatic cholangiocarcinoma and gallbladder cancer: Current advancements and future perspectives. Eur J Cancer. 2024;199:113564.
5. 中国抗癌协会胆道肿瘤专业委员会,中国临床肿瘤学会胆道肿瘤专家委员会. 胆道恶性肿瘤HER2分子诊断与临床应用中国专家共识(2024版)[J]. 中国实用外科杂志,2024,44(12):1321-1327.
本文由谭招丽教授和李晓松教授审核
查看更多