查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






庄成乐 博士
上海市第十人民医院胃肠外科副主任医师,主任助理
外科学博士,同济大学研究生导师,同济大学研究员
上海市第十人民医院匠心工程培养人才
擅长胃肠肿瘤的微创手术治疗和综合治疗
获得首届国际NOSES手术视频大赛亚军
中华医学会肠外肠内营养学分会第六届委员会青年学组副组长
中国抗癌协会肿瘤营养专业委员会常务委员
中国抗癌协会肿瘤营养专业委员会新苗委员会副主任委员
上海市抗癌协会肿瘤营养专业委员会秘书长兼青年副主委
主持国家自然科学基金2项,上海市卫健委等课题5项
以第一或通讯作者发表SCI论著35篇,累计影响因子超过200分
省部级医学科技奖一等奖及科技进步奖二等奖各1项
以第一发明人获得国家发明专利1项
病史简介
患者男性,60岁,2017-12-23因“大便习惯改变2月”来我院消化内科就诊,完善相关检查后提示:
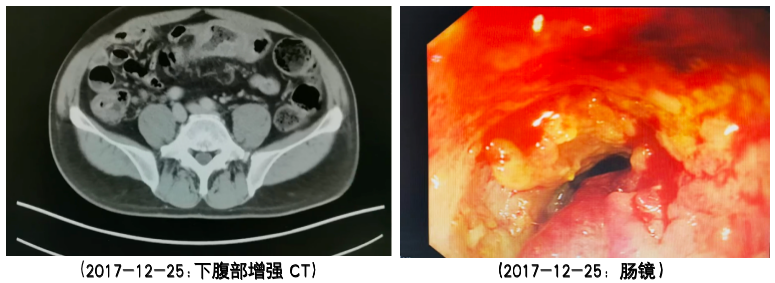
下腹部增强CT(2017-12-25):乙状结肠肠壁明显不规则增厚,病变累及浆膜面,与邻近腹膜关系密切;系膜多发小淋巴结,转移待排。
进一步完善肠镜(2017-12-26):距肛门约30cm结肠见一隆起型病变,表面凹陷糜烂,质脆,边界欠清,占整个肠腔2/3周,管腔狭窄,内镜不能通过。
肠镜病理:结肠黏膜腺体高级别上皮内瘤变。
血检:
CEA 11.08ng/ml,
CA199 71.32U/ml,
CA125 57.85U/ml,
CA724 81.2U/ml,
遂以乙状结肠肿瘤收治入院。
入院时查体:患者神志清楚,无贫血貌,皮肤巩膜无黄染,腹软,无压痛及反跳痛,肠鸣音正常,未及明显包块,Virchow’s LN(-)。
肛诊:未见明显异常。
第一次手术及术后化疗
患者完善检查后于2018-01-05行:腹腔镜下乙状结肠肿瘤根治术,手术顺利,术后7天康复出院。
石蜡病理:中分化腺癌,部分黏液腺癌,大小4.5x3.5cm,浸润至浆膜外脂肪组织;上下切缘:均未见癌组织累及;肠旁淋巴结转移情况:1/15;病理分期:pT4N1M0,ⅢB期。
患者于手术后3周开始行Capox方案化疗,累计8次。期间患者血检提示肿标轻度升高,影像学检查未见明显复发转移征象。
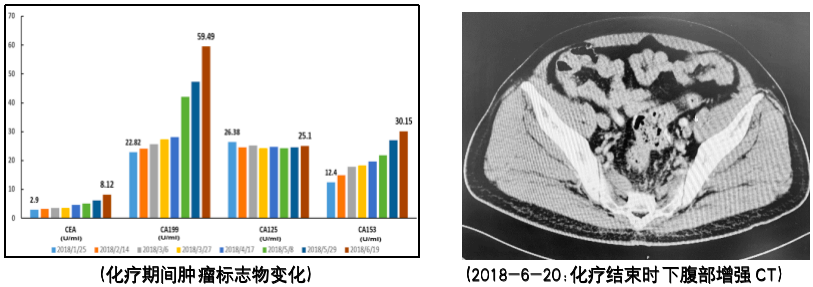
术后随访2年:肿瘤指标回升
影像学未见明显复发转移征象
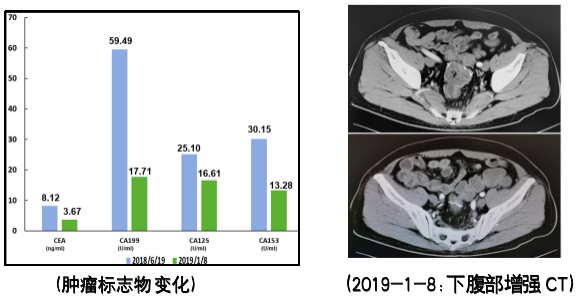
术后1年(2019-1-8)随访:肿标显著下降;影像学检查未见复发转移征象。
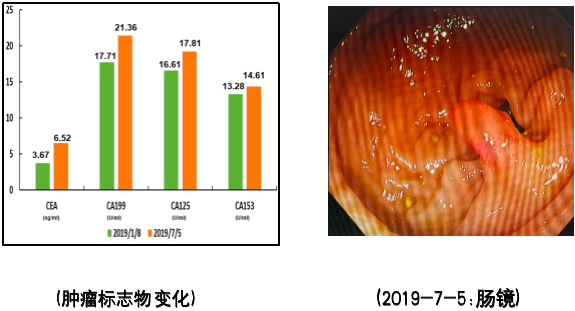
术后1年半(2019-7-5)常规复查,血检:肿标轻度升高;影像学:未见复发转移;肠镜:距肛门10cm直肠处有1枚息肉样隆起,大小2×1cm,呈乳头样,基底有蒂,予行EMR摘除,病理提示腺瘤性息肉。
术后2年(2019-12-23)常规复查:血检:肿标持续升高;影像学:未见明显复发转移征象。
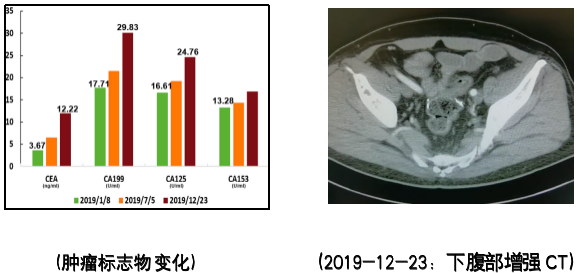
术后2年半,第一次肿瘤复发
2020-06-16(术后2年半),患者因“乙状结肠肿瘤术后2年余,大便习惯改变4月”再次入院。
辅助检查:
肿标:
CEA 10.2ng/ml,
CA199 37.78U/ml,
CA125 16.85U/ml,
CA153 13.2U/ml;
影像学:未见明显异常。
肠镜:距肛缘25cm可见新生物,占据肠腔1/2周,表面可见溃疡,上覆污苔,周围黏膜堤状隆起,距肛缘10cm可见吻合口,黏膜光滑;
病理:高级别上皮内瘤变,考虑癌变。
初步诊断:乙状结肠恶性肿瘤,分期:cT4N0M0,IIB期
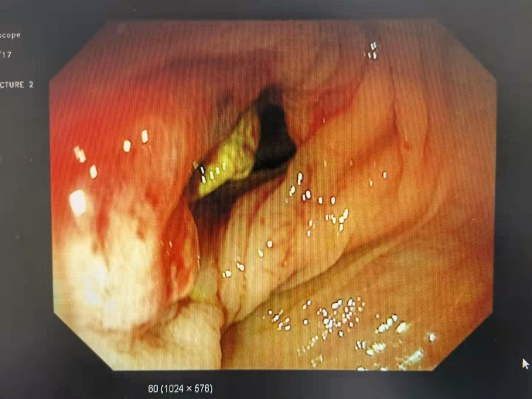
(2020-6-16:肠镜)
第二次手术及术后第二次化疗
完善检查后于2020-06-24行:腹腔镜下乙状结肠肿瘤根治术,术中发现侧腹壁可疑癌结节,予以取活检。
病理:黏液腺癌,大小3.3x3.0cm,浸润肠壁全层至浆膜外纤维脂肪组织;上下切缘:均未见癌组织累及;肠旁淋巴结转移情况:2/11;侧腹壁结节:见癌组织;分期:pT4N1M1b,IVB期。
基因检测:KRAS Exon-2 G12C/R/V/A、G13C位点突变;MSI检测:MSS。
患者恢复顺利,术后1月开始行第二次术后化疗。先予以FOLFOX方案化疗2次,患者肿标显著升高,后加用贝伐珠单抗继续化疗3次,肿瘤指标持续升高,后更改化疗方案为FOLFIRI+贝伐珠单抗*2次,患者肿瘤指标未见明显改善。期间复查PET-CT (2020/9/8;d3次化疗前):两侧侧腹膜、后腹膜、盆腔腹膜、肠系膜多发转移可能性大。
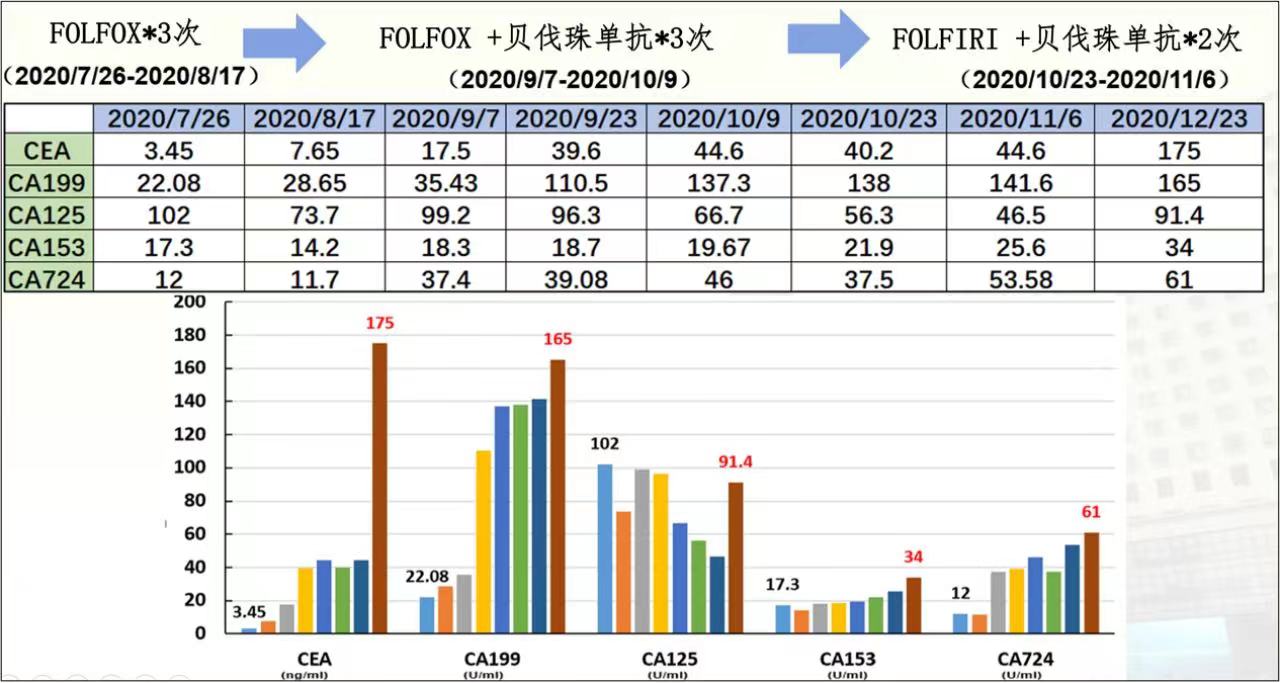
(患者化疗方案记录及肿瘤指标变化)
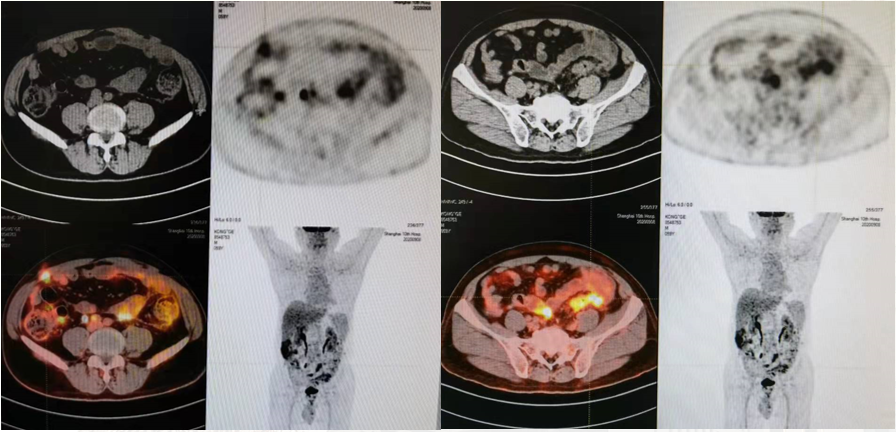
( 2020/9/8患者PET-CT影像;d3次化疗前)
尝试免疫治疗
考虑患者化疗效果欠佳,进一步加做石蜡切片基因检测,探寻潜在免疫治疗靶点。石蜡切片基因检测提示(2020-12):
1.患者存在MUTYH突变,提示肿瘤遗传风险较高;2. 患者肿瘤突变负荷(tumor mutational burden,TMB)较高,TMB=16.76%。

肿瘤突变负荷(tumor mutational burden,TMB):指特定基因组区域内每兆碱基对(Mb)体细胞非同义突变的个数,反映肿瘤细胞内 DNA 损伤修复情况。基因突变后产生的新蛋白可触发免疫反应,被认为是抗肿瘤免疫治疗的前提。TMB可预测多种实体肿瘤的免疫治疗效果,已成为继 MSI-H/dMMR 后的第二个肿瘤免疫治疗泛癌种伴随诊断标志物[1-3]。
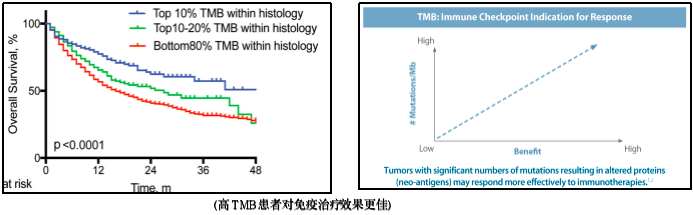
2020年6月,基于高TMB对免疫治疗有更好的反应性,FDA 批准 Pembrolizumab 单药用于治疗不可切除或转移性的高TMB (TMB≥10 个突变/Mb) 实体瘤患者[4]。目前研究表明,结直肠癌是TMB最高的实体瘤之一,且高TMB的结直肠癌患者对免疫治疗的效果更好[5,6]。2020年中国癌症预防杂志刊发肿瘤突变负荷检测及临床应用中国专家共识,希望进一步提升临床医师对TMB检测的关注[7]。但2021年CSCO结直肠癌肿瘤指南中,仅推荐MSI-H/dMMR的患者,在转化治疗或姑息性治疗中可考虑使用PD-1单抗免疫治疗,尚未把高TMB作为免疫治疗治疗的指征[8]。
结合患者既往化疗方案、基因检测结果,进行院内MDT讨论后,并结合患者自身意愿,决定更改治疗方案为三线化疗方案,并加用免疫治疗:瑞戈非尼+卡瑞利珠单抗。患者更改治疗方案后,第2次治疗前查肿瘤指标显著下降,故继续予以该方案治疗10次,期间复查下腹部增强CT(2021-07-22):与PET-CT相比,腹腔转移灶未见明显进展。
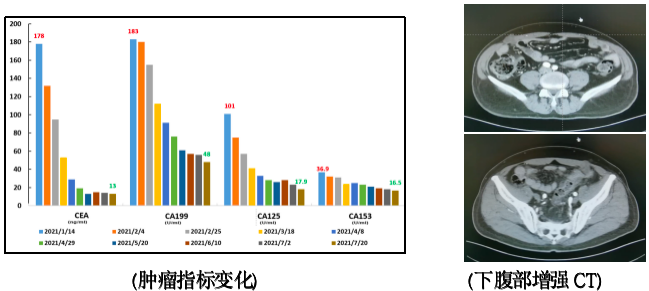
患者第10次瑞戈非尼+卡瑞利珠单抗治后,肿瘤标志物开始回升。继续治疗同时,进一步完善PET-CT复查(2021-10-29):提示双侧腹部、大网膜、肠系膜周围多发淋巴结,糖代谢增高,考虑转移,与2020-09-08相比病灶体积增大,糖代谢增高。
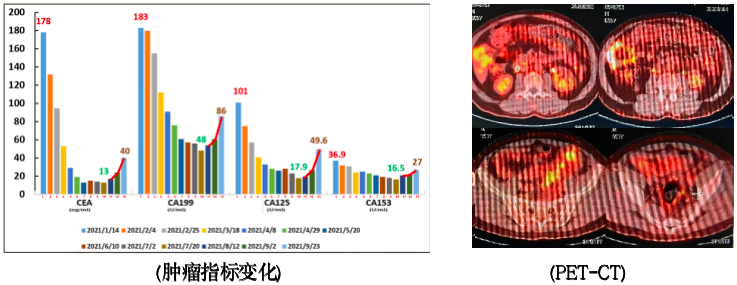
后复查患者肿瘤标志物CEA较为稳定,经MDT小组及多次学术会议讨论后,暂定予以原方案继续治疗,下图为患者第15-25次瑞戈非尼+卡瑞利珠单抗治前,肿瘤标志物变化情况。
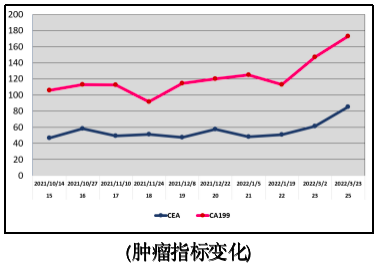
下一步治疗方案?
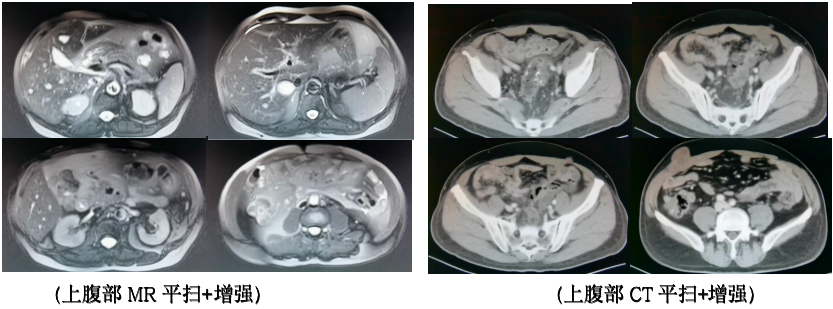
最近一次复查结果:上腹部MR平扫+增强 (2022-3-11):中上腹网膜及腹膜多发结节,考虑转移;左侧腹直肌、右侧腹外斜肌多发结节,考虑转移;下腹部CT平扫+增强 (2022-3-10):乙状结肠周围、部分腹膜间隙、两侧腹壁多发稍低密度灶,转移瘤可能大。
目前患者无明显不适主诉,肿瘤标志物、影像学检查提示肿瘤进展,目前正在积极探讨下一步治疗方案。
参考文献
1. Le, Dung T et al. “PD-1 Blockade in Tumors with Mismatch-Repair Deficiency.” The New England journal of medicine vol. 372,26 (2015): 2509-20.
2. Samstein, Robert M et al. “Tumor mutational load predicts survival after immunotherapy across multiple cancer types.” Nature genetics vol. 51,2 (2019): 202-206.
3. Chan, T A et al. “Development of tumor mutation burden as an immunotherapy biomarker: utility for the oncology clinic.” Annals of oncology : official journal of the European Society for Medical Oncology vol. 30,1 (2019): 44-56. doi:10.1093/annonc/mdy495
4. U.S. Food and Drug Administration. (2020, June 16). FDA approves pembrolizumab for adults and children with TMB-H solid tumors [Press release].
5. Lee, Chung-Han et al. “Update on Tumor Neoantigens and Their Utility: Why It Is Good to Be Different.” Trends in immunology vol. 39,7 (2018): 536-548.
6. Samstein, Robert M et al. “Tumor mutational load predicts survival after immunotherapy across multiple cancer types.” Nature genetics vol. 51,2 (2019): 202-206.
7. 中国临床肿瘤学会(CSCO)结直肠癌诊疗指南.2021/中国临床肿瘤学会指南工作委员会.北京;人民卫生出版社,2021.4.
8. 辇伟奇、聂勇战、应建明、张海伟、章必成、申鹏、王宏伟. 肿瘤突变负荷检测及临床应用中国专家共识(2020年版)[J]. 中国癌症防治杂志, 2020, 12(5):10.
参考文献
1. Le, Dung T et al. “PD-1 Blockade in Tumors with Mismatch-Repair Deficiency.” The New England journal of medicine vol. 372,26 (2015): 2509-20.
2. Samstein, Robert M et al. “Tumor mutational load predicts survival after immunotherapy across multiple cancer types.” Nature genetics vol. 51,2 (2019): 202-206.
3. Chan, T A et al. “Development of tumor mutation burden as an immunotherapy biomarker: utility for the oncology clinic.” Annals of oncology : official journal of the European Society for Medical Oncology vol. 30,1 (2019): 44-56. doi:10.1093/annonc/mdy495
4. U.S. Food and Drug Administration. (2020, June 16). FDA approves pembrolizumab for adults and children with TMB-H solid tumors [Press release].
5. Lee, Chung-Han et al. “Update on Tumor Neoantigens and Their Utility: Why It Is Good to Be Different.” Trends in immunology vol. 39,7 (2018): 536-548.
6. Samstein, Robert M et al. “Tumor mutational load predicts survival after immunotherapy across multiple cancer types.” Nature genetics vol. 51,2 (2019): 202-206.
7. 中国临床肿瘤学会(CSCO)结直肠癌诊疗指南.2021/中国临床肿瘤学会指南工作委员会.北京;人民卫生出版社,2021.4.
8. 辇伟奇、聂勇战、应建明、张海伟、章必成、申鹏、王宏伟. 肿瘤突变负荷检测及临床应用中国专家共识(2020年版)[J]. 中国癌症防治杂志, 2020, 12(5):10.
查看更多