查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





人工智能赋能乳腺癌个体化治疗专刊
Cancer Biology & Medicine
据统计,乳腺癌已成为全球女性发病率最高的恶性肿瘤,每年新发病例超过230万。面对这一沉重的疾病负担,乳腺癌诊疗领域正以前所未有的速度演进——精准医学不断深入临床实践,人工智能逐步赋能诊疗决策,国内外学者的研究步伐也在持续加快。在这一背景下,Cancer Biology & Medicine与中国人民解放军总医院江泽飞教授联合打造“人工智能赋能乳腺癌个体化治疗”专刊,旨在汇聚顶尖专家的智慧,系统呈现乳腺癌诊疗领域的新进展、新思考和新突破。
嵌合抗原受体巨噬细胞(CAR-M)作为一种新型细胞免疫治疗策略,在实体瘤治疗中展现出重要潜力。然而,肿瘤微环境中的营养匮乏和代谢竞争常限制免疫细胞的功能,从而影响CAR-M的抗肿瘤效果。谷氨酰胺是免疫细胞维持代谢稳态和效应功能的重要营养物质,其摄取与利用对巨噬细胞活化具有关键作用。SLC38A2作为关键的谷氨酰胺转运蛋白,在细胞代谢适应中发挥重要作用。本期专刊中,中山大学团队发表论著,研究者通过代谢工程增强CAR-M的SLC38A2表达,通过重编程谷氨酰胺代谢,为提升CAR-M抗肿瘤功能提供了新方案。

Cite

Liu M, Chen Q, Zhang L, Zhou Y, Wen N, Jin J, et al.Metabolic engineering of SLC38A2 reprograms glutamine utilization andenhances CAR-macrophage antitumor function in solid tumors. Cancer BiolMed. 2026; 23: 392-417. doi: 10.20892/j.issn.2095-3941.2025.0775
研究介绍
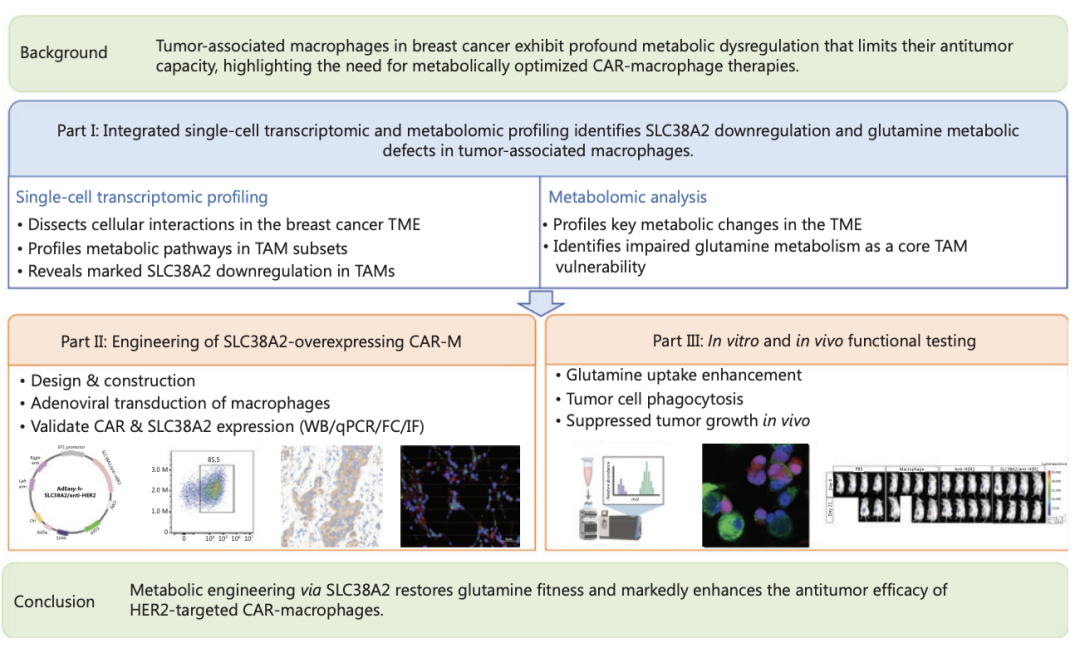
研究流程图
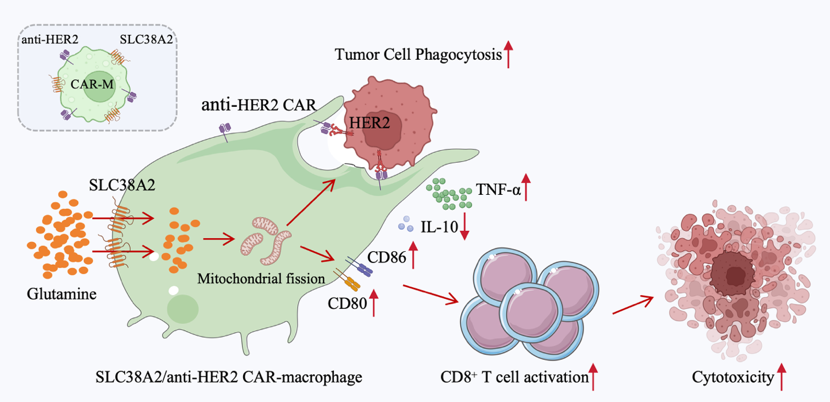
代谢工程化SLC38A2提升CAR-M抗肿瘤活性的机制示意图
本研究首先通过分析乳腺癌患者的单细胞转录组数据,系统描绘了肿瘤微环境(TME)中的免疫细胞景观。细胞间通讯分析显示,巨噬细胞在免疫细胞与肿瘤细胞之间以及免疫细胞内部的信号互作中处于核心节点地位,其配体-受体相互作用最为显著。通路富集分析进一步揭示,巨噬细胞除经典免疫功能外,还显著富集代谢通路,提示代谢活动在巨噬细胞功能调控中具有重要作用。进一步整合组织和细胞水平的代谢分析发现,谷氨酰胺在肿瘤细胞与巨噬细胞间存在重要差异。同时,在体外共培养实验中,单独培养的巨噬细胞与HER2+ SKBR3肿瘤细胞共培养后,SLC38A2 mRNA及蛋白水平显著下降,免疫荧光信号亦减弱,提示肿瘤微环境抑制了巨噬细胞SLC38A2表达(图1)。
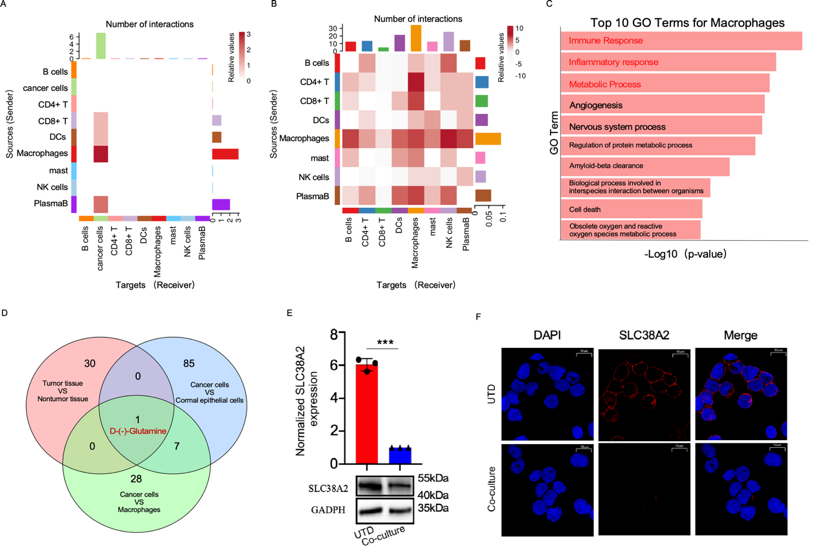
图1: 肿瘤微环境抑制巨噬细胞SLC38A2表达并造成谷氨酰胺代谢受限。(A, B) 细胞通讯热图。(C) 巨噬细胞显著富集的前10条GO通路。(D)代谢物Venn图。(E) qPCR及免疫印迹显示SLC38A2的表达。(F) 免疫荧光显示SLC38A2在共培养后信号减弱。 ***P < 0.001。
基于乳腺癌微环境中巨噬细胞谷氨酰胺代谢受限的特点,构建了SLC38A2过表达的抗HER2 CAR-M(SLC38A2/anti-HER2 CAR-M)。与常规抗HER2 CAR-M相比,该构建体谷氨酰胺摄取能力显著增强,关键谷氨酰胺代谢酶GLS、GLUD1及GOT2表达上调,显示细胞代谢活性明显提升。功能分析显示,SLC38A2/anti-HER2 CAR-M在与HER2+肿瘤细胞共培养后,CD80和CD86表达显著上调,TNF-α分泌增加,IL-10分泌下降,表现出促炎活化表型。在吞噬实验中,SLC38A2/anti-HER2 CAR-M对HER2+肿瘤细胞的吞噬率显著高于其他对照组,而与HER2-肿瘤细胞共培养时吞噬率差异不大。同时, 线粒体裂变水平升高,提示代谢增强改善了能量供应和效应功能。该构建体呈增强的促炎表型,CD80/CD86共刺激分子表达上调,TNF-α分泌增加,IL-10下降,同时显著促进CD8+ T细胞活化和增殖,显示可有效协同调动适应性免疫反应。在体内,采用SKBR3皮下异种移植模型进行干预,结果显示SLC38A2/anti-HER2 CAR-M显著抑制肿瘤生长,相较对照组肿瘤负荷下降最为明显,进一步验证了代谢增强策略对CAR-M抗肿瘤活性的有效促进作用。
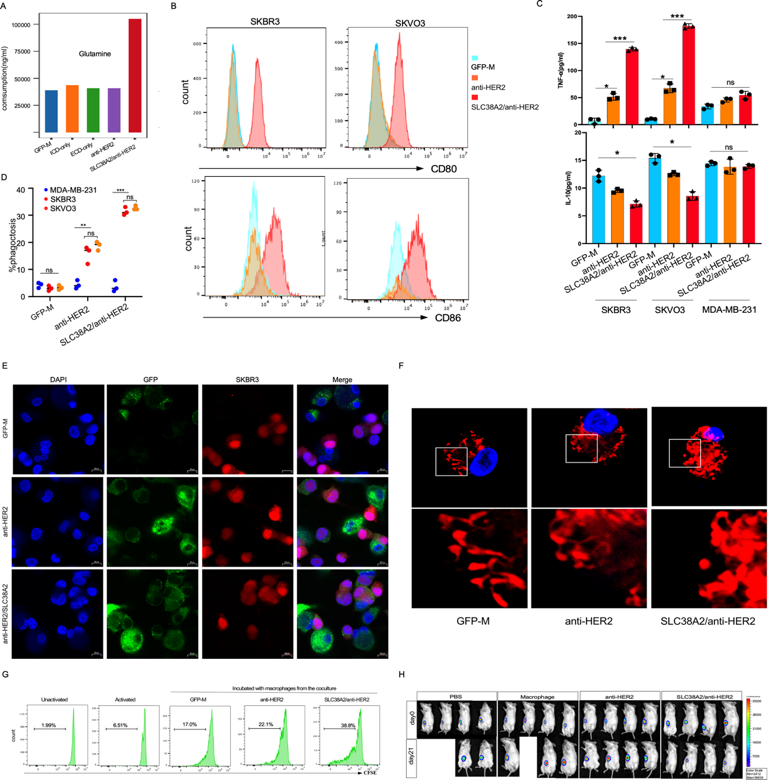
图2: 代谢工程化SLC38A2提升CAR-M的谷氨酰胺摄取及抗肿瘤效应(A) 质谱检测谷氨酰胺摄取水平。(B) 与HER2+ SKBR3或SKOV3细胞共培养后,巨噬细胞活化标志物CD80和CD86的流式细胞术分析。(C) ELISA检测共培养上清液中TNF-α和IL-10水平。 (D,E)流式和共聚焦检测吞噬水平。(F) 线粒体代表性免疫荧光图。(G) CFSE分析显示巨噬细胞促进T细胞增殖。 (H) BLI显示不同处理组肿瘤生长情况。*P < 0.05, *** P < 0.001。
小结
本研究围绕肿瘤微环境中代谢限制对免疫细胞功能的影响,提出通过代谢工程策略提升CAR巨噬细胞抗肿瘤能力的新思路。我们以谷氨酰胺代谢为切入点,通过在CAR-M中引入关键谷氨酰胺转运蛋白SLC38A2,增强其对谷氨酰胺的摄取能力,从而重编程细胞代谢状态,提高其在营养匮乏肿瘤微环境中的代谢适应性。研究结果表明,SLC38A2介导的代谢增强能够显著改善CAR-M的效应功能,提升其吞噬活性及抗肿瘤能力,为克服实体瘤免疫治疗中的代谢障碍提供了新的策略。
本研究不仅揭示了谷氨酰胺代谢调控CAR-M抗肿瘤功能,相较于传统仅通过信号通路或受体结构优化CAR设计的策略,从代谢层面重塑免疫细胞功能为提升CAR疗法在复杂肿瘤微环境中的有效性提供了新的方向。
未来,结合多组学分析和合成生物学技术,有望开发出更加精准和高效的CAR-M工程化策略。同时,SLC38A2介导的代谢重编程策略也有望拓展至其他免疫细胞类型,为实体瘤免疫治疗提供更加广阔的应用前景,并为推动细胞治疗在临床中的转化奠定基础。
*本课题由国家重点研发计划“干细胞研究与器官修复”专项支持。
通信作者
赵绮毅 研究员
中山大学
中山大学 研究员 博士生导师
中山大学未来生物医药学院PI、肝病实验室主任
“国家高层次人才特殊支持计划”青年拔尖人才、广东省杰青、广州市科技菁英
广东省病理生理学会肝病专委会副主任委员
主持国家重点研发计划青年项目、国家自然科学基金4项、教育部等纵向基金13项;以通讯/第一作者在 Cell、Nature Communications、SCIENCE CHINA Life Sciences等发表论文 19篇,总引达1000次。获广东省预防医学会优秀论文奖一等奖,参与广东省科技进步奖一等奖,授权/公开国家发明专利8项
来源:Cancer Biology Medicine
查看更多