查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





病情播报
6岁男孩,以“发现右侧胸壁包块2个月,伴间断发热”入院。患儿自幼确诊为慢性肉芽肿病。查体:右侧胸壁见约8×7.5cm包块,边界清,活动度差,质韧,中心区有波动感,皮温不高,无红肿,双肺呼吸音粗,右肺呼吸音略低。肺部CT:肺内间、实质病变,右侧胸腔积液。右下胸壁局限性增厚,密度偏低,沿肋骨间隙向内延伸。胸壁软组织包块穿刺脓液培养为烟曲霉菌。予伏立康唑及局部抽脓治疗后,胸壁包块明显缩小。
烟曲霉感染引起的胸壁脓肿
一、概述
儿童侵袭性曲霉菌病(Invasive Aspergillosis, IA)是免疫功能低下儿童最常见、最严重的感染性并发症之一。儿童IA的发病率逐渐增加。烟曲霉是IA中最常见的致病菌种,儿童侵袭性烟曲霉感染最常引起肺部疾病,其次为皮肤感染、鼻窦、中枢神经系统,而烟曲霉导致的胸壁脓肿甚为少见。
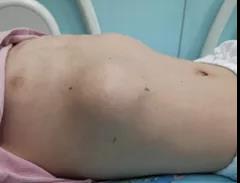
图1 胸壁包块
二、生物学特征:
曲霉菌(Aspergillus)普遍存在于自然界,分布于土壤、垃圾、腐败的食品中,人们经常会接触到其孢子。曲霉中常见的致感染菌为烟曲霉(A. fumigatus),其在曲霉菌中致病力最强,其他包括黄曲霉(A.flavus)、土曲霉(A. terreus)、黑曲霉(A. niger)等。烟曲霉在沙氏培养基的菌落质地呈绒毛状或絮状,表面呈深绿色、烟绿色,背面苍白色或淡黄色;显微镜下分生孢子头短柱形,呈深浅不同的绿色。分生孢子梗光滑,带绿色,近顶端膨大形成倒立烧瓶状顶囊,顶囊有单层小梗,布满顶囊表面4/5,仅上半部产生孢子。所有曲霉菌丝的共同特点为有隔膜菌丝,直径3-6μm,分支呈锐角45°,菌丝两侧平行。组织病理中,若发现一个水果样的曲霉头可以确定诊断。在HE染色中菌丝不易识别,但在银染如Gomori染色中很明显。
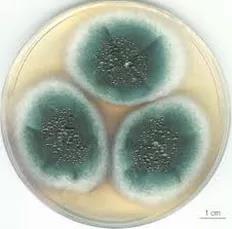
图2 烟曲霉菌落
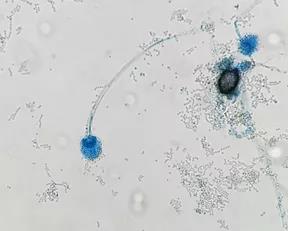
图3 烟曲霉镜下表现(乳酸酚棉蓝染色)
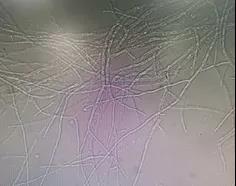
图4 镜下菌丝形态(呈45°角分支)
三、宿主因素
儿童侵袭性曲霉菌病的宿主因素与成人相似。易感人群为严重免疫功能低下儿童,包括血液系统恶性肿瘤(特别是急性髓细胞白血病)接受化疗和造血干细胞移植术后、原发免疫缺陷病儿童,尤其是慢性肉芽肿病(Chronic granulomatous disease,CGD)。CGD因吞噬细胞功能异常导致多种感染,真菌感染占约20%,其中曲霉是最常见的真菌感染,约占80%。
曲霉,尤其是烟曲霉菌引起的肺炎或败血症是最常见的致死原因。此外,易感因素还包括中性粒细胞缺乏症、接受高剂量激素治疗、其他免疫抑制状态、接受实体器官移植、早产新生儿等。
四、传播途径
曲霉菌感染的原发感染最常发生于吸入分生孢子后的肺部或鼻窦,有时可经胃肠道传播、皮肤直接感染或血行播散引起气管支气管炎、鼻-鼻窦炎、脑脓肿、骨髓炎、心内膜炎和胃肠疾病等。胸壁的曲霉感染(包括骨髓炎)有1/3是由肺部感染直接侵犯导致。
IA的临床表现因涉及不同系统而不同,肺部曲霉菌病最常见,播散性曲霉菌病还可累及鼻-鼻窦、中枢神经系统感染、皮肤、肝、肾、心、甲状腺、骨骼等,胸壁脓肿少见。发热是最常见的表现,部分患者仅表现为发热。肺部受累可出现咳嗽、呼吸困难、咯血、胸痛症状等。胸壁受累多与潜在的基础疾病如CGD有关。在CGD患者中,曲霉菌感染可累及胸壁及周围肋骨、胸骨、椎骨引起骨髓炎。临床表现不典型,发热比例低,进展缓慢,因此常不易被发现。
对感染部位体液进行真菌镜检、培养以及组织标本的病理学检查及培养仍是确诊IA的金标准。分子检测技术,如PCR技术简便,快捷,高效,有利于早期诊断。二代测序技术可能有利于病原诊断,但要结合临床进行结果综合判读。此外,真菌生物标志物如半乳甘露聚糖试验(galactomannan, GM)对IA诊断有重要意义。高危儿童血清GM试验总体敏感度、特异度分别为76%、86%,且阳性出现时间早于出现临床症状和影像学表现,利于早期诊断。免疫功能低下人群支气管肺泡灌洗液(BALF)样本的GM敏感度和特异性更高,诊断价值高于血清样本。需要注意的是中性粒细胞减少、土曲霉菌等生长缓慢的曲霉菌感染以及合并CGD等情况下GM试验敏感度降低。
(1)超声:超声因没有放射性而成为儿童胸壁病变患者首选检查方式,同时对囊性病变及病变内部血流状况的显示也优于CT和MRI。
(2)CT:烟曲霉胸壁脓肿为局限的液化灶,单房或多房。高分辨率CT对肺部IA诊断有重要的意义,晕轮征、空气新月征和空洞高度提示肺部曲霉病。儿童 (特别是年龄小于5岁) 常缺乏特异性影像学表现,以结节、团块样损害最常见。CGD患儿的肺部曲霉感染的影像学特点常不特异,可出现节段性或肺叶实变,类似细菌性感染性肺炎,伴或不伴空洞,可累及单侧或双侧,可见结节改变。CT扫描也能准确显示骨髓炎的细微骨改变和骨膜或骨膜内反应。
(3)MRI:MRI具有优越的软组织对比度,可发现胸壁软组织炎症以及程度。脓肿在MRI成像上表现为局部出现坏死及液体,单或多房,T2为高信号。MRI显示软组织脓肿的准确率为92%。
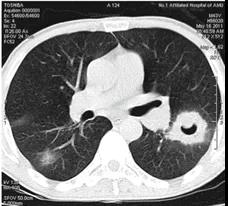
图5:肺部侵袭性曲霉菌病(新月征和晕轮征)
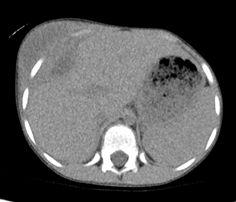
图6:患儿胸部CT示右侧胸壁包块
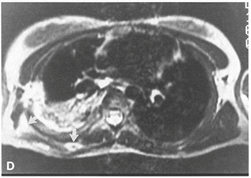
图7:肺部侵袭性曲霉病导致胸壁脓肿和临近肋骨受累
分级诊断:
IA的诊断采用2019欧洲癌症研究治疗组织(EORTC)和真菌研究组(MSG)对于IFD的分级诊断修订标准分为确诊(proven)、极似(probable)和拟诊(possible),修订标准如下:
(1)确诊(proven)标准:
霉菌出现以下情况可确诊:a.穿刺或活检获取的无菌部位标本组织病理学、细胞病理学或直接显微镜检见菌丝或黑色酵母样形态,伴有相关组织损伤的证据;b. 从正常无菌、临床或放射学异常的符合感染性疾病特征的部位(不包括BALF、鼻旁或乳突窦腔和尿液标本)通过无菌操作获得的标本进行培养,出现透明或着色的霉菌;c.血培养出现霉菌;d.组织进行PCR扩增,并结合DNA测序获得真菌序列。注意血清学检测不作确诊依据。
(2)极似(probable)标准:极似诊断(probable)IFD需要具备至少1个宿主因素、1个临床表现和1个真菌学证据。
a.宿主因素包括:中性粒细胞减少(中性粒细胞<0.5×10^9/L,持续10天以上,与侵袭性真菌病发病有时间相关)、血液系统恶性疾病、接受同种异体造血干细胞移植、实体器官移植、使用糖皮质激素(过去60天内,以≥0.3mg/kg治疗剂量长时间使用≥3周,不包括过敏性支气管肺曲霉菌病患者)或其他T细胞免疫抑制剂使用(过去90天内,如钙调磷酸酶抑制剂、肿瘤坏死因子α阻滞剂、淋巴细胞特异性单克隆抗体、免疫抑制核苷类似物)、使用识别B细胞免疫抑制剂治疗(例如Bruton酪氨酸激酶抑制剂如依布替尼)、严重免疫缺陷病(如慢性肉芽肿病、STAT3缺陷、重症联合免疫缺陷病)、累及肠道、肺部或肝脏的急性移植物抗宿主病Ⅲ级或Ⅳ级,用类固醇一线药物治疗无效。
b.临床表现包括:肺曲霉菌病(CT上至少出现下列4种影像中的1种:①致密、边界清楚的病变,伴或不伴晕轮征;②空气新月征;③空洞;④楔形、节段性或大叶性实变)、其他肺部霉菌病(和肺曲霉菌病类似,加反向晕轮征,即反晕征)、支气管炎(支气管镜下见气管支气管溃疡、结节、伪膜、斑块或焦痂)、鼻腔鼻窦疾病(急性局部疼痛包括眼部放射痛、鼻部溃疡伴黑色焦痂、从鼻窦延伸穿过骨屏障,包括进入眼眶)、中枢神经系统感染(至少出现两种特征中的一种:影像学上的局灶性病变、MRI或CT上的脑膜强化)。
c.真菌学证据包括:痰液/BALF/支气管毛刷/抽吸物培养或镜检霉菌;GM检测满足任何一项:单次血清或血浆≥1.0、BALF≥1.0、单次血清或血浆≥0.7和BALF≥0.8、脑脊液≥1.0;PCR曲霉检测下列任何一项:①血浆、血清或全血标本2次或多次及以上连续PCR阳性;②BALF 2次或多次重复PCR阳性;③血浆、血清或全血标本至少1次PCR阳性且BALF至少1次PCR阳性。
(3)拟诊(possible)标准:符合1个宿主因素和1个临床特征标准,但没有真菌学证据的病例,则是拟诊(possible)IFD。
侵袭性真菌病确诊定义适用于任何患者,而拟诊及极似定义除地方性真菌病外,仅适用于存在免疫功能低下的患者。
现有3类抗真菌药可用于治疗曲霉菌病:多烯类(两性霉素B、两性霉素B脂质体、两性霉素B脂质复合体)、唑类(伏立康唑、泊沙康唑、艾沙康唑、伊曲康唑)及棘白菌素类(卡泊芬净、米卡芬净)。美国感染病学会(Infectious Diseases Society of America, IDSA)2016指南推荐伏立康唑作为侵袭性曲霉菌病的初始治疗首选,伏立康唑+棘白菌素类(如卡泊芬净)联合治疗为重度疾病的初始治疗,尤其在血液系统恶性肿瘤和/或严重持续性中性粒细胞减少的患者中。对于无法耐受伏立康唑的患者,可选择两性霉素B脂类制剂或艾沙康唑。氟康唑对于烟曲霉呈天然耐药而不能用于治疗曲霉病。棘白菌素类脑脊液浓度低,因此不推荐用于中枢神经系统曲霉菌病。系统性抗真菌最短治疗时长为6~12周,治疗持续时间取决于感染部位、基础疾病、对治疗反应、是否需要进一步免疫抑制,一般要持续到感染的全部症状及体征缓解,影像学异常已稳定。
伏立康唑的用法及应用注意事项:2~12岁儿童和12~14岁且体重<50公斤者负荷剂量(适用于第1个24小时):9mg/kg/次,每12小时给药;维持剂量:8mg/kg/次,每12小时给药。注意监测血药浓度(谷浓度)维持在1.0~5.5mg/L(严重感染2~6mg/L)。伏立康唑最常见的不良反应是视觉损害,其他如皮疹、消化道症状、头痛、外周水肿、肝功能检查异常、呼吸窘迫和腹痛。此外,伏立康唑与 QTc 间期延长有关,有诱发尖端扭转型室速的风险,在使用伏立康唑治疗前或治疗期间应当监测心电图和血电解质。伏立康唑禁止与西罗莫司、利福平、卡马西平和苯巴比妥联合使用。
除抗真菌治疗外,在某些伴发慢性坏死性疾病的复杂病例中,如胸壁脓肿或骨髓炎,可行手术治疗作为辅助治疗,在定位慢性感染病灶后,对所有涉及的骨、软骨和软组织进行彻底清创。
IA是免疫抑制患者死亡的重要原因。该人群IA发作后的1年死亡率高达80%,发生IA的造血干细胞移植受者12周全因死亡率为58%。而近年来更近期的研究结果估计长期生存率明显提高,由1986-2000年的12.5%增加到了2001-2010年的58%。
作者:王珊、郭凌云
本文首发自BCH儿童感染
查看更多