查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





曲妥珠单抗与帕妥珠单抗双靶治疗在人表皮生长因子受体-2阳性乳腺癌新辅助治疗中的应用效果
作者:叶泽霖,郑金珠,冯杰鑫,吴雄*
福建医科大学附属漳州市医院,漳州 363000
乳腺癌是女性最常见的恶性肿瘤,近年来乳腺癌呈高发趋势,好发于40~60岁女性中,还具有发病年龄提前的趋势,乳腺癌侵袭性高,其预后受到多因素的影响,与疾病的发展阶段以及治疗时机和治疗方案等都有密切的联系,早发现、早诊断、早治疗能够改善患者的生活质量以及延长生存率[1]。人表皮生长因子受体-2(human epidermal growth factorreceptor-2,HER-2)是乳腺癌重要的驱动基因和预后指标,HER-2阳性乳腺癌患者预后往往较差,HER-2阳性提示乳腺癌的原位癌基因呈现快速增殖的状态,且具有较高的耐药性和复发性,患者生活质量堪忧,有效治疗尤为必要[2]。新辅助治疗在乳腺肿瘤疾病的恶性程度降低和肿瘤体积的降低、淋巴结转阴中起重要作用,治疗后再行手术可降低手术损伤,增加手术完全切除的可能性而提升预后,增加保乳治疗率,更符合患者的治疗需求,是当下肿瘤疾病中热门的治疗方法[3]。相关研究显示,化疗联合曲妥珠单抗的新辅助治疗方案在HER-2阳性乳腺癌患者中获得了理想的治疗效果,提高了患者术后病理完全缓解率,促进手术效果,对乳腺癌靶向药物治疗选择药物的靶点研究以及HER-2阳性乳腺癌的新辅助治疗中具有重要指导意义[4]。帕妥珠单抗为靶向药物之一,临床应用于具有高复发风险HER-2阳性乳腺癌的辅助治疗。相关研究中指出,对该类型乳腺癌患者在化疗以及曲妥珠单抗治疗基础上采用帕妥珠单抗治疗,可凭借双重抗HER-2 阻断的机制而协同抑制乳腺癌患者肿瘤的生长,延长患者生存期[5]。本研究选取2019年4月至2022年6月福建医科大学附属漳州市医院收治的52例人表皮生长因子受体-2阳性乳腺癌患者作为研究对象,探究曲妥珠单抗联合帕妥珠单抗治疗方案在人表皮生长因子受体-2阳性乳腺癌新辅助治疗中的应用效果。
1.1 研究对象 选取2019年4月至2022年6月福建医科大学附属漳州市医院收治的52 例人表皮生长因子受体-2 阳性乳腺癌患者作为研究对象。纳入标准:①病理学以及免疫组化检验诊断HER-2 阳性,且均为单侧肿瘤;②知情同意;③生存期预估≥ 1 年;④首次治疗。排除标准:①严重化疗不良反应;②其他脏器功能不全;③同时合并其他疗法者;④中途退出研究。本研究经医院伦理委员会批准。
1.2 方法 遵照随机数字表法分组原则将患者分为观察组与对照组,每组26 例。
对照组给予紫杉醇、卡铂和曲妥珠单抗疗法:紫杉醇于化疗第一天给药,用量为260 mg/m2,用0.9%生理盐水80 ml 稀释后进行静脉滴注治疗,滴注0.5 h;联合卡铂治疗,剂量AUC×(肌酐清除率+25)mg,AUC=5,用5% 葡萄糖注射液500 ml 进行稀释,静脉滴注治疗,滴注2.5 h。曲妥珠单抗治疗首剂量为8 mg/kg,滴注1.5 h ;以上药物均3 周(1 疗程:21 d)用药一次,曲妥珠单抗在第二个疗程时进行药物减量,减少至6 mg/kg,共治疗6 个疗程。
观察组则在对照组基础上联合使用帕妥珠单抗进行治疗:治疗首剂量为840 mg,用0.9% 生理盐水稀释后静脉滴注1.5 h,第二疗程减量至420 mg,治疗周期同上组。新辅助化疗完成后评估患者的病灶控制情况,可择期行手术治疗。
1.3 观察指标 治疗结束后观察下述指标:(1)临床疗效评价[6]。显效:患者病灶完全消失;有效:病灶体积减小> 50% ;无效:病灶体积减小25% ~ 50%,或病灶增加。(2)新辅助治疗后术后病理与治疗前活检病理进行对比,对肿瘤细胞减少比例进行Miller-Payne 系统分级,显效:MP 分级V 级(病理完全缓解)及MP 分级Ⅳ级(肿瘤细胞减少90% 以上),有效:MP 分级Ⅲ级(肿瘤细胞减少30% ~ 90%),无效:MP 分级Ⅱ级(肿瘤细胞减少不超过30%)及MP 分级I 级(肿瘤细胞无明显减少),术后病理缓解率=(显效例数+ 有效例数)/ 总例数×100%。(3)生活质量[7]。采用癌症治疗功能评价量表(FACT-B)对两组乳腺癌患者治疗前后的生活质量进行评价。量表包含了生理状况、心理状况、社会职能以及情感职能4 个维度,总分100 分,分数越高表示患者生存质量越好。(4)不良反应。记录两组患者治疗期间不良反应的发生情况,具体包括胃肠道反应、贫血、心脏毒性、口腔溃疡等。
1.4 统计学方法 运用SPSS 24.0 对数据进行分析,计量资料和计数资料分别采用x-±s 和例数(%)表示,组间对比则使用χ2/t 校检;若P < 0.05,认为差异具有统计学意义。
2.1 两组基线资料对比 对照组,年龄范围35 ~ 68 岁,平均(51.26±5.17) 岁;肿瘤分期:Ⅰ 期10 例,Ⅱ期11 例,Ⅲ期5 例;观察组,年龄34 ~ 70 岁,平均(51.30±5.22)岁;肿瘤分期:Ⅰ期9 例,Ⅱ期12 例,Ⅲ期5 例。对比两组患者相关临床资料无统计学差异(P > 0.05)。
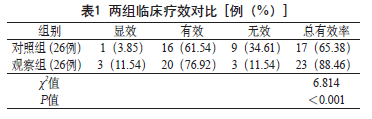
2.2 两组临床疗效对比 观察组治疗有效率88.46%高于对照组65.39%(P < 0.05)。见表1。
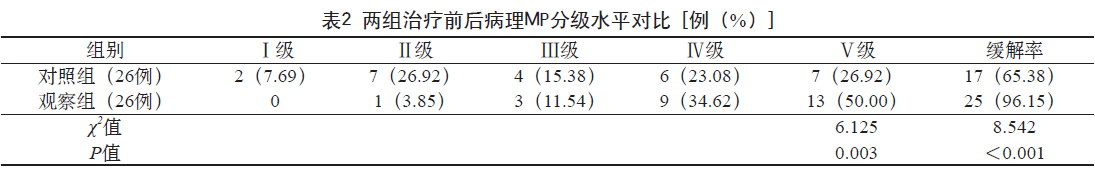
2.3 两组治疗前后病理MP 分级水平对比 观察组术后病理缓解率96.15% 高于对照组65.38%(P < 0.05);且观察组病理完全缓解率高达50.00%,高于对照组26.92%(P < 0.05)。见表2。
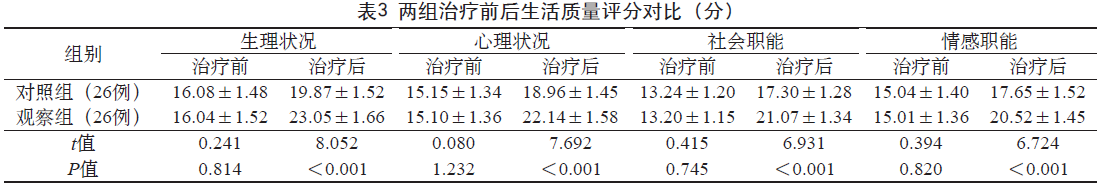
2.4 两组治疗前后生活质量对比 治疗前,两组患者生活质量各维度的评分差异无统计学意义(P > 0.05);治疗后,两组生活质量各个维度评分均有所提高,其中观察组各维度的评分高于对照组(P < 0.05)。见表3。
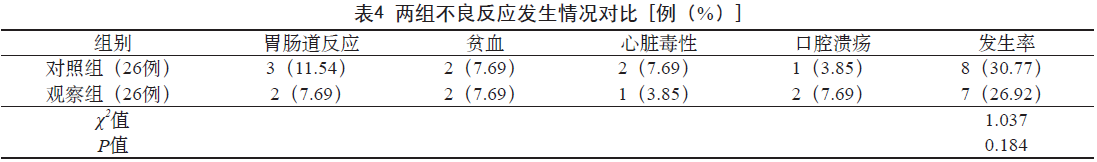
2.5 两组不良反应发生情况对比 观察组不良反应发生率26.92% 与对照组不良反应发生率30.77% 对比差异无统计学意义(P > 0.05)。见表4。
我国是乳腺癌高发国家,该病严重威胁女性身心健康。乳腺癌在早期发病时症状不明显甚至无症状,其早期症状容易与生理现象相混淆,常见于乳房胀痛、可触及乳房肿块为主,随着病情的发展,还会出现乳头溢液、乳腺变形等变化,主要有乳房皮肤橘皮状改变、局部凹陷、乳头回缩、乳头指向改变、乳头处皮肤瘙痒、破溃等表现[8]。乳腺癌的类型较多,其治疗会根据不同的类型以及分期进行综合性的判断,作为一种比较严重、具有较高转移率、较高化疗药物耐药性的类型,HER-2 阳性乳腺癌在乳腺癌中占比20% 左右,更易发生癌细胞的转移,且复发风险较高,对患者健康威胁严重,应对其及时开展有效且科学的治疗来实现早期治愈以及最大程度延长生存期[9]。化疗药物、靶向疗法等多种治疗方法的发展和应用为HER-2 阳性乳腺癌患者提供更多的治疗选择,相关共识中提出,规范治疗是相关疗效获得保障的基础[10]。
紫杉类化疗方案基础上应用曲妥珠单抗治疗已经公认为一线治疗方案,曲妥珠单抗能作用于HER-2的基因表达中,与其结合后可以激活患者自身的免疫系统,高选择作用于HER-2 细胞外部位而抑制癌细胞的基因表达;还可以阻断HER-2 细胞外第四结构人源化单克隆抗体相关信号的通路,降低其癌基因的相关酶物质活性,逐渐降低其恶性作用。郝凯峰等学者[11] 在化疗基础上联合曲妥珠单抗治疗晚期HER-2 乳腺癌患者的生存率36.36%,比单化疗治疗高出约22%。但是不断的临床实践发现曲妥珠单抗对HER-2 的基因信号控制并不全面,因此依然有部分患者对曲妥珠单抗治疗并不敏感。林红霞等[12] 在老年人HER-2 阳性转移性乳腺癌中应用长春瑞滨联合双靶治疗的肿瘤控制率中体现出比单靶更理想的效果。帕妥珠单抗也是一种人源化单克隆抗体,在抗HER-2 机制中是通过与该基因的CR1 区域结合,作用于HER-2 细胞内通道而形成异源二聚体,阻断其信号通道。本次研究分析双靶治疗效果,结果双靶治疗组的治疗有效率、生活质量评分改善上更领先,同时治疗的安全性上与单靶治疗相似,与马祥敏等[13]的研究结果有诸多的交叉结论,说明双靶治疗用于此类型乳腺癌新辅助治疗中可靠性和科学性。新辅助治疗后术后病理观察组缓解率较对照组更高,分析原因考虑可能与两种靶向药物的作用有关,虽然曲妥珠单抗、帕妥珠单抗均同样具有抗HER-2 的作用,但是与HER-2 结合位点以及靶区域、作用机制上不同,
 实施双靶治疗可以进行抗HER-2 抗体的互补,增加控制通道,从而促进疗效。
实施双靶治疗可以进行抗HER-2 抗体的互补,增加控制通道,从而促进疗效。
综上所述,双靶治疗(曲妥珠单抗、帕妥珠单抗)治疗HER-2 阳性乳腺癌的效果要明显优于单靶治疗,不仅能够有效降低癌基因的表达,减轻炎症反应,还有助于患者生活质量的提升,同时也不增加不良反应。
[1] 辛灵,张虹,张爽,等. 多西他赛+ 卡铂联合曲妥珠单抗方案对早期人表皮生长因子受体2 阳性乳腺癌的新辅助治疗效果[J]. 中华外科杂志,2021,59(3):222-227.
[2] 熊炳钧,吕大鹏,曹冰清,等. 229 例人表皮生长因子受体2 阳性Ⅳ期乳腺癌患者曲妥珠单抗的治疗分析[J]. 癌症进展,2021,19(1):23-27,45.
[3] 邹黎,钱军. 曲妥珠单抗联合不同化疗方案治疗人表皮生长因子受体-2 阳性晚期胃癌患者的回顾性研究[J]. 实用临床医药杂志,2020,24(4):36-39,44.
[4] 刘淑娟,陈秀兰,苏乌云,等. 曲妥珠单抗, 帕妥珠单抗联合应用于乳腺癌患者皮肤不良反应临床观察[J]. 内蒙古医科大学学报,2022,44(2):161-164.
[5] 任晓菲,贺宇彤,任曙光,等. 不同新辅助治疗方案对403 例乳腺癌患者HER2 表达状态的影响[J]. 中华肿瘤防治杂志,2022,29(9):669-673.
[6] 冯凌飞,贺曾. 赫赛汀联合多西他赛对人表皮生长因子受体2 阳性转移性乳腺癌的临床疗效[J]. 安徽医药,2020,24(10):2095-2098.
[7] 杨闻箫,国琳玮,凌泓,等. 基于免疫微环境特征的曲妥珠单抗与免疫治疗联合应用预测模型[J]. 中国癌症杂志,2023,33(5):484-498.
[8] 岳瑞雪,胡崇珠,郝鑫,等. 曲妥珠单抗和帕妥珠单抗联合不同化疗方案新辅助治疗HER-2 阳性乳腺癌真实世界疗效及安全性观察[J]. 中国肿瘤临床,2023,50(5):248-254.
[9] 杨锦,王倩荣,张俊美,等. 吡咯替尼治疗曲妥珠单抗耐药人表皮生长因子受体2 阳性晚期乳腺癌患者的近期效果及安全性[J]. 肿瘤研究与临床,2020,32(12):865-867.
[10] 杨艳芳,姜战胜,顾林. HER2 阳性乳腺癌治疗模式的进展和优化[J]. 中国肿瘤生物治疗杂志,2020,27(5):469-476.
[11] 郝凯峰,张明芳,仲广生. 吉西他滨联合曲妥珠单抗治疗人表皮生长因子受体2 阳性晚期乳腺癌的疗效[J]. 癌症进展,2023,21(1):105-107.
[12] 林红霞,刘小平,邓铖. 帕妥珠单抗联合曲妥珠单抗和长春瑞滨治疗老年人表皮生长因子受体2 阳性转移性乳腺癌的临床效果[J]. 中国医药,2022,17(3):345-348.
[13] 马祥敏,张香梅,周新平,等. 曲妥珠单抗和帕妥珠单抗联合化疗对HER2 阳性乳腺癌新辅助治疗的真实世界研究[J]. 肿瘤防治研究,2022,49(1):46-52.
查看更多