查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





2022年ESMO免疫肿瘤学大会(ESMO IO)将于12月7日-10日举行,本次大会涵盖了免疫治疗领域的重磅研究成果,来自全球的顶尖专家学者共聚一堂,共话热点。
替雷利珠单抗是百济神州自主研发的创新型程序性死亡受体-1(PD-1)抑制剂,其Fc段经过改造后最大限度减少了抗体依赖的细胞吞噬作用,减少了对于效应T细胞的消耗。基于RATIONALE-304,RATIONALE-307和RATIONALE-303三项研究的成功,替雷利珠单抗已获批联合化疗用于驱动基因阴性晚期非小细胞肺癌(NSCLC)一线治疗,以及单药用于二/三线NSCLC治疗。三项关键III期研究的成功,证实了替雷利珠单抗在驱动基因阴性晚期NSCLC一线/后线的全面获益。
此次大会公布了RATIONALE-304和RATIONALE-307两项研究的更新随访结果,本文将结合驱动基因阴性晚期NSCLC免疫治疗研究进展进行报道。
一、全面获益:晚期NSCLC免疫治疗进展
免疫治疗的出现全面变革了NSCLC治疗格局,从后线到一线, 免疫治疗已为晚期NSCLC患者带来全面获益:
替雷利珠单抗:唯一一个在晚期驱动基因阴性NSCLC III期研究中验证了全人群获益且没有失败记录的PD-(L)1单抗。

1)二/三线NSCLC免疫治疗
二/三线NSCLC免疫治疗历经了“彩虹”与“风雨”,多项III期研究的成功,奠定了IO在二线治疗新标准,也引起后续研究的对照组交叉接受IO治疗比例增加而潜在提升了对照组总生存期(OS),增加研究成功难度。RATIONALE-303研究后来者居上,尽管对照组20.4%的患者后续接受了IO治疗,替雷利珠单抗治疗组仍显示突出生存获益,且鳞癌和非鳞癌亚组一致显示同类研究中最大OS获益,为中国患者带来二线治疗新选择[1-10]。
![]6{I@MM0JM5DE]9W85TREAR.png ]6{I@MM0JM5DE]9W85TREAR.png](https://bcn.135editor.com/files/users/1246/12466084/202212/eRu8YY7u_XbuX.png)
2)一线非鳞状NSCLC免疫治疗
驱动基因阴性非鳞状NSCLC免疫治疗“百家争鸣”,多项III期研究均证实免疫联合化疗的获益。但各研究基线不尽相同,PD-L1表达分布存在差异,而PD-L1表达水平与非鳞癌免疫治疗疗效正相关,因此不同研究之间的对比需要考虑研究人群的不同。RATIONALE-304研究中PD-L1表达水平更接近真实世界数据,疗效数据更具代表性[11-16]。
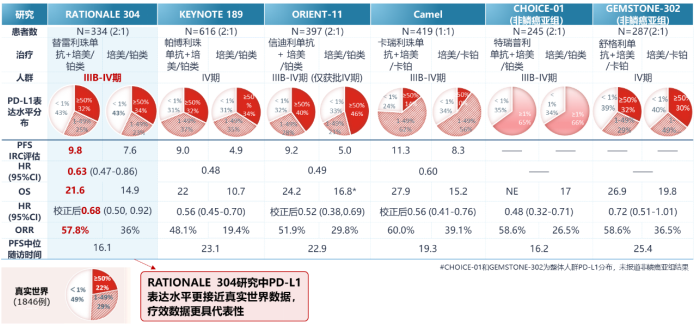
RATIONALE-304研究是一项III期、多中心、随机、开放研究,旨在评估替雷利珠单抗联合培美曲塞和铂类对比培美曲塞和铂类一线治疗晚期非鳞状NSCLC的疗效和安全性。中期分析无进展生存期(PFS)已达到主要终点,本次ESMO IO大会公布了更新分析的结果,替雷利珠单抗联合化疗组 vs 化疗组,显示出:
显著PFS获益:截至2020年10月26日,中位随访16.1个月,替雷利珠单抗联合化疗组的中位PFS达9.8个月,相较化疗组疾病进展风险显著降低37%。
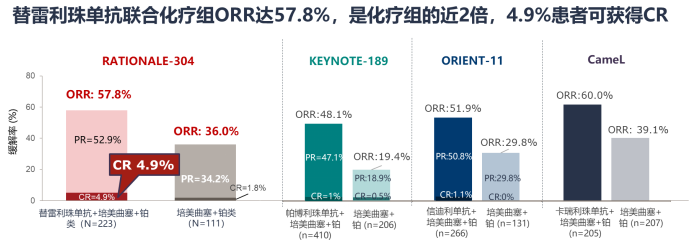
高缓解率和持久缓解:替雷利珠单抗联合化疗组客观缓解率(ORR)达到57.8%,是化疗组的近2倍,4.9%患者可达到完全缓解,中位缓解持续时间(DoR)为10.6个月。
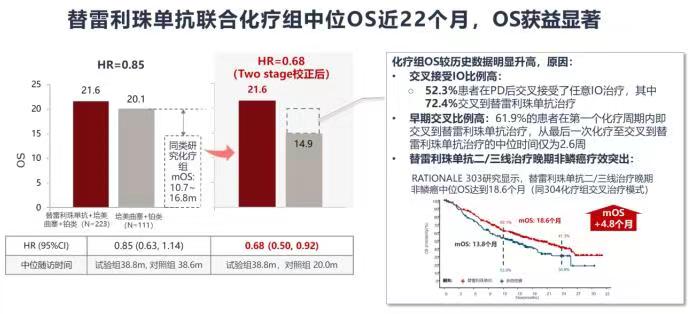
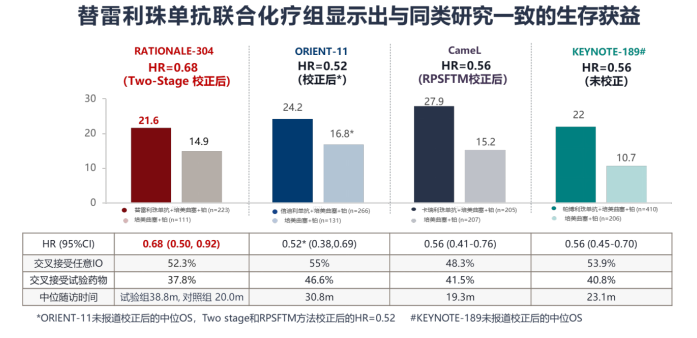
长期生存获益:截至2022年7月15日,替雷利珠单抗联合化疗组中位OS达到21.6个月,显示出长期生存获益。化疗组中位OS为20.1个月,明显高于历史数据,可能与交叉治疗及替雷利珠单抗单药后线疗效突出相关。通过敏感性分析,校正交叉治疗对对照组OS的影响后,替雷利珠单抗联合化疗组 vs 化疗组OS获益显著(中位OS: 21.6 vs 14.9个月,HR:0.68),患者死亡风险显著降低32%,与同类研究相当[11-14]。
 3) 一线鳞状NSCLC免疫治疗
3) 一线鳞状NSCLC免疫治疗
一线鳞状NSCLC免疫联合化疗研究“百花争艳”,其中中国原研药物研究尽显“中国特色”[19-24]:
立足中国人群特点,多项研究弥补不可根治局晚期患者数据。
提供丰富联合方案选择,满足临床多样化选择需求:RATIONALE-307研究独特设置替雷利珠单抗+紫杉醇/白蛋白紫杉醇+卡铂两个试验组,同时获批联合紫杉和白紫方案。
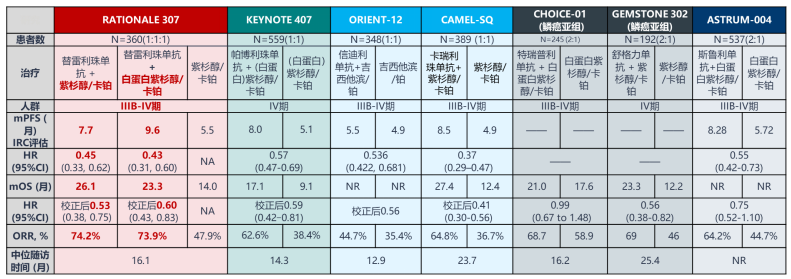
RATIONALE-307研究是一项III期、多中心、随机、开放研究,旨在评估替雷利珠单抗联合紫杉醇/白蛋白紫杉醇及卡铂对比紫杉醇及卡铂一线治疗晚期鳞状NSCLC的疗效和安全性。中期分析PFS已达到主要终点,本次ESMO IO大会公布了更新分析的结果,替雷利珠单抗联合化疗两组 vs 化疗组,显示出:
显著PFS获益:截至2020年9月30日,中位随访18.7个月,替雷利珠单抗联合紫杉醇/卡铂和白蛋白紫杉醇/卡铂两组的中位PFS分别达到7.7个9.6个月,疾病进展风险显著下降超55%。

高缓解率和持久缓解:替雷利珠单抗+紫杉醇/白蛋白紫杉醇+卡铂两组的ORR高达74.2%和73.9%,分别有5.8%和6.7%患者可达到完全缓解,中位DoR为8.4和8.6个月。
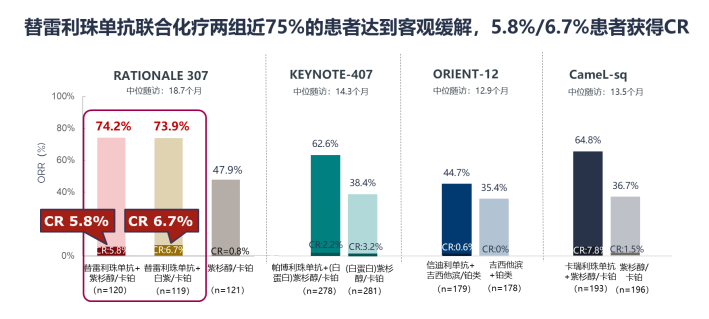
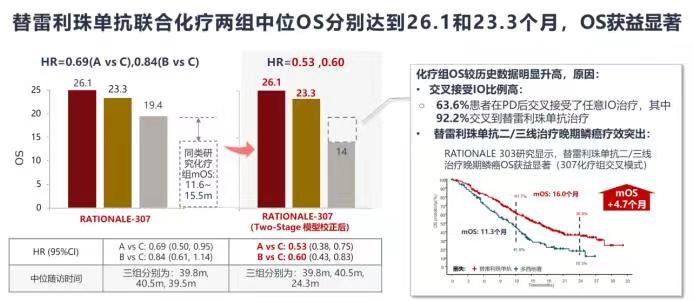
长期生存获益:截至2022年7月15日,替雷利珠单抗+紫杉醇/白蛋白紫杉醇+卡铂两组的中位OS分别为26.1和23.3个月,显示出长期生存获益。化疗组中位OS为19.4个月,明显高于历史数据,可能与交叉治疗及替雷利珠单抗单药后线疗效突出相关。通过敏感性分析,校正交叉治疗对对照组OS的影响后,替雷利珠单抗联合化疗两组 vs 化疗组OS获益显著(中位OS: 26.1 vs 23.3 vs 14.0个月,A vs C: HR=0.53,B vs C: HR=0.60),患者死亡风险显著降低47%和40%,与同类研究相当[19-22,26]。
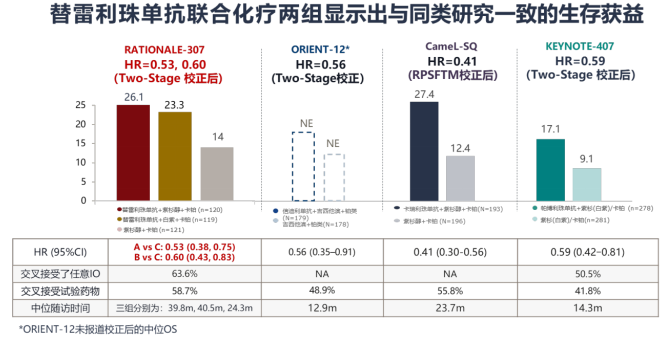
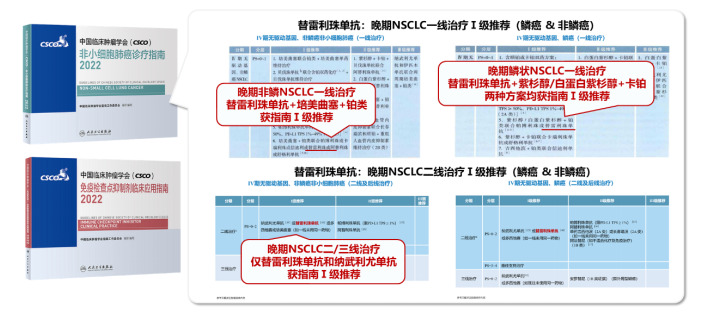
基于RATIONALE-303,304和307三项研究的突出表现,替雷利珠单抗已获得《CSCO 非小细胞肺癌诊疗指南》及《CSCO 免疫检查点抑制剂应用指南》两大权威指南在驱动基因阴性晚期NSCLC一线/后线的全面I级推荐[29-30]。
二、进无止境:晚期NSCLC免疫进阶探索展望
虽然免疫治疗已为驱动基因阴性晚期NSCLC患者带来全面获益,但仍存在诸多未解决的问题,需要更多进阶探索,例如:
探索更有效的免疫治疗策略,延缓耐药:
本次的ESMO IO大会上报道了一项替雷利珠单抗联合西达本胺(HDAC抑制剂)和化疗一线治疗晚期NSCLC的探索性研究结果[31]。研究共入组了20例患者,在19例疗效可评估患者中,ORR达到73.7%,疾病控制率(DCR)达到100%,其中腺癌患者ORR 60%,鳞癌患者ORR高达88.9%,中位PFS达到13.8个月,初步显示出良好的早期疗效信号,且整体安全性可控。
补充更丰富人群中免疫治疗的应用证据,惠及更多患者:
2022年WCLC大会报道了一项替雷利珠单抗联合白蛋白紫杉醇±铂类一线治疗晚期老年(年龄≥70岁) NSCLC的前瞻性研究[32],该研究独创性地聚焦在年龄≥70岁的NSCLC患者,并且采用个体化的治疗方案。研究共入组了33例患者,在26例疗效可评估的患者中,ORR达到57.7%,DCR达到92.3%。中位PFS达到14.7个月,大部分治疗相关不良反应(TRAEs)为1-2级,为晚期老年NSCLC患者的临床治疗决策提供了更多选择。
从后线到一线, RATIONALE-303,304和307三项研究彰显硬核实力,夯实了替雷利珠单抗在驱动基因阴性晚期NSCLC一线/后线的全面获益。未来以免疫为基石的进阶治疗策略探索,以及更丰富免疫治疗人群的探索,有望为临床决策提供更多治疗选择,驱动更多患者实现“全面获益”。
参考文献:
1. Brahmer J, et al. N Engl J Med 2015;373:123-35.
2. Borghaei H, et al. N Engl J Med 2015;373:1627-39.
3. Herbst RS, et al. Lancet 2016; 387: 1540–50.
4. Rittmeyer A, et al. Lancet. 2017; 389(10066): 255–265.
5. Yilong Wu, et al. J Thorac Oncol. 2019;14(5):867-875.
6. Barlesi F, et al. Lancet Oncol. 2018;19(11):1468-1479.
7. Planchard D, et al. Ann Oncol. 2020;31(5):609-618.
8. 2020 ESMO 1262P.
9. Yuankai S, et al. 2021 AACR CT041.
10. Caicun Z, et al. J Thorac Oncol. 2022; S1556-0864(22)01803-2.
11. Shun L, et al. 2022 ESMO IO 138P.
12. Gadgeel S, et al. J Clin Oncol. 2020;38(14):1505-1517.
13. Li Z, et al. Lung Cancer. 2022;171:56-60.
14. Caicun Z, et al. 2020 WCLC.
15. Jie W, et al. J Clin Oncol. 2022; JCO2200727.
16. Caicun Z, et al. Lancet Oncol. 2022;23(2):220-233.
17. Li Z, et al. J Thorac Oncol. 2020;15(10):1636-1646.
18. Caicun Z, et al. Lancet Respir Med. 2021;9(3):305-314.
19. Jie W, et al. 2022 ESMO IO 132P.
20. Paz-Ares L, et al. J Thorac Oncol. 2020;15(10):1657-1669.
21. Caicun Z, et al. J Thorac Oncol. 2021;16(9):1501-1511.
22. Caicun Z, et al. 2022 ELCC.
23. Jie W, et al. J Clin Oncol. 2022; JCO2200727.
24. Caicun Z, et al. Lancet Oncol. 2022;23(2):220-233.
25. Caicun Z, et al. J Thorac Oncol. 2022;17(4):544-557.
26. Pingyu C, et al. Front Public Health. 2022;10:956792.
27. Shun L, et al. J Thorac Oncol. 2021;16(9):1512-1522.
28. Jie W, et al. JAMA Oncol. 2021;7(5):709-717.
29. 2022 CSCO非小细胞肺癌诊疗指南.
30. 2022 CSCO免疫检查点抑制剂临床应用指南.
31. Yi H, et al. 2022 ESMO IO 131P.
32. Bo S, et al. 2022 WCLC EP08.01.
查看更多