查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





一般资料:患者男性,50岁,于2020年1月就诊。
主诉:食欲下降1个月余,查体发现肝占位10天。
既往史:乙肝病史10年,间断服用抗病毒药物治疗。
个人史及家族史:长期吸烟半包/天,偶尔饮酒;余无特殊。
ECOG PS评分:0分
查体:黄疸征(-),肝右肋下2 cm可扪及,质中,无压痛反跳痛,移动性浊音(-)。
乙肝抗原:乙肝表面抗原7447.0 COI(↑),乙肝病毒DNA定量2.05×104copies/ml(↑)。
肿瘤标记物:甲胎蛋白(AFP)17892 ng/ml(↑),CA19-9 116.70 U/ml(↑)。
胸腹盆CT增强(2020年1月30日):肝右后叶可见长径约为15 cm低密度肿块影,分叶状,瘤周散在小结节,均可见廓清征象,门脉右支示充盈缺损,如图1所示。

图1 治疗基线胸腹盆部CT增强
临床诊断:1.原发性肝细胞癌,BCLC C期,CNLC分期Ⅲa期,肝功能Child-Pugh分级A级,PVTT Ⅱ型;2.慢性乙型病毒性肝炎
治疗方案:经多学科会诊,肝胆外科认为Ⅲa期HCC,暂不考虑手术;肿瘤内科认为可行系统化疗,或在基因检测后尝试靶向治疗;放疗科认为肝内病灶较大,暂不适合外放疗及粒子置入治疗,癌栓可考虑放疗;介入科任务患者肝内病灶>5cm,不适合消融治疗。综合各科室意见,并与患者及家属沟通后,予患者经动脉化疗栓塞(TACE)联合索拉非尼治疗,患者先后于2020年1月31日及2020年3月2日进行TACE治疗(分别如图2及图3所示),并于2020年2月6日开始口服索拉非尼治疗。

图2 首次TACE治疗

图3 第二次TACE治疗
影像学及疗效评价:患者先后于首次(2020年2月27日)及第二次(2020年4月14日)TACE治疗后复查腹部CT,如图4所示。首次治疗后腹部CT见肝右叶可见长径15cm肿块,内见碘油沉积,周围可见卫星灶,门静脉右后支低密度充缺,根据mRECIST疗效评价,病情稳定(SD)。第二次治疗后腹部CT见肝右叶可见长径11.6cm肿块,内见碘油沉积影;门静脉右后支示充盈缺损。双肺见多发类圆形结节影,部分聚集生长,大者长径约1.5cm。诊断:肝癌介入治疗后改变,较前片缩小;门静脉瘤栓形成;双肺多发结节,考虑转移。根据mRECIST疗效评价,病情进展(PD)。



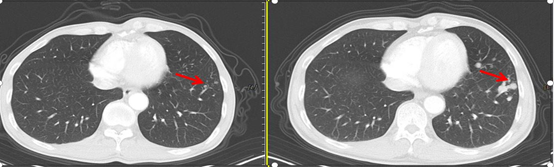
图4 左右分别为首次和第二次TACE治疗后影像学变化
治疗安全性评价:患者曾于TACE治疗后出现上腹疼痛、低热及I度肝功能异常,分别予止痛治疗疼痛可缓解、物理退热后体温可降至正常、保肝治疗后肝功能可恢复。应用索拉非尼期间曾出现血压升高(CTCAE I级,血压最高158/80mmHg)及手足综合征,予对症治疗后可缓解。
第二阶段治疗:TACE+免疫+靶向
治疗方案:因患者疾病进展,于2020年5月开始,予患者调整为TACE+免疫+靶向治疗方案,患者于2020年5月15日接受第三次TACE治疗,术中DSA示右肝结节样肿瘤染色,腹腔动脉、肝右动脉灌注洛铂50mg,微导管超选至肿瘤供血动脉,缓推300~500 μm栓塞微球0.9瓶,碘化油6ml栓塞,栓塞后造影肿瘤染色消失。患者于2020年5月14日开始接受替雷利珠单抗200mg q3w+瑞戈非尼80~120mg qd治疗,至2020年10月31日,患者共接受7周期免疫治疗。
影像学及疗效评价:患者治疗期间,定期复查影像学检查,2周期治疗后(2020年6月14日)复查如图5所示,见肝右后叶可见不规则低密度肿块影(4.3 cm×8.5 cm),分叶状,强化不明显,内见低密度坏死区及高密度碘油沉积影,门静脉右支可见低密度充缺,根据mRECIST疗效评价为部分缓解(PR)。此后患者定期复查,肝脏病灶逐渐缩小,至2021年3月2日末次复查时,患者肝脏原发及肺转移病灶增强CT完全没有强化,病灶已完全坏死,根据mRECIST疗效评价为完全缓解(CR),治疗期间病灶动态变化如图6所示。



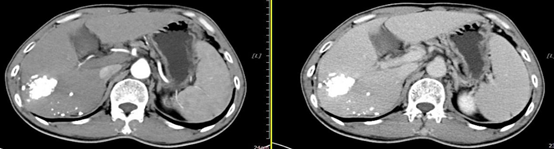

图5 左右分别为免疫联合治疗前及2周期治疗后影像学变化

图6 免疫联合治疗期间影像学变化
不良反应及治疗:治疗期间曾出现轻度甲状腺功能减退,给予小剂量左甲状腺素钠口服治疗后缓解。
本例患者中年男性,乙肝病史10年,因“食欲下降1个月余,查体发现肝占位10天”为主诉就诊,结合患者病史及辅助检查结果,明确诊断为原发性肝癌,BCLC分期 C期,CNLC分期Ⅲa期。患者腹部增强CT示肝右后叶巨块型肝癌并局部卫星灶形成,门静脉右支癌栓形成,经MDT会诊,评估肿瘤不适合手术切除及放疗,根据《原发性肝癌诊疗规范(2019年版)》[1]治疗推荐,给予介入治疗(TACE)联合靶向治疗,治疗后患者肝脏病灶未得到有效控制,并出现了肺转移病灶,疗效评价为PD,此时肝功能也较前下降,肝功能Child-Pugh分级从A级变为B级。予患者二线调整为TACE+免疫治疗(替雷利珠单抗)+靶向治疗(瑞戈非尼)方案,2个月后复查时患者肝脏原发病灶及肺转移灶均较前缩小,疗效评价为PR,在后续的治疗后,患者肿瘤持续退缩,至2020年8月11日复查时,患者病灶完全坏死,达疗效CR;更为可贵的是,患者在后续的治疗中,至2021年3月2日的末次复查,患者疗效仍持续CR。安全性方面,患者在免疫联合治疗期间安全性及耐受性较好。治疗期间AFP、CA19-9动态变化如图7及图8所示。
图7 治疗期间AFP动态变化
图7 治疗期间CA19-9动态变化
原发性肝癌是目前我国第4位常见恶性肿瘤及第2位肿瘤致死病因,严重威胁我国人民的生命和健康[1]。肝癌起病隐匿,早期诊断困难,病情进展迅速,大部分患者初诊时即诊断为疾病中晚期,无法进行根治性手术治疗,正如本例患者,确诊时已出现了门静脉癌栓,处于CNLC分期IIIa期,无法进行手术治疗。
目前TACE是不能手术的中晚期肝癌最常用的治疗手段之一,但对于巨大或合并脉管侵犯的肿瘤,单纯TACE等局部治疗降期后的转化成功率及手术比例仍偏低,肿瘤坏死不完全;且由于中晚期肝癌的全身性疾病特征,局部治疗虽能够使病灶缩小、切除率提高,但单纯提高切除率不一定能够提高患者的生存率。也正基于以上原因,《原发性肝癌诊疗规范(2019年版)》中,对于中晚期肝癌,积极主张综合治疗[1]。而《中国临床肿瘤学会(CSCO)原发性肝癌诊疗指南(2020版)》也主张酌情通过TACE联合系统治疗等其他方法,产生协同增效作用,以更好地控制肿瘤进展,提高患者生活质量和延长患者带瘤生存时间[7]。
近年来,靶向治疗经验的广泛积累、免疫治疗的成功突破,为肝癌患者带来了新的治疗希望。本例患者在确诊时为肝细胞癌合并门静脉癌栓状态,对于此类患者,靶向药物现已成为国际标准一线治疗推荐,但靶向单药治疗在控制肿瘤方面的效果欠佳,其联合局部或免疫治疗研究所取得的突破,意味着靶向药物治疗需联合局部治疗或其他系统治疗有望更好地提高中晚期肝癌的疗效[8]。正如本例患者,在一线治疗时,患者接受了TACE联合索拉非尼治疗,但病灶并未得到有效控制,一线治疗以失败告终。根据ESMO、EASL、NCCN、AASLD、CSCO等国内外权威指南的治疗推荐[2-6],免疫治疗是晚期HCC治疗的新选择。对于本例患者,在先前TACE联合靶向治疗的基础上,加用了替雷利珠单抗联合治疗,经过7次免疫治疗,疗效评价达到了完全缓解,取得了非常好的治疗效果。
免疫治疗是近年来肝癌系统治疗的重点研究方向,极大地改善了肝癌患者的预后,并有望改变肝癌的治疗模式。其中,免疫检查点抑制剂(ICI)程序性死亡受体-1(PD-1)/程序性死亡受体-1配体(PD-L1)抑制剂在晚期肝癌治疗中表现尤为突出。替雷利珠单抗是国内自主研发的创新型PD-1抑制剂,其具有与PD-1高亲和力和特异性结合的能力;此外通过基因工程技术对抗体Fc段改造,使其与巨噬细胞FcγR的结合能力最小化,从而防止巨噬细胞通过抗体依赖的细胞吞噬作用清除激活的T细胞,避免抗PD-1治疗发生耐药[8]。研究显示,替雷利珠单抗单药治疗经治晚期肝癌患者,ORR达12.2%,DCR达56.3%[9]。此外,替雷利珠单抗治疗中国晚期肝癌患者的疗效也可圈可点,2019年CSCO会议上的口头报告提出[10],替雷利珠单抗治疗中国不可手术的晚期HCC患者ORR达17%,DCR为56%,在同类药物中处于领先水平。
替雷利珠单抗独特的药学特性,能够发挥良好的抗肿瘤效果,在一众PD-1抗体药物中脱颖而出。免疫联合治疗方案也取得了令人振奋的疗效,在本例患者的治疗结果中得到了很好的体现。TACE+靶向治疗+免疫治疗的方案值得进一步探索,在未来的研究中进一步探索其达到如此好疗效的深层次原因,以便更有效地筛选出真正可以从联合治疗中获益的人群。
参考文献:
[1] 吴孟超, 汤钊猷, 刘允怡,等. 原发性肝癌诊疗规范(2019年版)[J]. 中国实用外科杂志, 2020(2):121-138.
[2] Vogel A, et al. Ann Oncol, 2018, 29(S4):iv238-iv255.
[3] NCCN Guidelines.Hepatobiliary Cancers Version 2.2018 -June 7, 2018.
[4] 中国临床肿瘤学会. 原发性肝癌诊疗指南. 人民卫生出版社. 2018.
[5] EASL.J Hepatol. 2018 Jul;69(1):182-236. 、
[6] Heimbach JK, et al.Hepatology. 2018 Jan;67(1):358-380
[7] 2020版中国临床肿瘤学会(CSCO)《原发性肝癌诊疗指南》
[8] 傅毅振,等. 2019年原发性肝癌治疗进展. 肿瘤综合治疗电子杂志, 2020, 2(6), 86-89.
[5] El-Khoueiry AB, et al. Nivolumab in patients with advanced hepatocellular carcinoma (CheckMate 040): an open-label,non-comparative, phase 1/2 dose escalation and expansion trial[J].Lancet, 2017, 389(10088): 2492-2502.
[6] Yau T, et al. CheckMate 459: A randomized, multicenter phase III study of nivolumab (NIVO) vs sorafenib(SOR) as first line(1L) treatment in patients (pts) with advanced hepatocellular carcinoma (aHCC)[J]. Ann Oncol, 2019, 30(5 suppl): LBA38.
[7] Zhu AX, et al. Pembrolizumab in patients with advanced hepatocellular carcinoma previously treated with sorafenib(KEYNOTE-224): a non-randomised, open-label phase 2 trial[J]. Lancet Oncol, 2018, 19(7):940-952.
[8] Zhang T, Song X, Xu L, et al. The binding of an anti-PD-1 antibody to FcγRΙ has a profound impact on its biological functions[J]. Cancer Immunology, Immunotherapy, 2018.
[9] BGB-A317-001.
[10] 沈琳,2019 CSCO.
中国医学论坛报编辑|金金 整理
查看更多