查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





美国临床肿瘤学会(ASCO)年会是全球肿瘤领域的盛会,来自世界各地的专家学者借此机会交流最新的研究进展,探究学术前沿。
世界卫生组织国际癌症研究机构(IARC)发布的全球癌症数据显示,在癌症分布类型上,2020年乳腺癌新发病例数达226万人,首次超过肺癌(220万人),成为“全球第一大癌”。
在本次ASCO年会上,乳腺癌领域研究成了关注的重点,那么究竟有哪些亮点研究可能乳腺癌患者带来新的福音呢?本报特邀江苏省人民医院殷咏梅教授对ASCO年会中乳腺癌精彩内容进行盘点。
DESTINY-Breast04研究:T-DXd对比医生选择治疗(TPC)方案治疗HER2低表达不可切除或转移性乳腺癌患者的随机、对照Ⅲ期研究(摘要号LBA3)
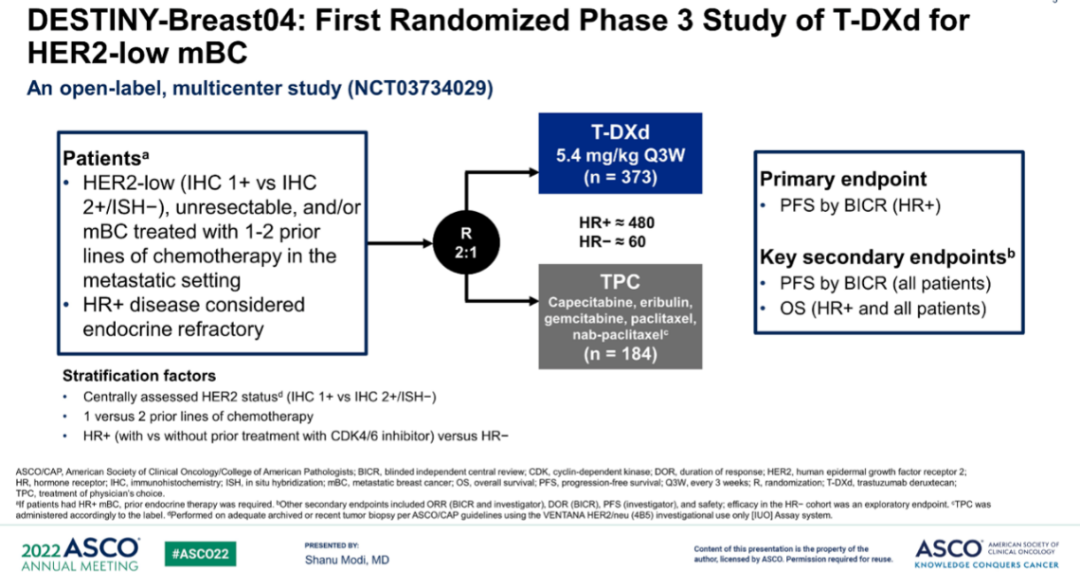
DESTINY-Breast04研究纳入既往内分泌治疗进展的表皮生长因子受体2(HER-2)低表达不可切除和/或转移性乳腺癌(mBC)患者,评估T-DXd相比医生选择化疗方案(卡培他滨、艾立布林、吉西他滨、紫杉醇或白蛋白紫杉醇)的疗效和安全性。
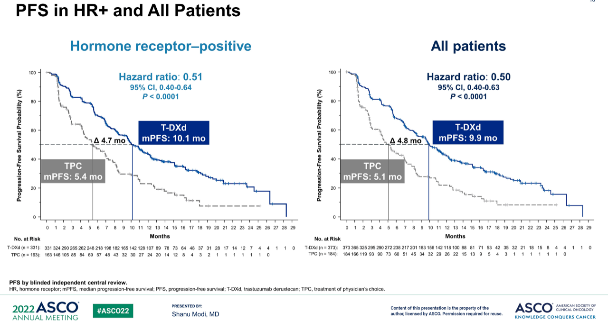
研究结果显示,激素受体(HR)+人群中,T-DXd组和医生选择治疗组的中位无进展生存(PFS)分别为10.1个月和5.4个月(HR=0.51,95%CI:0.40~0.64,P<0.0001);总人群中,T-DXd组和TPC组的中位PFS分别为9.9个月和5.1个月(HR=0.50,95%CI:0.40~0.63,P<0.0001)。
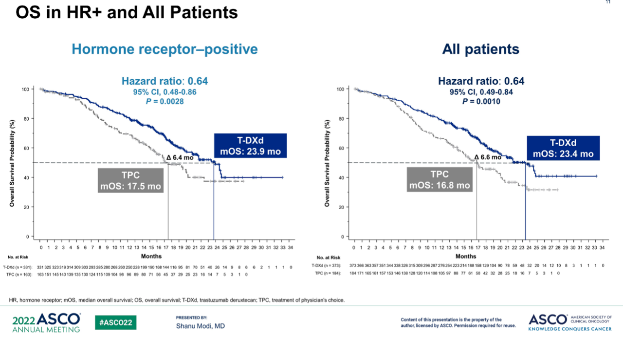
在总生存(OS)期方面,HR+人群中,T-DXd组OS相较于TPC组延长6.4个月(23.9个月对17.5个月,HR=0.64,95%CI:0.48~0.86,P=0.0028);总人群中,T-DXd组OS相较于TPC组延长6.6个月(23.4个月对16.8个月,HR=0.64,95%CI:0.49~0.84,P=0.0010)。
探索性终点方面,在HR-人群中,T-DXd组相比TPC组同样取得了有统计学意义的PFS及OS的延长。
安全性方面,T-DXd和TPC治疗期间不良事件(TEAEs)的发生率相似(99%对98%),且T-DXd治疗的≥3级TEAEs发生率低于TPC治疗(52.6%对 67.4%)。T-DXd组45例(12.1%)患者发生与药物相关的间质性肺疾病/肺炎,TPC组为1例(0.6%),未发现新的安全性问题。
TROPiCS-02研究:戈沙妥珠单抗对比TPC治疗HR+/HER2-晚期乳腺癌的随机、对照Ⅲ期研究
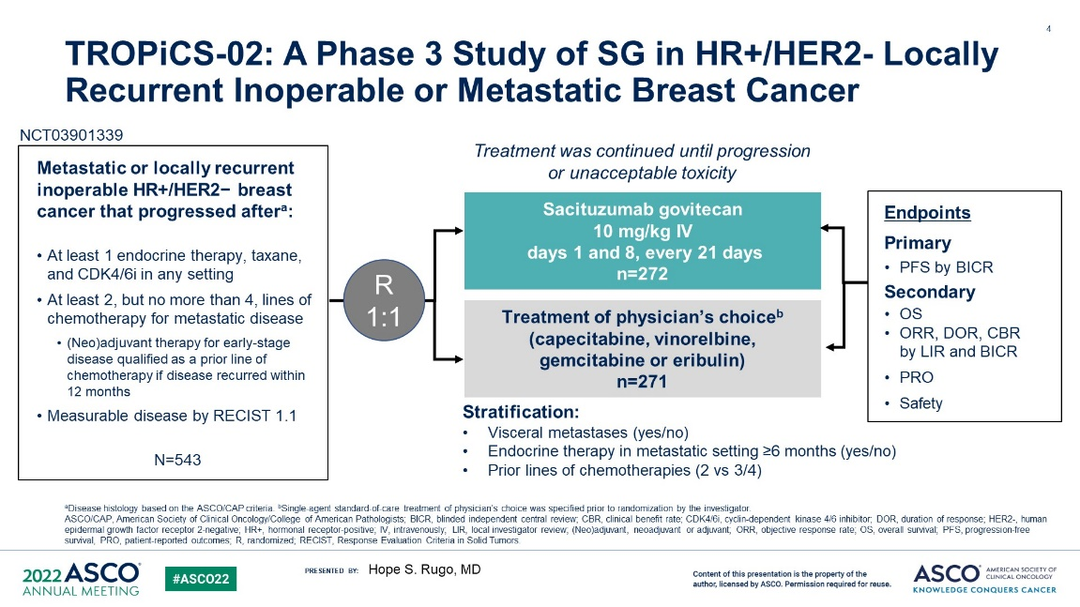
TROPiCS-02研究旨在评估戈沙妥珠单抗(SG)对比TPC在既往经内分泌治疗及2~4线化疗进展的HR+/HER2-局部晚期或转移性乳腺癌患者中的疗效与安全性,研究最终纳入543例患者,SG组和TPC组盲法独立中央审查(BICR)的中位PFS分别为5.5个月和4.0个月(HR=0.66,95%CI:0.53~0.83,P= 0.0003),6个月和12个月的PFS率分别为46% 对30%和21% 对 7%。
在OS方面,目前有约一半的总生存事件,SG组有数值上的延长但未显示统计学差异(13.9 个月对12.3个月;HR,0.84,95%CI:0.67~1.06,P=0.143)。
SG组安全性特征与既往研究一致,没有发现新的安全问题,并且SG组患者生活质量优于TPC组。
U31402-A-J101研究:靶向HER3的抗体药物偶联物(ADC)在HER3表达转移性乳腺癌患者中的Ⅰ/Ⅱ期研究(摘要号:1002)
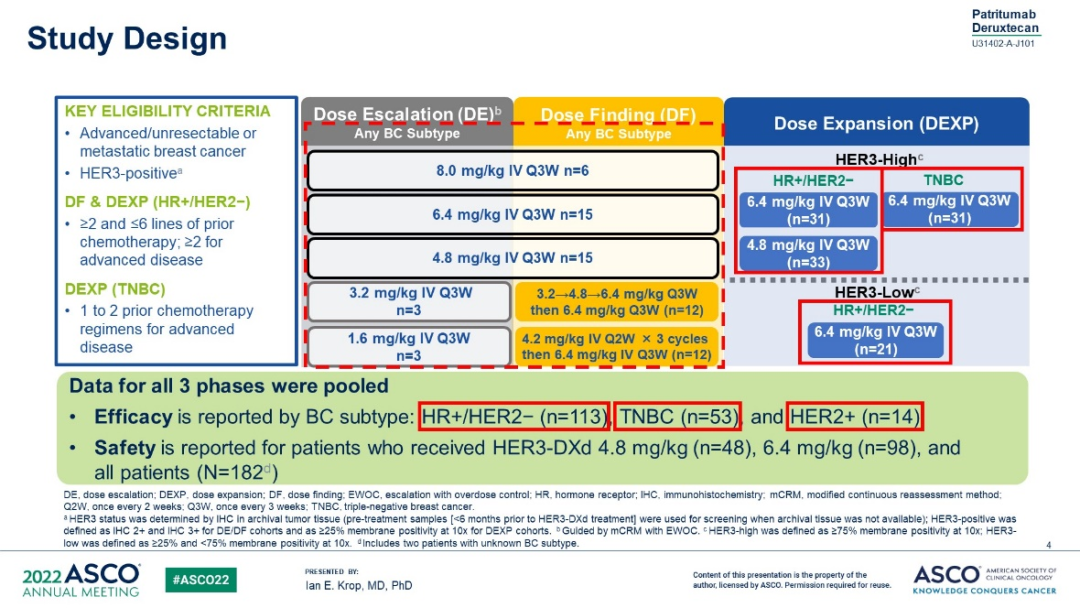
HER3-Dxd是一种靶向HER3的新型ADC药物,U31402-A-J101研究是一项多中心、开放标签、Ⅰ/Ⅱ期临床研究,旨在评估HER3-dxd在转移性乳腺癌患者中的安全性和有效性,研究分为剂量递增(3.2~8.0 mg/kg IV q3w)阶段和基于不同分子亚型的剂量探索阶段。研究共入组182例患者,晚期阶段中位治疗线数为5线。
结果显示,HR+/HER2-、三阴性和HER2阳性转移性乳腺癌患者的客观缓解率(ORR)分别为30.1%、22.6%和42.9%,疾病控制率(DCR)为7.2%、5.9%和8.3%。
安全性方面,共有130例患者(71.4%)出现≥3级TEAE,与停止治疗相关不良反应发生率整体较低(9.9%),胃肠道反应和血液学毒性是最为常见的治疗相关不良反应。
近年来众多新型ADC药物不断研发问世,可谓是“群雄逐鹿、异彩纷呈”,其卓越的疗效使得晚期乳腺癌的生存数据不断更迭。
随着乳腺肿瘤异质性研究的不断深入,HER2低表达这一变革性概念的提出打破了HER2“非阳即阴”的定义。
DB-04研究是T-DXd在乳腺癌抗HER2治疗历史上又一个具有里程碑意义的关键研究,研究结果提示:与标准治疗相比, T-DXd治疗HER2低表达mBC患者的PFS和OS均取得了有统计学意义和临床意义的提高。DB-04研究中大多数患者接受过多线治疗,既往中位治疗达3线,并且有70%左右的患者接受过细胞周期蛋白依赖性激酶4/6(CDK4/6)抑制剂治疗,研究入组人群符合当前临床实践的现状,具有极大的临床应用价值,T-DXd将为HER2低表达晚期乳腺癌人群带来新的靶向治疗标准。
Ⅲ期ASCENT研究证实了SG在难治复发转移性三阴性乳腺癌中的显著疗效,TROPiCS-02研究中SG进军HR+/HER2-乳腺癌患者,结果证实SG可显著降低晚期后线HR+/HER2-乳腺癌患者的疾病进展风险,总生存数据尚未完全成熟,但已表现出获益趋势,进一步夯实了其在靶向联合内分泌耐药的晚期HR+/HER2-乳腺癌中的价值。
30%~50%的乳腺癌患者存在HER3过表达,U31402-A-J101研究提示HER3-DXd在经过多线治疗的HER3表达晚期乳腺癌患者中具有可观的疾病缓解率,期待HER3-DXd的Ⅲ期临床研究结果,有望为HER3表达的乳腺癌患者提供新的治疗策略。
PALOMA-2研究总生存分析(摘要号LBA1003)
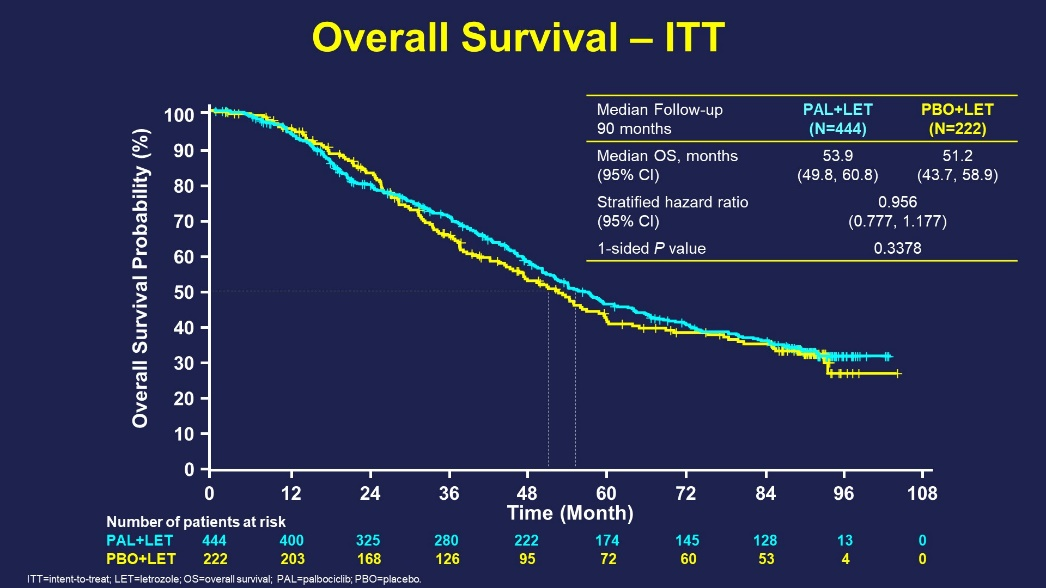
PALOMA-2研究是哌柏西利联合来曲唑对比来曲唑治疗绝经后ER+/HER2–晚期乳腺癌的Ⅲ期研究,本次ASCO会议公布了其总生存数据,中位随访时间90个月后,哌柏西利组和安慰剂组中位OS分别为53.9个月和51.2个月(HR=0.956,95%CI:0.777~1.177,P=0.3378)。
亚组分析显示:无病间期大于12个月,辅助阶段曾接受内分泌治疗和仅骨转移的患者获益显著。
MAINTAIN研究:CDK4/6抑制剂治疗失败的HR+/HER2-晚期乳腺癌患者,跨线再挑战瑞博西利联合内分泌治疗(摘要号LBA1004)
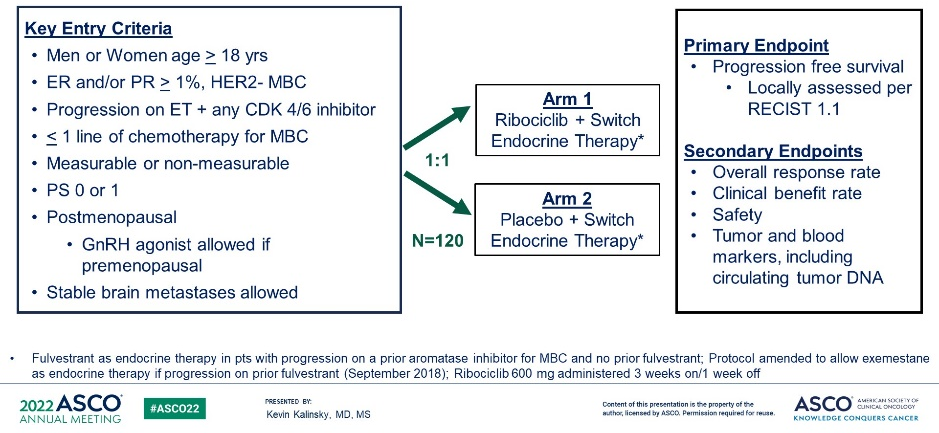
MAINTAIN研究是一项随机、双盲、安慰剂对照Ⅱ期试验,旨在评估CDK4/6抑制剂治疗进展后换用内分泌治疗搭档联合瑞博西利的疗效,研究共入组119例患者,其中86%的患者前线CDK4/6抑制剂为哌柏西利。
研究结果显示,氟维司群或依西美坦联合瑞博西利相比安慰剂组中位PFS显著延长(5.29个月对 2.76个月,HR=0.57,95%CI:0.39~0.95,P=0.006)。
瑞博西利组和安慰剂组6个月的PFS率分别为41.2%和23.9%,12个月的PFS率分别为24.6%和7.4%。
哌柏西利、阿贝西利和瑞博西利在HR+/HER2-乳腺癌晚期一线的总生存获益不尽相同。
本次大会公布的PALOMA-2研究提示哌柏西利联合来曲唑与来曲唑单药相比,总生存数值上体现一定程度的延长,但未达到统计学差异。而纳入2888例HR+/HER2-乳腺癌患者的大样本P-reality X真实世界研究提示哌柏西利联合AI对比AI单药治疗总生存有显著获益,是PALOMA-2 OS数据的有效补充,因此,临床实践中应辩证看待统计学数据,PALOMA-2的阴性结果并不能完全否定哌柏西利在生存上的获益。
在CDK4/6抑制剂成为一线治疗的标准后,二线治疗中对于前线使用过CDK4/6抑制剂的患者如何选择方案一直是争议的热点及临床治疗的难点。
MAINTAIN研究提示在一种CDK4/6抑制剂耐药后,跨线再挑战瑞博西利联合内分泌治疗是临床治疗中的可选策略。该研究为小样本Ⅱ期研究,其结论需进一步Ⅲ期临床研究证实。
CDK4/6抑制剂跨线治疗的疗效生物标志物,以及与其他内分泌联合治疗方案包括磷酸肌醇3激酶(PI3K)抑制剂、依维莫司、组蛋白去乙酰化酶(HDAC)抑制剂等孰优孰劣,需要未来的临床研究数据给到我们答案。
伊匹木单抗和纳武利尤单抗联合紫杉醇新辅助治疗以蒽环类药物为基础的新辅助化疗后耐药的早期三阴性乳腺癌患者(摘要号602)
该研究为单臂Ⅱ期临床试验,入组经蒽环类药物新辅助治疗4周期后残余肿瘤大小≥15 mm或肿瘤为10 mm且伴有一个阳性淋巴结的三阴性乳腺癌患者,接受伊匹木单抗和和纳武利尤单抗联合紫杉醇新辅助治疗。
研究共入组34例患者,33例可评价主要终点。所有可评价患者的病理学完全缓解(pCR)率为24.2%,程序性死亡受体配体1(PD-L1)阳性患者为37.5%,PD-L1阴性患者为23%。在14个月中位随访期内,12个月无事件生存(EFS)率估计为85%,12个月OS率为94%。
KEYNOTE-B49研究:帕博利珠单抗联合化疗用于局部复发不可手术或转移性HR+/HER2乳腺癌患者的随机、双盲、Ⅲ期研究(摘要号1118)
KEYNOTE-B49研究纳入既往内分泌治疗后疾病进展的PD-L1阳性、HR+/HER2-局部复发不可手术或转移性乳腺癌患者,评估化疗联合帕博利珠单抗或安慰剂的疗效与安全性。
研究分层因素包括PD-L1表达(CPS 1-9对 ≥10)、是否存在内脏转移(是对否)和研究期间化疗方案(紫杉烷对多柔比星脂质体对卡培他滨),主要终点为BICR评估的PFS以及PD-L1 CPS≥10和≥1患者的OS,目前204家国际研究中心正在进行入组。
乳腺癌的免疫治疗仍然是机遇和挑战并存,IMpassion031研究和KEYNOTE-522研究证实免疫检查点抑制剂联合化疗可提升三阴性乳腺癌新辅助治疗的pCR率,免疫联合免疫治疗作为一种新的治疗模式,在晚期乳腺癌中的小样本临床研究初露锋芒。
本届ASCO大会公布的在蒽环类新辅助治疗疗效不佳的患者中序贯双免疫联合化疗的模式,为三阴性乳腺癌患者的新辅助免疫治疗提供了新的思路。
免疫检查点抑制剂在晚期TNBC中的阳性数据使其逐步向HR+/HER2-乳腺癌中拓展,KEYNOTE-B49是首个免疫治疗联合化疗在HR+/HER2-晚期乳腺癌中的Ⅲ期对照研究,期待研究结果的公布,以期明确免疫联合化疗在HR+/HER2-患者中的疗效及优势人群。

殷咏梅教授
江苏省人民医院
教授,主任医师,博士生导师
江苏省人民医院妇幼分院副院长
中国临床肿瘤学会(CSCO)副理事长
北京希思科临床肿瘤学研究基金会副理事长
CSCO乳腺癌专家委员会副主任委员
中国抗癌协会乳腺癌专业委员会常委
CSCO患者教育专家委员会候任主任委员
查看更多