查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





定义与分类
机化性肺炎(OP)是损伤的肺组织自我修复的过程,可分为隐源性机化性肺炎(COP)和继发性机化性肺炎(SOP)。SOP指由特定的原因如药物毒性、放射治疗、吸入性损伤等引起,或与明确的临床疾病如感染、结缔组织病、炎症性肠病、器官移植、恶性肿瘤、其他类型的间质性肺疾病等相关。COP病因不明,被认为是特发性间质性肺炎(idiopathic interstitial pneumonias, IIP)的一种类型,易被误诊漏诊,如早期识别并及时治疗,大多数病例可较快缓解。
病理特点
OP的发病机制尚不明确。从病理的角度看,肺组织结构似乎未受到严重破坏,其发生发展过程如下:①肺泡损伤:早期,I型肺泡上皮细胞坏死和基底层剥脱致血浆蛋白渗漏、纤维蛋白沉积和炎性细胞迁移至肺泡腔(图1A);②肺泡腔机化:成纤维细胞通过基底膜进入肺泡腔,增殖分化为肌成纤维细胞,参与形成OP特征性的肉芽组织栓,即Masson小体(图1B)。③重塑:病情恢复阶段,炎性细胞和纤维蛋白沉积物从肺泡肉芽组织栓中消退,肌成纤维细胞与由Ⅲ型前胶原、胶原纤维和纤连蛋白等构成的胶原蛋白束呈同心圆样交替排列,逐渐融入肺泡壁并被重塑为肺间质。I型肺泡上皮快速增殖覆盖胶原束,并恢复肺泡毛细血管膜的连续性和肺泡单位的完整性(图1C)。因此,OP的镜下病理特征主要为炎性细胞浸润,肺泡腔、肺泡管内可见纤维黏液样变及肉芽组织栓(图2)。
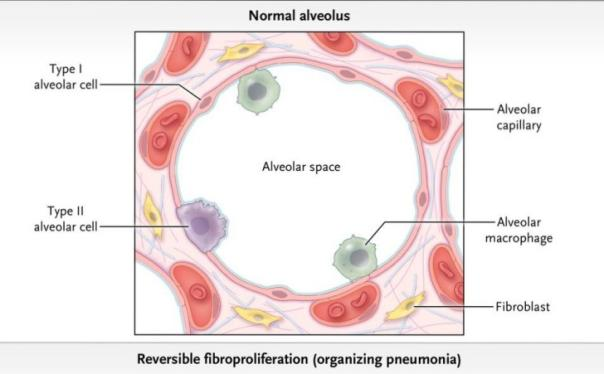
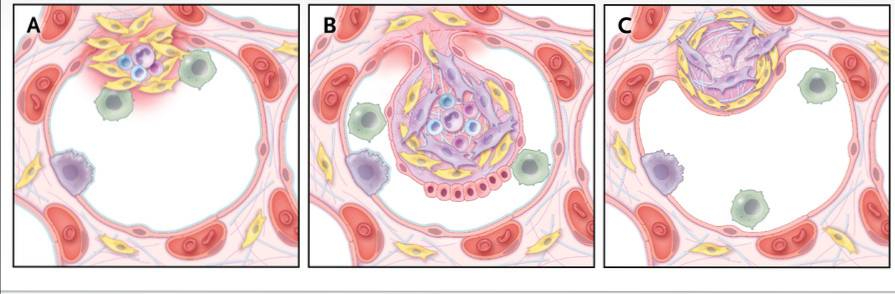
图1 OP可逆的纤维性增生过程
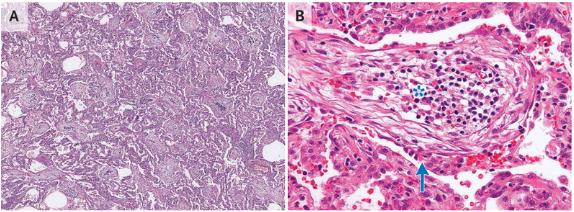
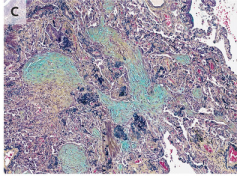
图2 OP的组织病理特征
图2A:多个肺泡腔内可见不同形状的疏松结缔组织填塞,肺泡壁呈炎症浸润状态并轻度增厚,无明显纤维化;图2B:肺泡腔内呈纤维黏液样变,并混有炎性细胞(星号),扁平状再生上皮(箭头)细胞覆盖肉芽组织;图2C:肺泡腔内的疏松结缔组织通过Kohn孔相连,呈蝴蝶状。
临床特征
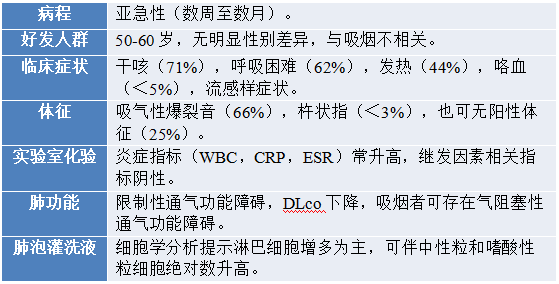
回顾并总结相关文献,COP的临床特征缺乏特异性(表1)。值得注意的是,OP可早在结缔组织病出现症状前数周,甚至数月出现,因此,拟诊COP前有必要行相关抗体(如ANAs、抗CCP抗体、抗dsDNA抗体、抗scl-70抗体、抗Jo-1抗体等)检查。另外,支气管肺泡灌洗检查有助于明确有无感染,其中不同炎性细胞的升高对寻找OP的继发因素(如过敏性肺炎、嗜酸粒细胞性肺炎等)也有一定价值。
表1 COP的临床特征
影像表现
影像学上,COP的X线主要表现为双肺局灶或弥漫性实变影(图3A)。典型的CT征象为多发性实变影,多分布于双下肺、胸膜下或支气管血管束周围,可单侧或双侧,伴或不伴支气管充气征(图3B)。其他征象:①结节/肿块型:大小不等,单发或多发,可呈实性、部分实性或磨玻璃样。部分结节或肿块边界不清且有毛刺;也可为边界清楚、直径约8mm的腺泡型结节或边界不清、直径更小、弥漫分布的微结节(图3C);②游走性改变(图3D-E);③小叶周围型:小叶间隔增厚,胸膜下可见边界不清的弓形或多边形实变;④线状和带状影:平行或垂直于胸膜的曲线带;⑤反晕征或环礁征(图3F);⑥进行性纤维化或蜂窝样改变、纵隔淋巴结肿大和胸腔积液等较少见。
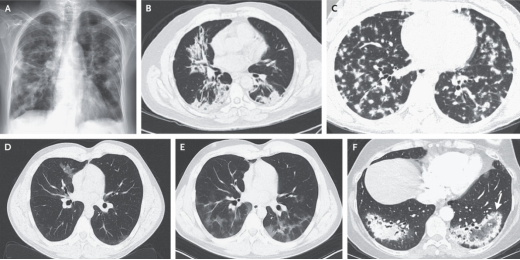
图3 COP的影像学表现
COP的影像学表现多样,其早期最常被误诊为感染性肺炎,因此,应对抗生素治疗无反应或效果差的“肺炎”提高警惕。结合临床背景并依据影像线索进行鉴别诊断后(表2),如拟诊为COP患者病情稳定,可考虑给予激素治疗并随访观察。若怀疑高风险疾病(如恶性肿瘤、血管炎等)或临床治疗效果与初步诊断相矛盾时,建议尽早完善组织病理检查,这也有助于我们进一步寻找继发因素。
表2 COP的影像学鉴别诊断

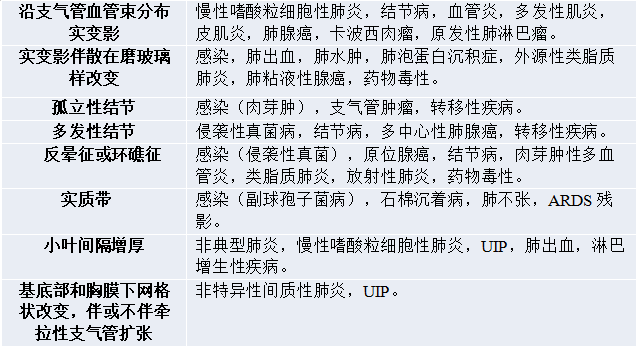
注:UIP普通型间质性肺炎;ARDS:急性呼吸窘迫综合征
治疗与预后
目前COP的一线治疗为口服糖皮质激素。一般以泼尼松0.5~1mg/kg/d起始,维持2~4周,如治疗反应佳,6~12个月内可逐渐减量至停用。对于少数病情严重或有呼吸衰竭征象的患者早期可给予大剂量甲泼尼龙(500~1000mg/d)冲击治疗。
通常COP患者在激素治疗24~72小时内临床症状会有所改善,3个月内影像学可见缓解,5年生存率>90%。在激素减量的过程中,部分病例(<25%)存在复发,但与预后无关。文献报道与复发相关的因素有:诊断延迟;治疗延迟(症状出现后2个月以上);低氧血症(PaO2<70mmHg);DLco下降(DLco%预计值<50%);牵拉性支气管扩张;胆汁淤积;肺泡腔内大量纤维蛋白沉积。绝大多数复发者对激素仍敏感,建议加量至20mg/d。
COP的辅助或替代药物包括:①大环内酯类抗生素(红霉素、克拉霉素):多为辅助用药,单独使用效果欠佳;②细胞毒性药物(环磷酰胺、硫唑嘌呤):疗效有限且副作用大,其中环磷酰胺治疗疗程最好不超过6个月;③其他:少数病例报道吗替麦考酚酯、环孢素、利妥昔单抗和免疫球蛋白等可成功治疗快速进展性或激素耐药性COP,其有效性和安全性值得进一步研究。
未来方向
1. 目前关于COP的经验总结主要来自于小型回顾性研究,未来可前瞻性建立专病队列,收集相关数据进一步明确其发病率、患病率、危险因素和临床发生发展规律等。
2. 鉴于COP和UIP的病理学差异,如Masson小体和成纤维细胞灶,进一步深入研究相关的细胞分子机制,可能有助于识别UIP 中持续进展或不可逆性纤维化的危险因素和关键靶点,并指导临床治疗。
3.在COP的治疗方面,糖皮质激素的最佳剂量和维持时间尚无统一的规范,免疫抑制剂的有效 性也仅见于病例报道,期待未来开展一系列临床试验进行探索。
来源南山呼吸 作者 董亮 曾荣
查看更多