查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





内镜下经口经食管隧道技术进行肿瘤切除:一项新的胃肠道外间质瘤的完整切除方法
复旦大学附属中山医院内镜中心周平红教授团队的一项研究发现,内镜下经口经食管隧道技术(ETER)是一项新的治疗技术,能够安全有效地用于可进行R0切除的胃肠外间质瘤(EGIST)患者,但是还需要大规模循证医学证据进行验证。
胃肠外间质瘤(EGIST)的治疗目前正面临挑战,传统的手术切除方法不仅是有创的,而且其发病率和死亡率均较高。
该研究收集了1年以内诊断为EGIST的患者进行ETER治疗。
结果显示,最终有8例患者诊断为EGIST,并进行了ETER治疗。治疗前肿瘤横轴和纵轴分别为2.8 ± 0.6厘米和2.3 ± 0.8厘米。平均手术时间为67 ± 4.4分钟。完整切除率和完全恢复率分别为100%和87.5%。组织病理学检查提示有六例被确认为EGIST,但有两例肿瘤不是EGIST,其中一例是神经鞘瘤,另一例是前肠囊肿。在手术过程中,有五例患者出现了肺炎,但都痊愈了没有遗留任何并发症。有一例患者进行了粘膜切开,并予以止血铗处成功处理。整个研究中没有出现严重不良事件及死亡。平均住院时间中位数为3天。平均随访时间为10.0 ± 2.1月,在此期间,没有一例患者出现影像学可以检测到的肿瘤复发。
内镜黏膜下剥离术与食管切除术治疗T1期食管鳞癌的疗效比较:一项真实世界研究
复旦大学附属中山医院内镜中心周平红教授团队的一项研究显示,在T1a和T1b的早期食管鳞状细胞癌(EESCC)患者中,内镜黏膜下剥离术(ESD)的围手术期不良事件更少,但生存率或复发/转移率与食管切除术组无差异。当然,仍需要有长期随访的前瞻性研究才能找到最佳的治疗方案。
食管切除术一直被认为是治疗EESCC的金标准,但其围术期仍伴随着较高的死亡率和并发症概率,且患者的短期和长期生活质量都有受损。相较而言, ESD是一种微创治疗EESCC的手术方式,应用并取得良好的临床结果已超过十年。EESCC患者的高淋巴结转移风险让大家更加关注ESD的治疗结果,但目前尚未有直接比较ESD与食管切除术在治疗EESCC方面的研究。
该研究为一项单中心病例对照研究纳入并分析了2011年10月1日至2016年9月30日期间在我院接受治疗的EESCC患者(T1a-m2/m3和T1b)。接受ESD者为实验组,接受食管切除术者为对照组。研究者采集并比较了两组患者的临床情况,肿瘤情况,手术参数,病理情况,不良事件和生存信息等内容。
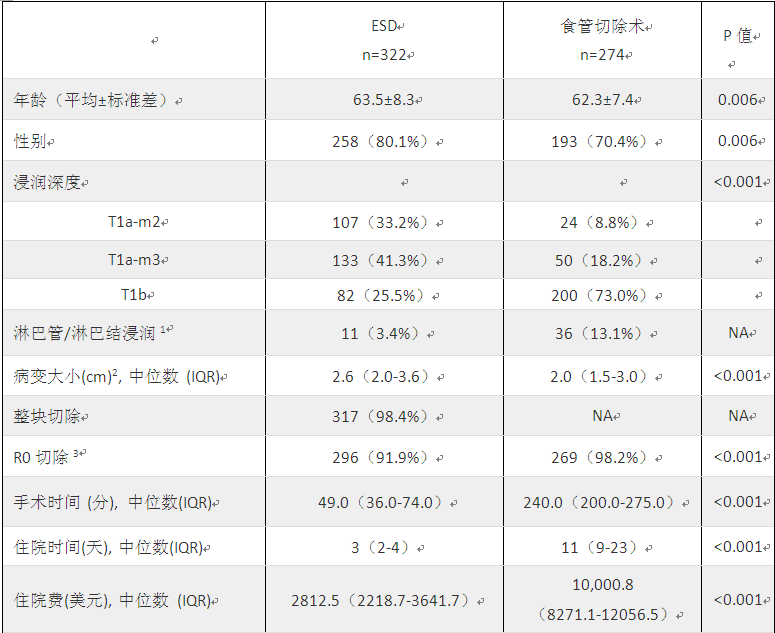
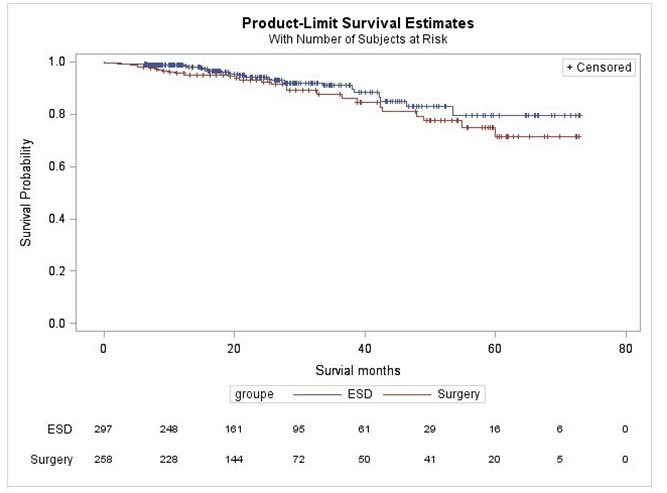
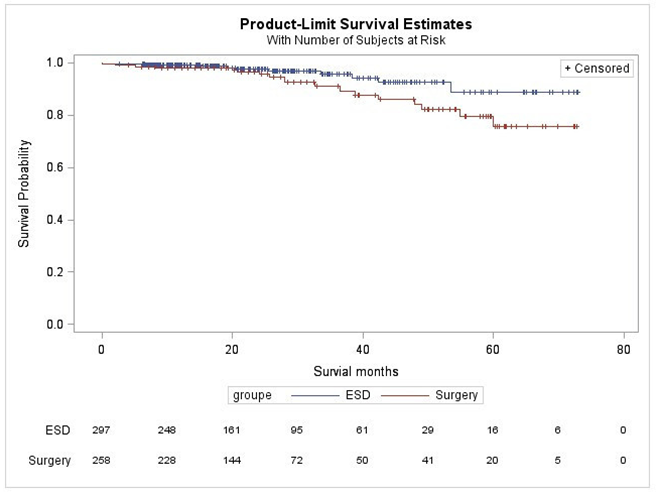
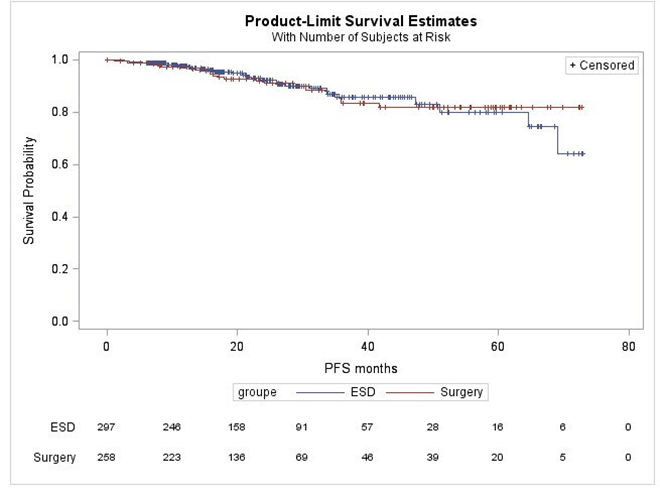
研究结果:ESD组纳入322例患者,食管切除术组纳入274例患者。其中,ESD组的患者年龄偏大(平均63.5岁比平均62.3岁,p<0.01),男性较多(80.1%比70.4%,p<0.01),T1a期的肿瘤患者更多(74.5%比27%,p<0.01),T1b期的患者更少(25.5%比73.0%,p<0.01),肿瘤病变更大(中位直径2.6cm比2.0cm,p<0.01),围术期死亡率更低(0.3%比1.5%,p= 0.19),非致命性的严重不良事件较少(15.5%比30.7%,p<0.01),特别是食管瘘的概率较少(0.3%比16.4%,p<0.01),肺部并发症少(0.3%比3.6%,p<0.01)。中位随访时间为21个月(随访时间为6-73个月),其后两组间的全因死亡率相似(3.4%比10.9%,p=0.21),但ESD组的疾病特异性死亡率较低(3.4%比7.4%,p=0.05),癌症复发/转移率相似(9.1%比7.4%,p=0.95)。
Cox回归分析显示肿瘤浸润深度是同全因死亡相关的唯一危险因素(T1-m3或更深与T1-m2相比,HR=3.54,p=0.04)。亚组分析提示在T1a-m2,T1a-m3或T1b患者中,ESD和食管切除术组之间在全因死亡率,疾病特异性死亡率或复发/转移率方面没有差异。研究者利用倾向评分匹配(PSM)在两组匹配了年龄,性别,其他肿瘤,浸润深度和辅助放疗这几个项目后,共找到了127对病例,其中ESD组与食管切除术组相比出现围术期严重不良事件的发生率较低(15.7%比29.9%,p=0.01),但生存或复发/转移的概率并无差异。
表1:患者临床资料及肿瘤情况
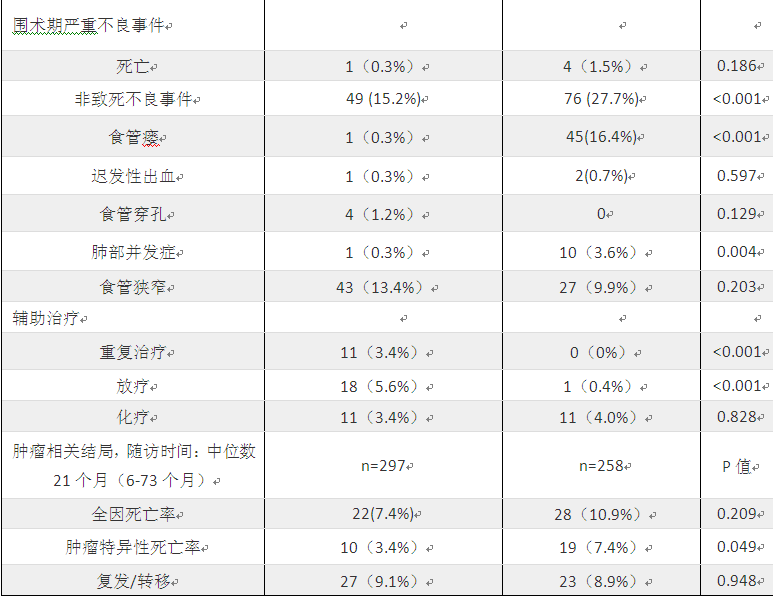
1、ESD标本的淋巴管侵犯;食管标本淋巴结转移。
2、病变大小:拉伸和非固定病理标本上最大直径的裸眼测量。
3、R0切除:水平和垂直边缘无癌和癌前病变组织(HGIN)。
内镜下黏膜剥离术治疗食管或胃切除术后食管癌的可行性和安全性初步研究分析
复旦大学附属中山医院内镜中心周平红教授团队的一项研究显示,对于有食管切除术或胃切除病史的早期食管鳞状细胞癌(ESCC)患者,ESD技术上是可行且是安全的。当然仍需要更多的随访资料进行进一步的分析,以研究其对这些患者群体的长期疗效。
有胃/食管切除病史的患者可能由于肿瘤复发或反流的原因导致罹患食管鳞状细胞癌(ESCC)的风险较高。部分患者可在随访期间通过胃镜检查发现早期ESCC。食管切除术被认为是食管鳞癌的金标准,然而,消化道的二次重建是非常困难的,这使得结肠代食管术往往成为唯一的方法,更糟的是,这种方法往往伴随着不良事件的高风险,导致生活质量和生存率较为低下。相关文献已证明ESD在符合适应症的早期ESCC中是有效的,但尚无针对这一特殊人群的分析研究。
在这项单中心回顾性研究中,研究者对在2012年1月1日至2016年12月31日期间在该中心接受ESD的早期ESCC患者(有胃/食管切除病史)进行了分析。
该研究纳入49例早期食管鳞癌患者(共53个病灶)(表1)。
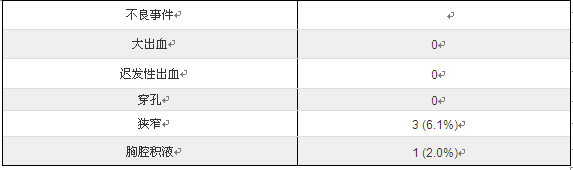
结果显示,大多数病例为男性(93.9%),44例有胃切除史,其余5例有食管切除史。在53个病灶中,32个(60.4%)病灶侵犯上皮或固有黏膜,9个(17.0%)病灶侵入黏膜肌层,两者均被视为早期ESCC的ESD指征。12个(22.6%)病灶侵入黏膜下层。有50例(94.3%)和42例(79.2%)获得整块切除和R0切除。4例(7.5%)有淋巴血管侵犯。所有未获得R0切除或存在黏膜下浸润或淋巴血管侵犯的患者均未接受第二次手术,其中部分接受了放疗。随访中没有发现致命的围术期不良事件。1例患者出现双侧胸腔积液,通过改善呼吸功能和抗生素治疗,未进行手术或引流。3名患者出现狭窄并经内镜扩张治疗得以缓解。
表1 患者临床资料及肿瘤情况
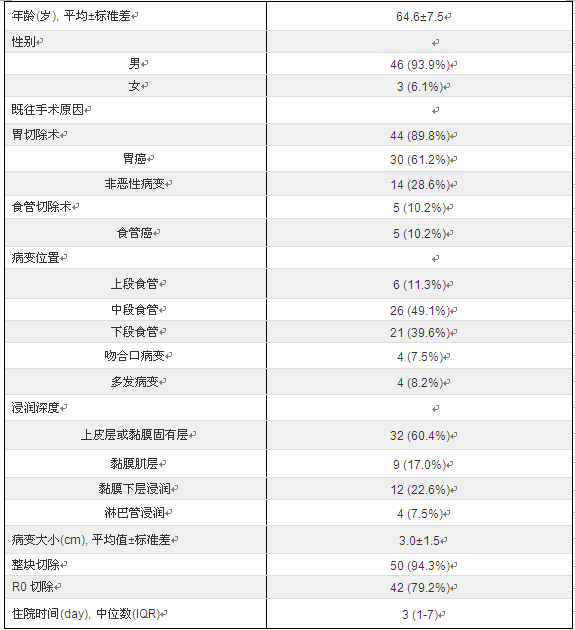 病变大小:拉伸和非固定病理标本病灶最大直径的测量
病变大小:拉伸和非固定病理标本病灶最大直径的测量
表2 不良事件统计
ESD治疗食管胃同时性多原发早期癌的临床分析
复旦大学附属中山医院内镜中心周平红教授团队的一项研究显示,内镜下同步治疗食管胃同时性病变的报道很少。还有很多问题需要进一步讨论,比如应该同时还是分阶段切除病灶;哪类病灶应首先切除;如果选择逐步切除,间隔时间应该是多久等等。但是,作为一种微创内镜手术,ESD仍是一种可用于治疗食道胃同时性多原发早期癌症的方法。
该研究回顾2008年1月至2016年12月本中心接受ESD治疗的12例早期食管胃癌患者的资料,研究者收集并分析了这些病人的病史,病变的大小,病理结果,切除完整性等信息。
结果显示,研究者收集的12名患者中,所有患者均诊断为食管胃同时性多原发早期癌。其中有9名男性病例。平均年龄为(67±10.6)岁。食管病灶平均大小为(2.2±1.1)cm,其中3例位于上段食管,中段食管8例,下段食管1例。胃部病灶平均大小为(2.1±1.3)cm,胃窦5例,胃角2例,贲门5例。 10例患者同时行ESD切除病灶,剩余2例分期切除病灶。完全切除率为100%(10/10)。术后病理结果显示:食管癌前病变伴胃癌前病变4例,食管癌前病变伴早期胃癌2例,早期食管癌伴胃癌前病变3例,早期食管癌伴早期胃癌3例。12例24个病灶均符合内镜下切除适应证,其根治性切除率为100%。术后2例患者出现食管狭窄,予扩张后好转。中位随访时间为30(8-115)个月,共有9例患者存活,3例患者死亡,但死因均与疾病治疗无关。
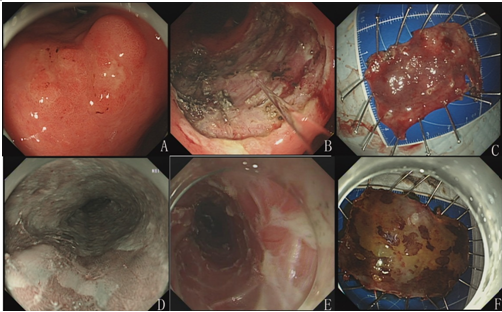
图 ESD治疗食管胃同时性病变。A\B\C:胃病变的处理;D\E\F:食管病变的处理
内镜黏膜下剥离术治疗符合相对适应证(日本标准)老年早期食管鳞癌疗效分析:一项中国回顾性研究
复旦大学附属中山医院内镜中心周平红教授团队的一项研究显示,ESD 治疗符合相对适应证的老年早期食管鳞癌病人,不进行追加治疗可能也可以获得与符合绝对适应证组相似的长期生存。因此,对于这部分病人,定期随访是可接受的。
日本食管学会(JES)发布的食管癌诊治指南指出,早期食管癌ESD治疗相对适应证为肿瘤侵犯至黏膜肌层(M3)或黏膜下<200 μm(SM1),由于相对适应证病人发生淋巴结转移风险较高,ESD治疗后还应结合临床及病理学资料决定是否追加外科手术或放化疗。然而,我国许多ESD 相对适应证的早期食管癌老年(≥60 岁)病人由于身体状况较差,或经济条件不允许,放弃了内镜切除后的外科手术或放化疗等追加治疗。该研究回顾性分析2008年1月至2013年12月在我中心行ESD治疗的老年早期食管鳞癌病人的临床资料158例,观察并分析术后长期生存情况。
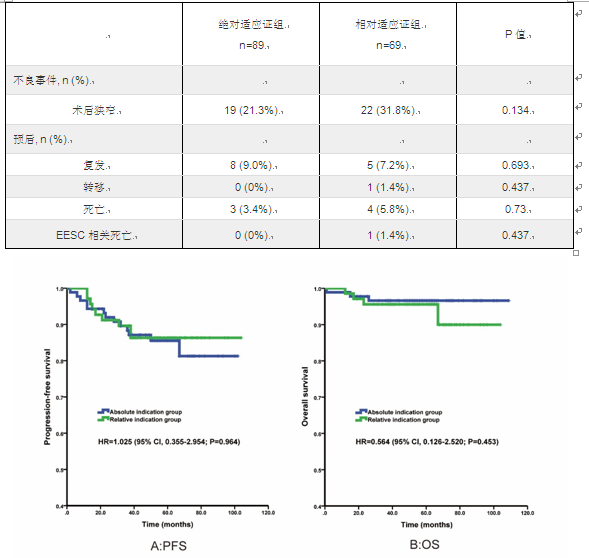
结果显示,89例患者符合绝对适应证(AI组),69例符合相对适应证(RI组),两组间基线情况相似。在随访期内(中位随访时间56个月(1-108月))内,RI组及AI组间短期并发症发生率(4.3%比1.1%, p=0.319)及术后狭窄发生率(31.8% 比21.3%, p=0.134)无明显差异。5年无复发率(85.8%比87.2%, p=0.561)、无转移率(100%比98.6%, p=0.437)及无病生存率(98.9%比98.5%, p=0.264)在AI组及RI组也相似。
表1 绝对适应证组及相对适应证组不良事件及预后转归
张丹枫 译
查看更多