查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





肺癌新型治疗方案的进展日新月异,但仍有大约三分之一的晚期非小细胞肺癌患者会发生骨转移,超过一半的骨转移患者会发生骨相关事件(SREs)。近年来也开展了多项抗肿瘤治疗联合骨靶向药物(BTA)的探索,以期在预防SRE发生的基础上,为患者带来更多获益。
正在召开的2021年第22届世界肺癌大会(WCLC)上公布了一项研究[1],通过分析进展期非小细胞肺癌(aNSCLC)合并骨转移(BM)患者使用BTA联合免疫检查点抑制剂(ICIs)的治疗结果,以探索联合治疗的最佳获益人群。

王哲海 教授
主任医师
中国肿瘤临床学会非小细胞肺癌专家委员会副主任委员
中国肿瘤临床学会抗肿瘤药物安全专家委员会副主任委员
中国医学促进会胸部肿瘤分会副主任委员
中国抗癌协会化疗专业委员会常委
中国抗癌协会老年专业委员会肺癌分会常委
中国医师协会肿瘤医师协会常委
中国医师内科培训专家委员会常委
中国抗癌协会肿瘤药物临床研究专业委员会常委
山东抗癌协会常务理事
山东省抗癌协会肺癌分会主任委员
山东省癌症中心副主任
山东省合理用药专家委员会副主任委员、
抗肿瘤药物专业组组长
山东省肿瘤医院药物临床试验机构主任
该研究回顾性收集了单中心接受ICI治疗的aNSCLC合并BM患者的数据(2013年3月至2020年6月)。BTA治疗定义为在ICI治疗前60天或治疗后30天内给予地舒单抗(DN)或唑来膦酸(ZA)治疗。高骨肿瘤负荷(HBTB)定义为患者存在≥3处骨转移(BM)。用Kaplan-Meier法预估中位OS(mOS)和中位无进展生存期(mPFS),用Cox比例风险回归模型进行多变量分析。
1. 在纳入的151例患者中,有68例(45%)接受了BTA治疗。在BTA治疗的患者中,中位年龄为68岁(范围30~87岁),男性占59%,85%的患者组织学分类为非鳞癌;ECOG评分≥2 的患者占18%;60%的患者PD-L1表达≥1%;有27例(40%)在一线治疗时接受了ICI治疗,41例(60%)接受ICI作为二线/后线治疗;存在HBTB的患者为45例(66%),有31例患者(46%)因骨转移同时接受了放疗(表1)。
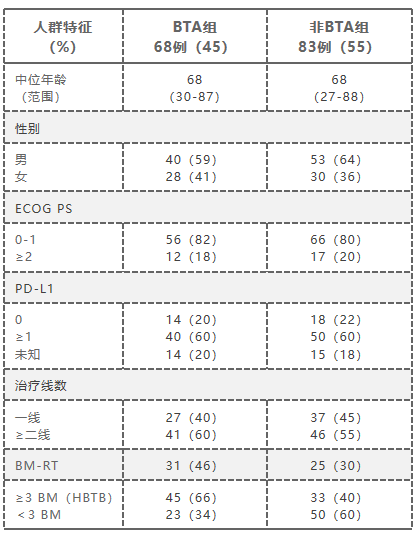
表1. 患者基线信息
2. ICI治疗伴多发骨转移NSCLC患者,联合BTA显著改善了mOS和mPFS
在中位随访34个月时,BTA并未显著延长总人群的mOS及mPFS。但是,对于存在HBTB的78例患者中:16例(21%)接受了DN治疗,29例(37%)接受了ZA治疗,33例(42%)未接受任何BTA治疗。在HBTB患者中,BTA显著改善了mOS [7.8个月(95% CI 3.4~12.2) vs. 3.5个月(95% CI 2.9~4.0),P=0.01],和mPFS [2.6个月(95% CI 2.1~3.1) vs. 1.8个月(95% CI 1.5~2.1),P=0.002]。在多变量分析中,通过校正患者PS评分、转移部位数量、治疗线数及骨转移放疗等因素后,证实了BTA治疗与患者OS [HR 0.59 (95% CI 0.35~0.90),P=0.02]和PFS [HR 0.53 (95% CI 0.32~0.83),P=0.006]的获益有相关性(图1)。
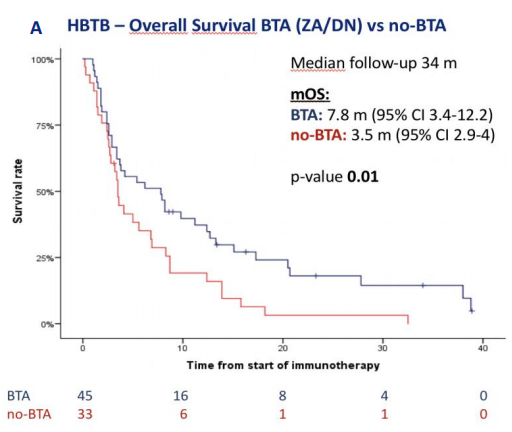
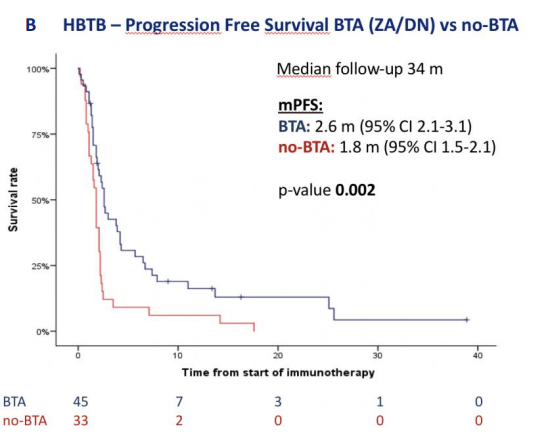
图1. 骨转移高负荷组接受BTA治疗患者的OS(A)和PFS(B)K-M曲线
3. ICI治疗伴多发骨转移NSCLC患者,联合地舒单抗显著改善了mOS和mPFS,唑来膦酸组未获益
在HBTB 患者中,ZA并没有延长mOS [3.8个月(95% CI 0.3~7.3) vs.3.5个月(95% CI 2.9~4.0),P=0.27],而接受DN的患者与未接受任何BTA治疗的患者相比,显著改善了mPFS [2.6个月(95% CI 0.6~4.6) vs. 1.8个月(95% CI 1.5~2.1),P=0.01]和mOS [15.1个月(95% CI 0.1~33.1) vs. 3.5个月(95% CI 2.9~4.0),P=0.002](图2)。
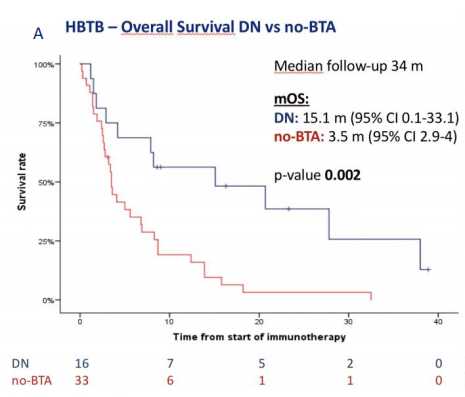
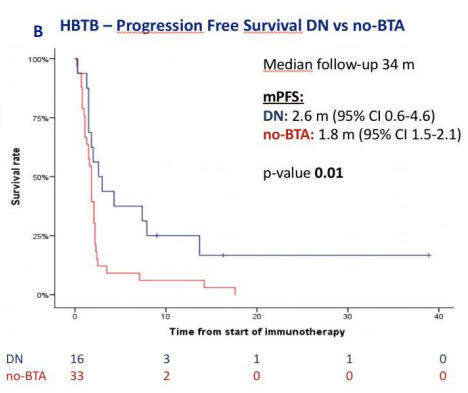
图2. 骨转移高负荷组接受地舒单抗治疗患者的OS(A)和PFS(B)K-M曲线
虽然BTA联合ICIs治疗aNSCLC合并BM的患者对其生存期无明显影响,但在使用ICIs的HBTB亚组,BTA显著延长了OS和PFS,提示HBTB患者使用BTA联合ICIs治疗可显著获益。同时相较于唑来膦酸,地舒单抗治疗可为这部分患者提供更好的生存获益,这也进一步证实了ICIs和RANKL抑制剂之间可能存在一定的协同作用。
肺癌是目前全球最常见的恶性肿瘤之一,而肺癌在我国的发病率也长期居于首位[2]。NSCLC在肺癌中占比约85%,其中,30%~40%的晚期患者会出现骨转移,这些患者多经历了剧烈疼痛、骨折、脊髓压迫甚至瘫痪等症状,严重影响了生活质量[3]。近年来,随着诊疗技术的发展,靶向治疗、免疫治疗的出现拓宽了诊疗思路,进展期NSCLC患者生存时间有显著延长。在生存期延长的同时需要更关注患者生活质量,特别是在BTA进入临床后,对于减少骨相关事件均显现出重要的作用。
临床前数据已证实肿瘤微环境和局部淋巴结均可表达RANK/RANKL[4]。动物实验也显示,在不同小鼠模型中,使用PD-1+RANKL联合治疗组,肺转移负荷最小,肿瘤增长最慢;同时证明,在PD-1+CTLA-4的基础上进一步联合α-RANKL可增加肿瘤浸润CD4+/CD8+T细胞比例,从而产生更多的IFN-ɣ和TNF[5]。地舒单抗是RANKL的全人化单克隆抗体,可特异性结合人RANKL,抑制破骨细胞活性,减少骨吸收,从而减少肿瘤引起的骨破坏和SRE。目前已报道的地舒单抗联合免疫治疗的数据多为回顾性观察研究结果,尚缺乏大样本前瞻性临床数据和更进一步的作用机制等相关数据的支持。一项纳入166例同时接受地舒单抗和免疫治疗的NSCLC患者研究显示,两者同时使用的时间越长,患者OS获益越多[5]。在安全性方面,目前观察到联合治疗的不良反应包括疲乏、反复呼吸道感染、肝毒性和肺炎等,但均为1~2级不良反应,对患者生活影响较小,且总体可控。
本项回顾性研究比较了接受ICIs治疗的aNSCLC合并BM患者,在使用地舒单抗及唑来膦酸后mOS、mPFS之间的差异。亚组分析结果显示,与唑来膦酸相比,地舒单抗可显著延长高骨转移负荷NSCLC患者的mOS和mPFS,提示这类患者或可成为地舒单抗+ICIs联合治疗方案的最佳人群,也期待这一联合治疗模式成为NSCLC合并BM患者的治疗新希望。
参考文献(向下滑动查看更多):
[1] S. Manglaviti, et,al. #637 Bone-targeted agents improve survival in advanced non-small-cell-lung cancer patients with high bone tumor burden treated with immune-checkpoint inhibitors. 2021 World Conference on Lung Cancer. September 8-14, 2021.
[2] 蒋晓岚,等.非小细胞肺癌骨转移患者预后影响因素分析[J].山东医药,2016,56(35):88-90.
[3] 王海玉,等.非小细胞肺癌发生骨转移的危险因素分析[J].现代肿瘤医学, 2021,29(13): 2274-2278.
[4] Ahern E, et al. Nat Rev Clin Oncol. 2018 Nov;15(11):676-693.
[5] Liede A, et al. Oncoimmunology. 2018 Sep 5;7(12):e1480301.
牛晓辉教授:精准骨靶向药物——RANKL抑制剂地舒单抗的研发历程
查看更多