查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:江南大学附属医院 浦红
患者基本情况
年龄:54岁,已婚女性,汉族,江苏省无锡市人。
2014-03-15入院。
病史
主诉:发现左附件囊肿五天。
现病史:患者2014-03-10在外院体检行B超检查,示“左附件约34*18mm低回声团”,余无明显不适,于2014-03-11我院复查B超示:左附件囊肿,约28*20mm,查肿瘤标记物正常,患者要求手术,收治入院。病程中患者无恶心、呕吐,无畏寒发热,无异常阴道出血及排液,无体重减轻,饮食睡眠好,大小便正常。
既往史:既往体健,否认呼吸系统疾病,否认高血压、糖尿病及免疫系统疾病,否认血吸虫,伤寒等传染病接触史。预防接种史不详。既往行阑尾切除术,否认外伤及输血史。无药物过敏史。
个人史:出生、生长于无锡,否认疫水疫区接触史,否认吸烟史、饮酒史。
婚育史: 已婚,1-0-3-1,上环20年余。
月经史: 14 5/30,量中,已绝经三月。
家族史:否认家族性遗传病史,否认家族成员肿瘤病史。
手术经过(2014-03-20)。
术前诊断:左附件囊肿。
探查见:少量淡血性腹水,子宫前位,正常大小,左输卵管壶腹部见增粗,约3*1cm,左卵巢稍增大。右侧附件外观正常,左后侧盆壁见一直径约2*3cm菜花样肿瘤,盆腔淋巴结未见明显肿大,肝胆胃未见明显异常。
腹腔镜下左附件+盆腔肿瘤切除术
快速病理提示左侧附件低分化癌。
中转开腹卵巢癌肿瘤细胞减量术(全子宫+右附件+大网膜+盆腔淋巴结清扫+腹主动脉旁淋巴结活检术),术后无肉眼残留。
术中诊断:左输卵管癌。
病理检查
(左卵巢、左输卵管及盆腔)低分化浆液性腺癌。 脉管、神经未见明显侵犯。 右卵巢滤泡囊肿,右输卵管未见特殊。
增生性子宫内膜,部分呈囊性扩张。
慢性宫颈炎伴潴留囊肿形成。
阴道壁及左右宫旁未见癌。
总数(0/22)(淋巴结转移数/淋巴结数) 左髂外 +腹股沟深淋巴结(0/2);右髂外+腹股沟深淋巴结(0/4);左髂总淋巴结(0/1);右髂总淋巴结(0/1);左髂内+闭孔淋巴结(0/5);右髂内+闭孔淋巴结(0/9)。 送检大网膜组织未见癌。
腹水见癌细胞。

免疫组化:ER(+),PR(少量+),AE1/AE3(+),EMA(+), CAM5.2(+),P16(+),CK7(+),Vimentin(-), CK20(-),P63(-),CD10(-),CD15(-),Ki-67(+,约 80%);。
ERCC1 mRNA表达:低ERCC1基因mRNA表达水平与铂类药物疗效呈负相关。
TUBB3 mRNA表达:低TUBB3基因mRNA表达水平与紫杉醇类、多西紫杉醇类、长春碱类药物疗效呈负相关。
术后诊断:左输卵管高级别浆液性腺癌IIC期。
治疗过程
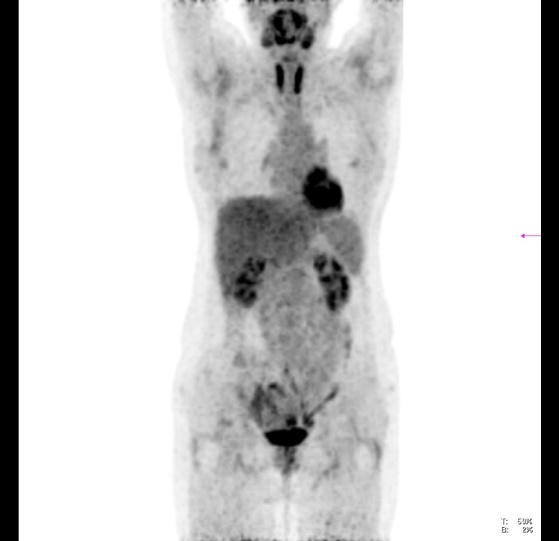
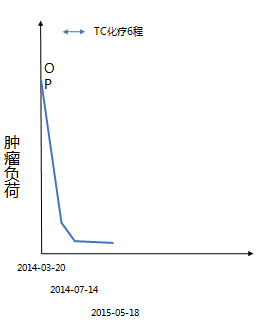
PET/CT:回盲部内侧旁见一结节,FDG代谢增高,对照前次为新发病灶,考虑转移性病变不能排除。
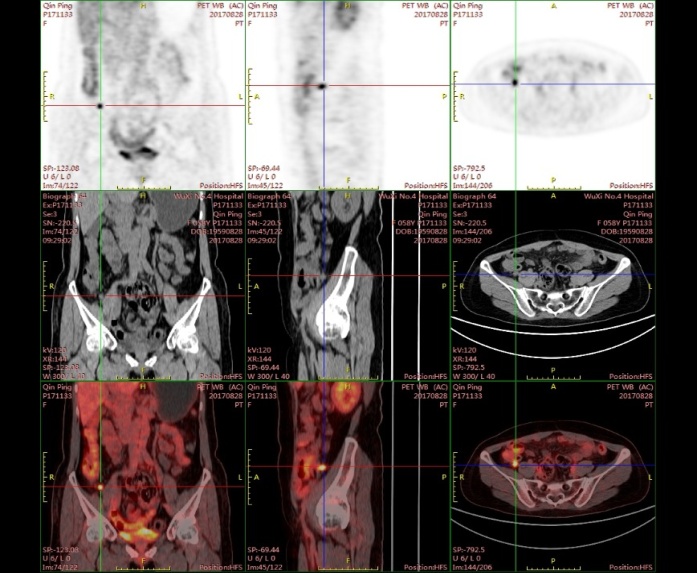

PET/CT:回盲部内侧旁见一结节,FDG代谢增高,对照前次为新发病灶,考虑转移性病变不能排除。
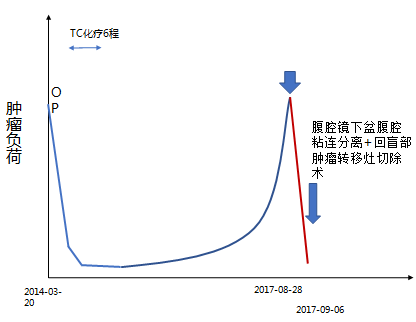
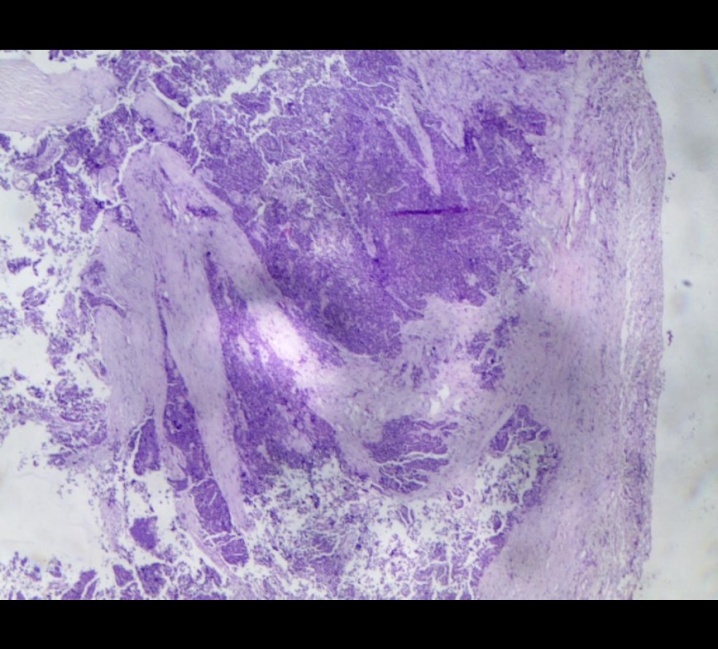
二次术后病理
(回盲部结节)低分化癌。(回盲部结节切缘)未见癌。
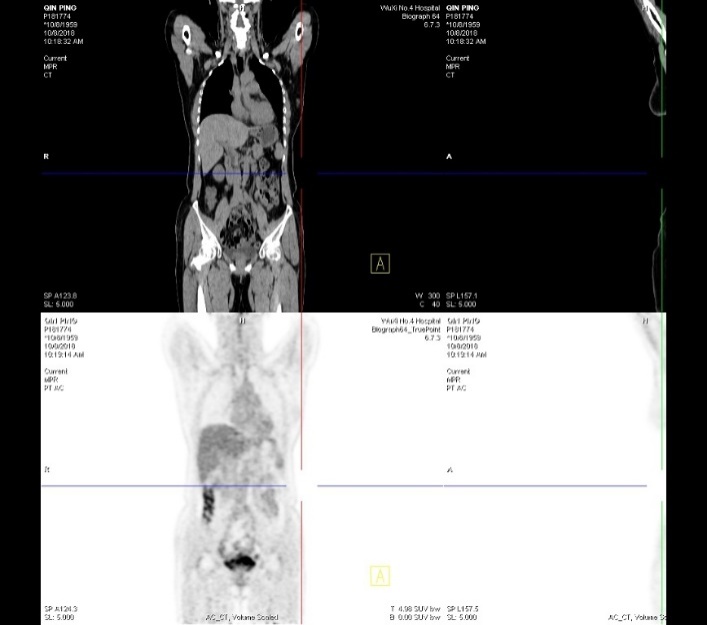
PET/CT:回盲部内侧旁见一结节,FDG代谢增高,对照前次为新发病灶,考虑转移性病变不能排除。
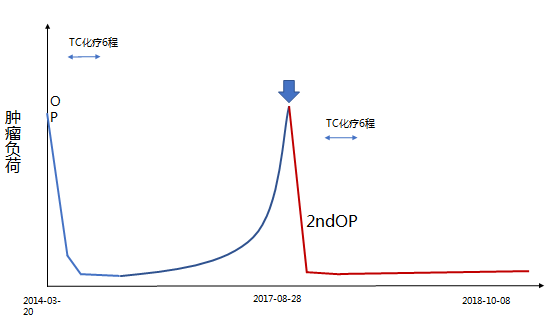
BRCA1/2突变阴性。
2019-01-08口服“奥拉帕利 300mg bid”至今
目前疾病无进展。
不良反应:乏力、血红蛋白轻微降低。
分析和总结
如何获取最佳的临床收益?
基于循证的规范化治疗(NCCN)


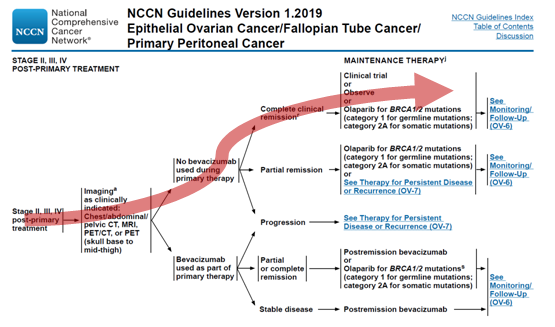
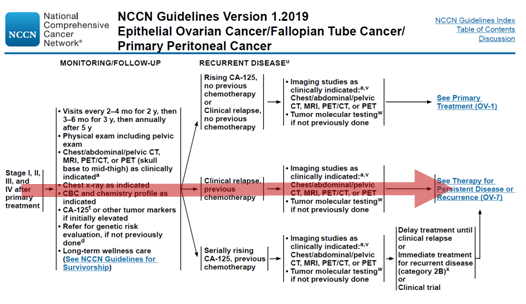

如何获取最佳的临床收益?
1.基于循证的规范化治疗(NCCN)
2.积极采用靶向药物(Olaparib)



【药品名称】
通用名: 奥拉帕利片
商品名: 利普卓®/LYNPARZA®
【适应症】
本品适用于铂敏感的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者在含铂化疗达到完全缓解或部分缓解后的维持治疗。
【用法用量】
本品应在有抗肿瘤药物使用经验的医生的指导下使用。
推荐剂量: 本品有150 mg和100 mg规格。推荐剂量为300 mg(2片150 mg片剂),每日2次,相当于每日总剂量为600 mg。100 mg片剂用于剂量减少时使用。患者应在含铂化疗结束后的8周内开始本品治疗,持续治疗直至疾病进展或发生不可接受的毒性反应。
详细剂量调整方案请参阅产品说明书。
【禁忌症】
对药物活性成分或任何辅料成份过敏者禁用。治疗期间和末次给药后1个月内停止哺乳。
【注意事项】
血液学毒性。
在接受本品治疗的患者中报告了血液学毒性,包括轻度或中度(CTCAE 1级或2级)贫血、中性粒细胞减少症、血小板减少症和淋巴细胞减少症的临床诊断和/或实验室检查结果。既往抗肿瘤治疗引起的血液学毒性未恢复之前(血红蛋白、血小板和中性粒细胞水平应恢复至 ≤ CTCAE 1级),患者不应开始本品治疗。在治疗最初的12个月内,推荐在基线进行全血细胞检测,随后每月监测一次,之后定期监测治疗期间出现的具有临床意义的参数变化。
如果患者出现重度或输血依赖性的血液学毒性,应中断治疗,并且应进行相关的血液学检测。如果本品给药中断4周后血液指标仍存在临床异常,则推荐骨髓分析和/或血细胞遗传学分析。
骨髓增生异常综合征/急性髓系白血病。
在临床研究(包括长期生存随访)中,接受本品单药治疗的患者中骨髓增生异常综合征/急性髓系白血病(MDS/AML)的发生率<1.5%。大多数事件的结局为死亡。在发生MDS/AML的患者中,奥拉帕利治疗持续时间为<6个月至>2年不等,更长暴露时间的数据有限。所有患者均存在导致MDS/AML的潜在因素,且既往均接受过铂类化疗。部分患者还接受过其它DNA损伤药物的治疗以及放疗。其中部分患者既往有肿瘤或骨髓发育不良的病史。如果奥拉帕利片治疗期间确诊患MDS和/或AML,建议应停止奥拉帕利片治疗,并对患者进行适当治疗。
单纯强调BRCA1/2检测会遗漏可能从PARP抑制剂获益的患者,而HRD是PARP抑制剂潜在获益人群的相对可靠生物标志物。“铂敏感”指征在一定程度上避免了BRCAm和HRD检测的不足,在复发卵巢癌患者中是目前较为可行的识别PARP抑制剂获益人群的方法。
如何获取最佳的临床收益?
1.基于循证的规范化治疗(NCCN)。
2.积极采用靶向药物(Olaparib)。
3.重视二级预防(cost-benefit,insurance)。
查看更多