查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





刘义思, 陈新月
首都医科大学附属北京佑安医院肝病中心一科
目前全球仍约有2.57亿慢性HBV感染者,如不进行治疗,会有20%甚至更多的慢性感染者发展为终末期慢性肝病,如肝硬化或肝细胞癌(HCC)[1]。抗病毒治疗是慢性乙型肝炎(CHB)患者最重要的治疗,通过抗病毒治疗可以抑制HBV的复制,减轻肝细胞炎症及纤维组织增生,以减少肝衰竭、肝硬化失代偿以及HCC的发生[2]。然而当下还没有一种药物可以完全清除感染肝细胞中的共价闭合环状DNA(cccDNA),这也是当前的抗病毒药物不能治愈CHB的主要原因[3-4]。随着现代医药水平的进步以及对HBV复制周期的深入了解,不同靶点的新型药物正处于研发和临床试验阶段,这些药物对于治疗CHB有着重大的意义。
目前治疗CHB的新药大致分为两类[3]。第一类主要针对HBV的生命周期:包括阻止HBV进入细胞、直接靶向cccDNA、靶向HBV基因表达、抑制核衣壳组装和HBsAg释放等。第二类主要针对宿主的免疫系统:包括固有免疫和适应性免疫。由于针对不同靶点的新药种类众多,在此仅讨论临床试验数据较详尽的代表性药物(图1)。
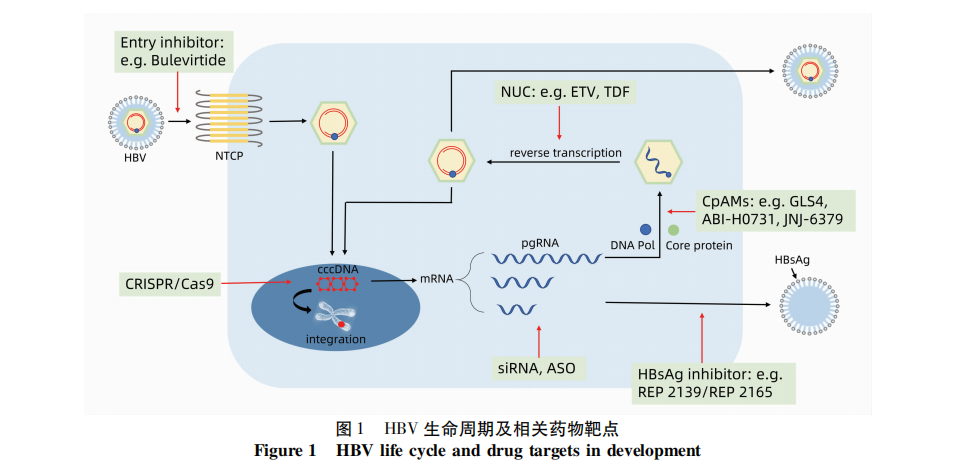
1 进入抑制剂(Entry inhibitor)
北京生命科学研究所李文辉团队[5]于2012年在世界上首次发现钠离子-牛磺胆酸共转运蛋白(sodium taurocholate contransporting polypeptide,NTCP)是HBV进入人体肝细胞的特异性受体。NTCP是一个多重跨膜的蛋白分子,HBV通过L-HBsAg 的前S1区与肝细胞表面的NTCP结合,介导HBV进入细胞[6]。这一发现不仅大大促进了HBV感染相关的研究,同时为HBV新药研发提供了新靶标。
基于Myrcludex B的使用,德国的海德堡大学医院Stephan Urban团队[7]提出了HBsAg阻断策略。Myrcludex B 是L-HBsAg的前S1结构域内47个氨基酸衍生的肉豆蔻酰化脂肽,通过竞争性与NTCP受体结合,进而抑制HBV进入肝细胞[8]。而Hepcludex B(Bulevirtide)则是由德国的MYR GmbH公司与俄罗斯的Hepatera Ltd公司合作研制的皮下注射型Myrcludex B。早些年作为治疗丁型肝炎的药物,Bulevirtide的临床试验进展较快,已于2020年在欧洲上市,批准剂量为2 mg/d[9]。而作为治疗乙型肝炎的药物,目前尚处于临床试验Ⅱ期阶段。研究结果表明,对于HBeAg阴性的CHB患者,2 mg的Hepcludex B和聚乙二醇干扰素(PEG-IFN)联用体现出显著的协同作用:治疗48周结束时,46.7%(7/15)的患者HBsAg下降>1 log10,有20%(3/15)的患者出现HBsAg的丢失[10]。Bulevirtide的安全性与耐受性均良好,最常见的不良反应是总胆盐的升高和注射部位的反应,但停止治疗后均可逆转[9-11]。从现有的实验结果来看,Bulevirtide单药治疗下降HBsAg效果并不明显,而联合PEG-IFN治疗可提高降低HBsAg的能力。不过目前该药物对于HBV DNA影响的试验结果较少,以后与PEG-IFN或核苷类似物(NUC)等抑制病毒复制的药物联用具有良好的临床应用前景。
2 靶向cccDNA
CRISPR/Cas9在2013年被发现可高效的编辑基因,成为继ZFN、TALEN技术之后出现的第三代基因编辑工具[12-14]。作为HBV复制的模板,很少有药物可以直接作用于cccDNA,这也是CHB难以治愈的主要原因。核酸内切酶介导的cccDNA突变是目前唯一在实验中建立的可以使cccDNA永久失活的方法[15]。临床前实验[16-19]表明,CRISPR/Cas9可以导致cccDNA的功能突变和缺失,从而有效抑制HBV的复制和降低HBsAg的表达。虽然CRISPR/Cas9仍处于临床前实验阶段,但目前的研究已经证实其在治疗HBV感染方面具有很大的潜力,不仅仅是临床治愈,更有望彻底治愈乙型肝炎。今后的研究需要克服CRISPR/Cas9技术可能存在药物脱靶效应、HBV DNA双链断裂损伤后的修复以及对宿主细胞基因组的影响等潜在问题。
3 靶向病毒mRNA
目前靶向病毒mRNA进展较快的策略主要是RNA干扰(RNA interference,RNAi)和反义寡核苷酸(antisense oligonucleotides,ASO)。
3.1 小干扰RNA(small interfering RNA,siRNA)
siRNA通常为19~25 bp短双链RNA,主要参与RNAi[20],通过靶向与HBV转录的mRNA碱基互补结合并对其进行降解来阻止基因翻译[21]。
首个进入临床研究的siRNA药物是美国Arrowhead公司研发的ARC-520。早期该药物在小样本试验中表现出良好降低HBsAg的能力,并且对HBeAg阳性的患者更有效[22]。但因该药物在灵长类动物黑猩猩试验造成了死亡,研发已于2016年被叫停。JNJ-3989(ARO-HBV)是Arrowhead公司研发的第二代siRNA药物。临床试验[23]的研究结果显示,对于40例HBeAg阳性CHB患者不同剂量的JNJ-3989皮下注射(每月1次,共3次),各剂量的JNJ-3989均可有效降低HBsAg,无明显剂量依赖。每月接受300 mg的NUC经治患者HBsAg最大减少2.5 log10,而初治患者HBsAg最大减少2.3 log10。有97%的患者治疗约90天时HBsAg降低>1 log10。其他病毒学指标如HBV DNA、RNA、HBeAg较基线水平都有不同程度的下降。但是后续的观察发现,患者在停用JNJ-3989后HBsAg基本未继续下降,且有回升趋势[24]。治疗期间并未出现严重的不良反应。JNJ-3989目前已经进入Ⅱb期临床试验阶段。
VIR-2218(ALN-HBV02)是由美国Alnylam和Vir Biotech公司联合开发的siRNA类药物。关于VIR-2218安全性和抗病毒活性的研究[25]显示,2次皮下注射VIR-2218治疗后,大多数患者在第12周达到最大HBsAg下降幅度,平均比基线HBsAg水平下降1.5 log10。并且无受试者因不良事件而终止治疗,大多不良反应为轻度,未观察到ALT的显著升高。在2021年欧洲肝病学会(EASL)年会上发表的另一项VIR-2218联合PEG-IFN治疗的部分数据[25]表明,治疗24周时联合治疗组HBsAg下降幅度大于VIR-2188单药治疗组(分别是1.8和1 log10)。不过与JNJ-3989类似,在VIR-2218停药后HBsAg也有回升的趋势。目前VIR-2218的Ⅱ期研究正在积极寻找多种方案的联合治疗。
其他siRNA药物,如罗氏(Roche)公司的RG6346(DCR-HBVS)和美国Arbutus公司的AB-729(GalNAc-RNAi)也均处于Ⅱ期试验阶段(表1)。总体来说siRNA的HBsAg下降效果较好,但是单一治疗下降幅度有限,且停药后可导致HBsAg的反弹。不过与PEG-IFN的联合用药效果更佳显著,未来多药物联合的抗病毒治疗方案前景令人期待。
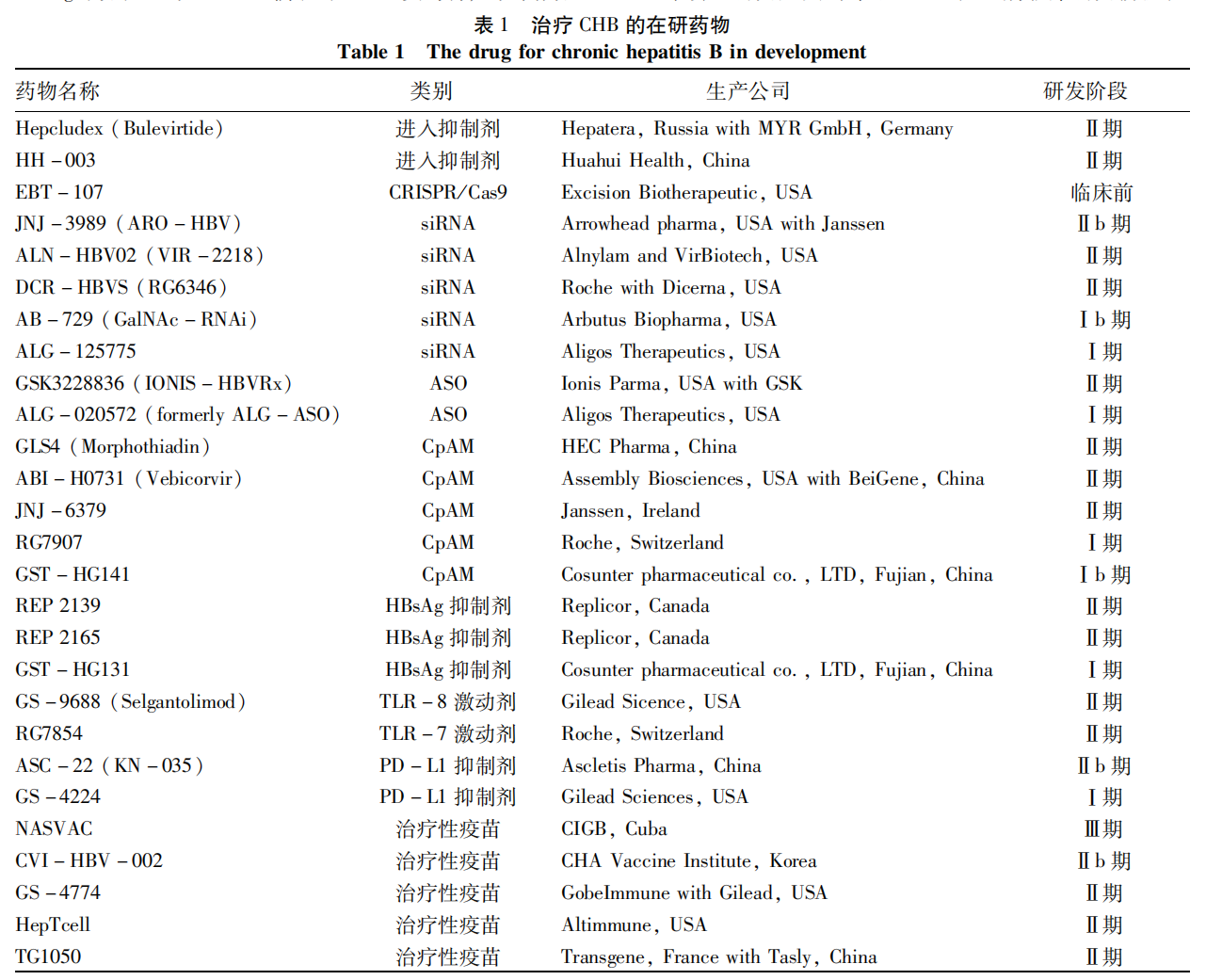
3.2 反义寡核苷酸(ASO)
ASO是长度为8~50 bp人工合成的小单链核酸,它们与靶mRNA碱基互补配对结合后,通过核糖核酸酶H依赖的切割机制降解病毒的mRNA[26]。
GSK3228836(IONIS-HBVRx)由美国Ionis公司和葛兰素史克公司研发,该药是无配体的ASO类药物。GSK3228836的Ⅱ期临床试验给予患者6次共1800 mg的IONIS-HBVRx皮下注射,治疗29天时NUC经治患者HBsAg较基线相比平均下降2.5 log10,初治患者HBsAg较基线相比平均下降1.6 log10[27]。最常见的不良事件为注射部位的反应,发生率为29.4%(5/17)。然而治疗后HBsAg低于检测下限的患者均有ALT骤升,其中1例患者ALT最高至781 U/L,其余患者多为(1.7~15)×ULN。ALT骤升不伴随其他症状,并且可以自行下降,研究者考虑这与HBsAg下降有关。目前该药物处于Ⅱ期阶段。
RO-7062931是由罗氏公司研制的一类与N-乙酰半乳糖胺(GalNAc)偶联的ASO类药物,配体可以增强药物的靶向性,从而降低所需药物的剂量和频率[28-29]。该药物早期研究[30]结果显示,在NUC经治的患者中,仅有1例患者HBsAg下降达1 log10,并且停止治疗后约12周,HBsAg水平逐渐恢复到基线水平。随后罗氏公司认为RO-7062931不太可能成为一线的抗乙型肝炎药物而停止了该药物的研发。
作为GalNAc偶联的药物,罗氏的RO-7062931降低HBsAg的效果远不如GalNAc偶联的siRNA类药物,比如同为罗氏的RG6346和Arrowhead的JNJ-3989。有研究者认为这可能与两类药物机制有关。另外,无配体的ASO药物GSK3228836可使HBsAg下降幅度更大,这或是更高剂量暴露引起(4周内的总剂量达到了1800 mg)。如何在提高靶向性和安全性的同时增强药效,将成为ASO类药物将来面临的重要难题。
4 核心蛋白变构调节剂(CpAM)
核心蛋白由pgRNA翻译而来, 240个核心蛋白相互结合形成一个完整的核衣壳[31-33]。CpAM是以核心蛋白为靶点的一类抗病毒药物,其通过改变核心蛋白的构象来干扰核衣壳的装配,进而影响病毒分子组装和逆转录等过程,最终抑制HBV复制。根据机制可将CpAM分为两类,Ⅰ类CpAM诱导异常核衣壳或非核衣壳核心蛋白的组装,形成异常组装的核衣壳,随后在肝细胞中降解;Ⅱ类CpAM则形成不能包裹pgRNA的“正常形状”核衣壳,即空衣壳。
GLS4(甲磺酸莫非赛定)是由我国东阳光药业开发的一款Ⅰ类CpAM药物。该药Ⅰb期的临床试验比较了不同剂量GLS4和恩替卡韦(ETV)单药治疗的效果,治疗结束时各组HBV DNA、pgRNA下降水平无明显差异[34]。随后2020年EASL年会上研究人员公布了GLS4的Ⅱb期临床研究阶段性[35]。两组CHB患者分别接受了12周的GSL4联合ETV或ETV单药治疗。半年内未接受过抗病毒治疗者中,联合治疗组HBV DNA和pgRNA较基线水平下降分别为5.02 log10和1.59 log10,均高于ETV单药治疗组的3.84 log10和0.37 log10。而在ETV经治患者中,联合治疗组pgRNA下降水平也显著高于ETV单药治疗组(分别是1.59 log10和0.15 log10)。研究表明联合用药安全性和耐受性良好。最常见的不良反应是ALT升高,多数为轻中度升高,且不需药物治疗。研究者分析这可能与HBV DNA水平降低有关。另一款罗氏公司研发的Ⅰ类CpAM药物RG7907也进入了Ⅱ期阶段。
ABI-H0731是由美国Assembly Biosciences公司和我国BeiGene公司研发的一种Ⅱ类CpAM药物。该药的Ⅱ期试验结果同GLS4相似[36],无论是在NUC经治或是初治患者中, ETV+ ABI-H0731组HBV DNA/RNA下降幅度均高于ETV+安慰剂组。
CpAM作为一类新兴的抗HBV药物,早期临床研究发现单一治疗的抗病毒作用相比于NUC并无明显优势,而联合NUC治疗时对HBV DNA和RNA的抑制效果比单用NUC更加显著。不过CpAM+NUC联用方案对于HBsAg下降效果并不明显,未来与PEG-IFN等药物联用的抗病毒方案可能具有良好的前景。
5 HBsAg抑制剂
HBsAg抑制剂是一种核酸聚合物(nuleic acid polymers,NAP),该类化合物可以阻止细胞内亚病毒颗粒的组装,从而抑制HBsAg的分泌[37]。而细胞内的HBsAg通过蛋白酶体或自噬相关途径降解,使得HBsAg不会在胞内累积[38-39]。
目前最具代表性的NAP药物是由加拿大Replicor公司研制的REP 2139和REP 2165。REP 2139的单药治疗在临床试验中表现出色[40]。12例初治HBeAg阳性的CHB患者中有9例血清HBsAg较治疗前下降2.79~7.10 log10,其中3例患者出现HBsAg的清除。在随后的Ⅱ期试验中[41],Replicor公司又评估了REP 2139/REP 2165联合替诺福韦酯(TDF)和PEG-IFN的安全性和有效性。接受实验性疗法(REP 2139/REP 2165+TDF+PEG-IFN)的20例患者中有15例在10周内HBsAg迅速下降4~6 log10,并且治疗48周时共有11例患者出现HBsAg血清学转换。而接受对照疗法(TDF+PEG-IFN)的20例患者中只有3例HBsAg下降>1 log10,并且没有患者出现HBsAg血清学转换。治疗期间两组HBV DNA下降趋势相似,48周时两组共有18例患者HBV DNA低于检测下限。虽然在HBsAg下降期间,共有37例患者出现ALT的升高,试验组ALT升高的幅度更大,不过大多患者在后续治疗过程中均自行缓解。
NAP类药物降低HBsAg的能力显著,是目前众多抗HBV新药中降低HBsAg效果最好的。其与PEG-IFN和NUC三药联用的治疗方案目前看来耐受性和安全性良好,并且在随访期间未出现病毒学指标反弹,与其他抗病毒药物联合疗法可能成为抗HBV治疗的趋势。
6 针对固有免疫的策略
HBV可依托自身多种蛋白质成分,干扰Toll样受体(TLR)或维甲酸诱导基因Ⅰ(RIG-Ⅰ)两种抗病毒信号转导途径,从而抑制固有免疫应答强度[2,42-43]。所以利用细胞因子(IFNα、IFNγ等)或模式识别受体激动剂(TLR、RIG)激活肝细胞和NK细胞等可以强化固有免疫反应[3]。固有免疫可直接抑制肝细胞内病毒复制。
GS-9688(Selgantolimod)是由美国吉利德(Gilead)公司开发的一种TLR-8激动剂[44]。然而该药的Ⅱ期临床研究结果[45]显示,口服3 mg的GS-9688治疗24周,仅使21%(4/19)HBeAg阴性的患者HBsAg下降>0.1 log10。由美国Spring Bank公司研制的一种RIG-Ⅰ激动剂SB-9200(Inarigivir)在早期临床研究[46]中显示出一定下降HBV DNA和HBsAg的作用,但是该药在随后的试验中2例患者出现了重度不良反应,严重的肝毒性导致其中1例患者死亡[47]。Spring Bank公司在2020年初终止了该药的研发。
针对固有免疫的新药临床试验效果并不理想,目前也正在积极寻找与其他药物联用的策略。如何在提高疗效的同时,提高药物安全性和保证患者安全仍是今后该药物研制的方向。
7 针对适应性免疫的策略
慢性HBV感染时,T淋巴细胞长时间暴露于大量病毒抗原以及肝细胞免疫耐受导致HBV特异性T淋巴细胞的功能衰竭[48-49]。缺陷的HBV特异性T淋巴细胞功能可以通过治疗性疫苗和免疫检查点抑制剂来恢复。
治疗性疫苗通过设计HBV特异抗原来刺激抗病毒效应细胞,打破免疫耐受,激发对HBV的特异性免疫反应。治疗性疫苗的研制相比于其他抗乙型肝炎新药开始的较早,但是多项临床试验结果表明治疗性疫苗的效果并不理想:由古巴CIGB研制的NASVAC在治疗NUC经治患者和携带者的研究[50]中,治疗6个月仅有5.6%(4/71)的患者出现HBsAg的清除;由美国吉利德和GlobeImmune公司研发的GS-4774与NUC联合治疗对于HBsAg的下降幅度相较于NUC单药治疗并无明显差异,且并没有患者出现HBsAg清除[51]。如何提高HBV特异性免疫细胞的应答强度与时间,是治疗性疫苗未来研发过程中面临的挑战。可能需要选择更合适的佐剂和抗原与递呈方式,或者需要联合其他类型药物的抗病毒治疗方案。
免疫检查点抑制剂通过靶向阻断抑制受体的负调控信号达到恢复HBV特异性CD8+T淋巴细胞的功能。我国歌礼公司(Ascletis)研发的ASC-22是一款皮下注射的PD-L1抗体。该药物早期试验[52]结果表明, HBsAg呈剂量依赖性下降,且不同剂量组均表现出良好的安全性和耐受性。目前该药处于Ⅱ期阶段。近些年免疫检查点抗体相关药物在治疗肿瘤领域进展较快,然而在治疗CHB进入临床试验的药物不多,不过基于恢复HBV特异性免疫细胞功能的特性在将来治疗HBV感染方面值得期待。
8 展望
过去几十年,乙型肝炎疫苗的全面推广、抗HBV新药的不断研发,均使乙型肝炎的防治工作取得了长足的进步。目前临床上使用PEG-IFN和NUC两类抗HBV药物虽然可以有效抑制病毒复制,促进HBeAg血清学转换,但达到功能性治愈仍比较困难,更无法彻底清除HBV。cccDNA和整合DNA的存在以及HBV特异性免疫的调节仍是抗病毒治疗方法上面临的关键挑战。就目前新药研发的情况来看,尽管siRNA、CpAM等新药进展较快,但进入临床使用及治疗仍需一定时间。并且新药临床试验结果显示单药治疗的效果和稳定性不够理想,而与PEG-IFN、NUC或其他药物联用时下降HBsAg或HBV DNA的能力明显增强。所以针对生命周期和免疫系统,多靶点、多药物联合的治疗方案可能成为将来治疗HBV感染的趋势。
点击链接,免费下载全文
刘义思, 陈新月. 治疗慢性乙型肝炎新药研发的研究进展[J]. 临床肝胆病杂志, 2022, 38(6): 1387-1392.
查看更多