查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





一般资料:患者男性,61岁,于2019年12月就诊。
主诉:间断右上腹不适1个月。
既往史:乙型肝炎病史20余年。
实验室检查:AFP 311 ng/ml,PIVKA II 4390 mAU/ml。
肝功能:AST 71.22IU/L, ALT 104.64IU/L,TBIL 41.15umol/L, DBIL21.87umol/L,IBIL 19.28umol/L,ALB 33.9g/L。
肝脏MR平扫+增强:肝内巨块型病灶,门脉癌栓,腹腔淋巴结转移,未见肺内转移灶,如图1所示。






图1:治疗基线肝脏MR平扫+增强
诊断:原发性肝细胞癌(BCLC C期,CNLC Ⅲb期,Child-Pugh B级),慢性乙型病毒性肝炎
治疗经过
第一阶段治疗
治疗方案:患者于2019年12月行第一次微球导管动脉化疗栓塞术(TACE)治疗,空白微球100-300um。
疗效评价:TACE术后1周复查肝功能提示:AST 130.05IU/L,ALT 161.70IU/L,TBIL 73.24umol/L,DBIL 39.26umol/L,IBIL 33.98umol/L,ALB 30.86g/L;TACE术后4周复查MR肝内肿瘤体积显著退缩,如图2所示。


图2:左右分别为TACE术前与术后4周MR
第二阶段治疗:放疗
治疗方案:患者于2020年1月放弃碘125粒子植入,转行适形调强放疗。
靶区:GTV门脉右支癌栓,CTV:GTV外扩0.5cm;
剂量:6000cGy/30f;患者放疗中耐受性良好,无明显不良反应(图3、图4)。

图3:放疗靶区勾画

图4:放疗剂量
疗效评价:放疗5周后复查,肝内病灶及门脉癌栓未见进展且T2信号减低,如图5所示;腹腔淋巴结增大与肺内新增结节,如图6所示。


图5:放疗5周后肝脏病灶未见进展

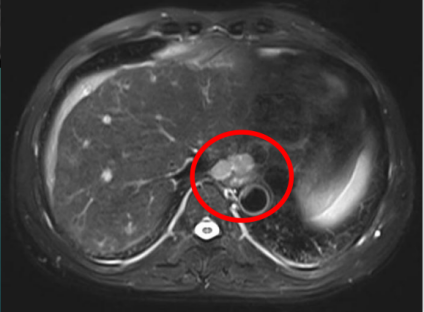
图6:左右分别为肺内及腹腔新发病灶
第三阶段治疗:局部治疗+系统治疗
治疗方案:患者肺内新发病灶、腹腔淋巴结增大,考虑疾病进展,2020年2月起予患者调整为局部联合系统治疗,系统治疗方案为替雷利珠单抗+仑伐替尼;期间患者先后于2020年3月接受第二次TACE载药微球(30-60um)+ 法玛新40mg(四倍法)治疗,2020年6月接受第三次微球TACE治疗。
疗效评价:患者在局部联合系统治疗期间,先后于2020年4月(第二次TACE治疗1月后)、2020年6月(第二次TACE治疗3月后及第三次TACE治疗前)、2020年9月(第三次TACE治疗3月后)复查胸腹部影像,可见门脉癌栓无进展,腹腔淋巴结及右肺转移灶持续缩小,疗效评价为部分缓解(PR),影像变化如图7所示。




图7:治疗期间各病灶变化
病例总结
本例患者老年男性,乙型肝炎病史20余年,本次以“间断右上腹不适1个月”就诊,结合既往病史及辅助检查结果,明确诊断为原发性肝细胞癌(BCLC C期,CNLC IIIb期,Child-Pugh B级)。
患者确诊后,先后进行了TACE治疗及放疗,肝癌病灶虽在短期内得到控制,但仍无法避免短期内出现病情进展——患者于放疗后1个月左右出现了肺内新发病灶及腹腔淋巴结增大。面对复发转移的新挑战,予患者调整为局部联合系统治疗。基于近年来靶向与免疫治疗在晚期肝癌诊疗中取得的诸多突破性进展,两者联合能发挥“协同增效”作用,故在系统治疗方面,予患者应用了替雷利珠单抗联合仑伐替尼治疗,期间予患者先后进行了第二次及第三次TACE治疗。患者在联合治疗期间,门脉癌栓无进展,腹腔淋巴结及右肺转移灶持续缩小,疗效评价达PR。
由此可见,对于肿瘤多发、不可手术切除、进行局部治疗的晚期肝癌患者,推荐联合免疫治疗,发挥“协同增效”作用。局部治疗能进一步提高患者对免疫药物的适用率和受益率、减少反应时间、增强对肿瘤症状/进展的临床控制、延长患者对药物反应的程度和持续时间,给患者带来更多获益。
本例患者应用的替雷利珠单抗经Fc段改造,消除了抗体依赖细胞介导的吞噬作用(ADCP),具有更好的抗肿瘤活性。近期,替雷利珠单抗用于不可切除肝癌二线及以上治疗的全球、多中心、Ⅱ期临床研究——RATIONALE 208研究公布了最新数据,替雷利珠单抗单药方案在后线治疗中显示了可喜的有效性,中位OS达13.2个月,比肩国际同类药物既往数据。同时部分患者能够实现深度缓解,获得完全缓解(CR);近80%的疾病缓解患者PFS超过一年,提示患者人群一旦起效,则不易耐药,抗肿瘤作用稳定而持久。而基于RATIONALE 208研究结果,替雷利珠单抗已于2021年6月22日获得国家药品监督管理局(NMPA)批准用于至少经过一种全身治疗的肝细胞癌的治疗。
▼
往期推荐
▼

扫码二维码
查看往期
更多精彩
中国医学论坛报编辑|金金 整理
查看更多