查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





16岁的男孩,出现肢端肥大(杵状指)、乳房发育等内分泌功能障碍多年,无家族史,外院MRI提示垂体病变(垂体Rathke囊肿?),遂来我科咨询。
一看头颅MRI,我们惊呆了!
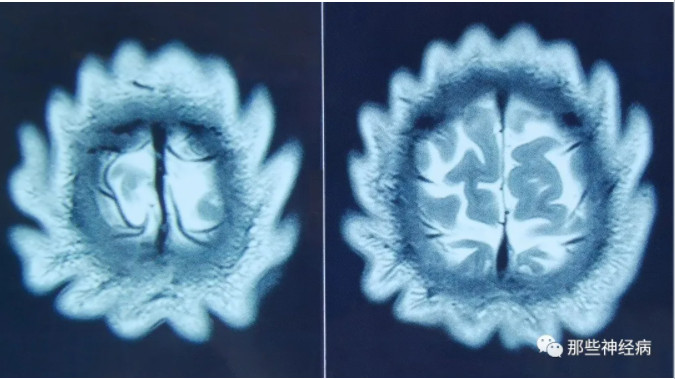
神经科的同行,猜猜这是什么罕见病?
结合病史若不能猜出,那再加点料,看看患者前部额头的皮肤:
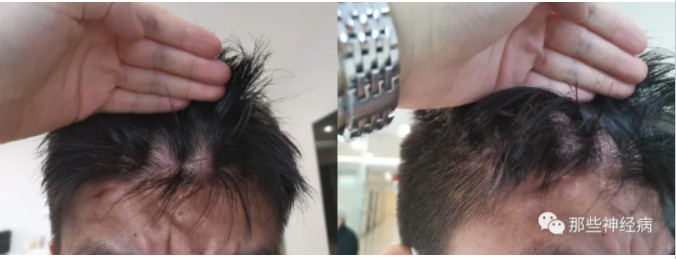
内分泌科已秒杀:PHO!
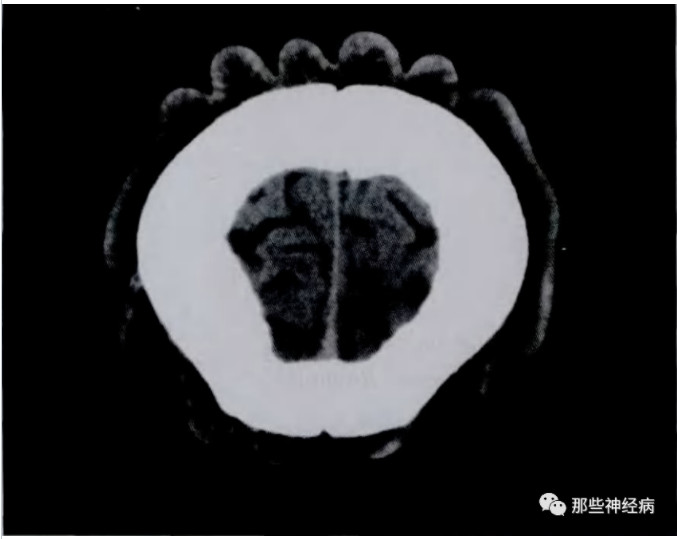
(李东明等. 中华内分泌代谢杂志. 2014.)
皮肤科也已拿下:PDP!
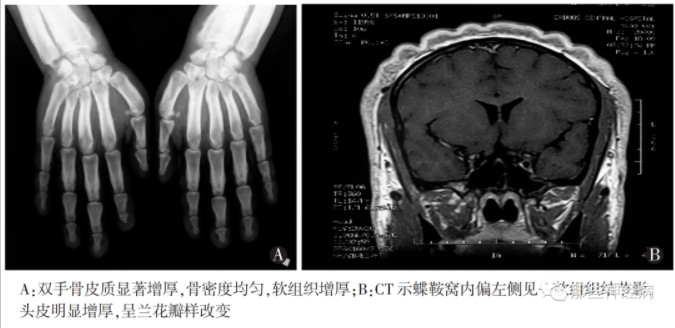
(杨怡等.临床皮肤科杂志.2010.)
而神经科的你,猜到了吗?
头部皮肤软组织增厚皱褶,文献在查体中描述为“头皮回纹征”,而如此影像还未命名,我们姑且称她为“花瓣征”。
这例花瓣征患者基因检查已外送,半月后静待花开!
皮肤骨膜增厚症
1868年,Friedreich首次报道了皮肤骨膜增厚症(pachydermoperiostosis,PDP),又称原发性肥大性骨关节病(primary hypertrophic osteoarthropathy,PHO),该病的主要表现为骨骼和皮肤异常。
PDP是一种十分罕见的遗传性骨病,呈常染色体隐性或非完全外显性遗传。其主要临床表现为杵状指、骨膜增生、回状头皮和皮肤肥厚,有的患者还伴随有肢端骨质溶解症、多汗症、皮脂溢男性女乳症等症状。
临床表现
杵状指是PDP最常见的体征,皮肤增厚以脸部皮肤和头皮进行性增厚、逐渐形成皱褶为特征。
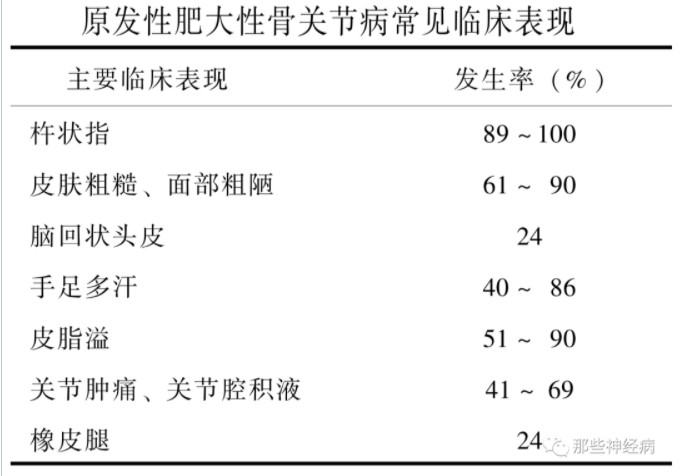
双手及足指(趾)皮肤粗糙、肥厚,末端呈杵状膨大。
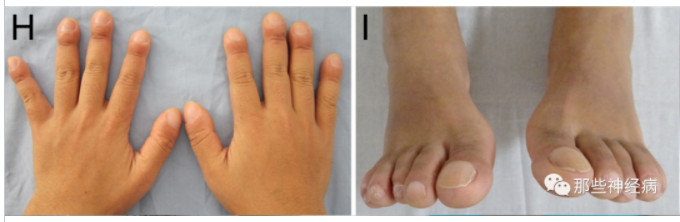
脑回状头皮为患者头部皮肤粗糙,明显增厚起皱如脑回状,多位于前额头皮。

(Zhang Z, et al. J Clin Endocrinol Metab. 2013. )
面部皮肤增生可呈“狮面征”,下肢可有“象腿样”改变。
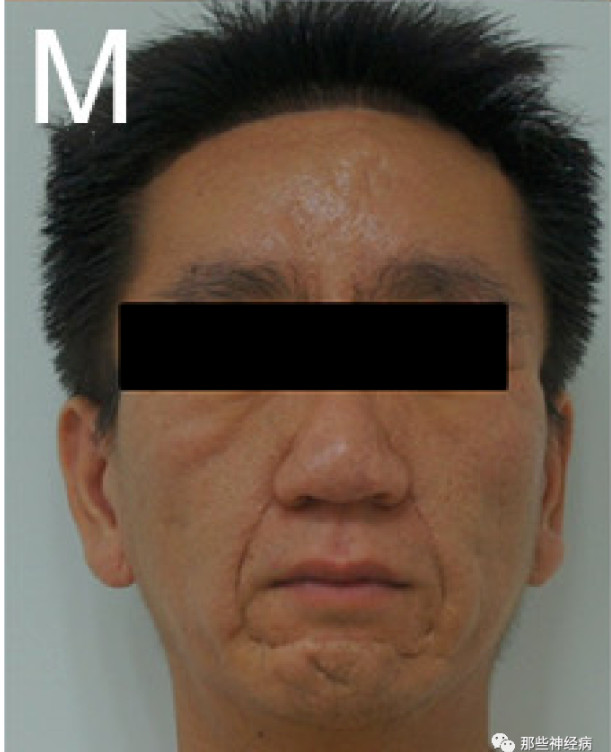
(Zhang Z, et al. J Clin Endocrinol Metab. 2013. )
头颅影像学如下:
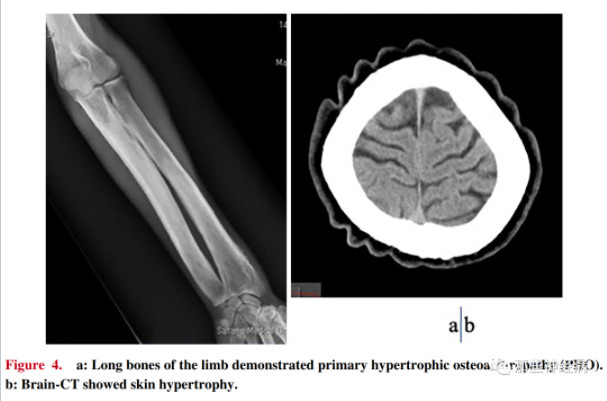
(Tsuzuki Y, et al. Intern Med. 2020.)
骨骼异常主要影像学表现为X线片示骨膜增生、骨赘形成、指趾末端骨质溶解(多发生在发病10年后),骨扫描示骨骼摄取弥漫性增高。
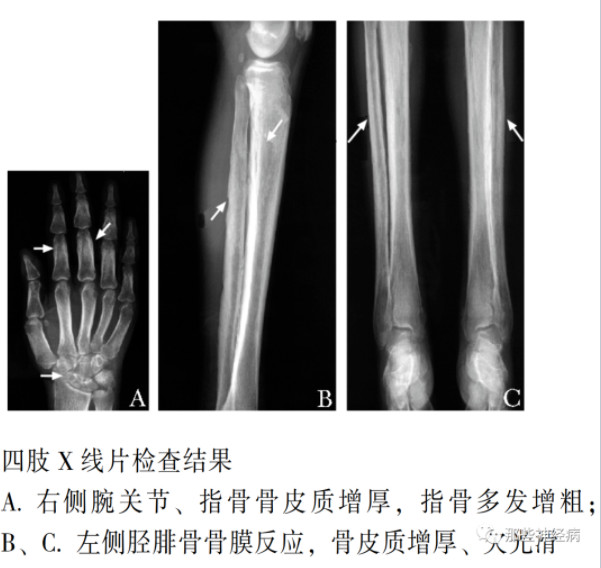
(都雪朝等. 协和医学杂志. 2015. )
临床分型
根据PDP临床表现可分为3种亚型:
①完全型:同时存在皮肤增厚、骨膜增生及杵状指;
②不完全型:表现为骨膜增生明显而皮肤增厚不明显;
③顿挫型:存在皮肤增厚表现,但骨膜增生轻微或缺如。
发病机制
发病机制涉及15-羟基前列腺素脱氢酶基因(HPGD)及前列腺素转运体2A1基因(SLCO2A1),其表达产物均参与前列腺素E2的运输和代谢,二者的异常是导致原发性厚皮性骨膜病的主要原因。
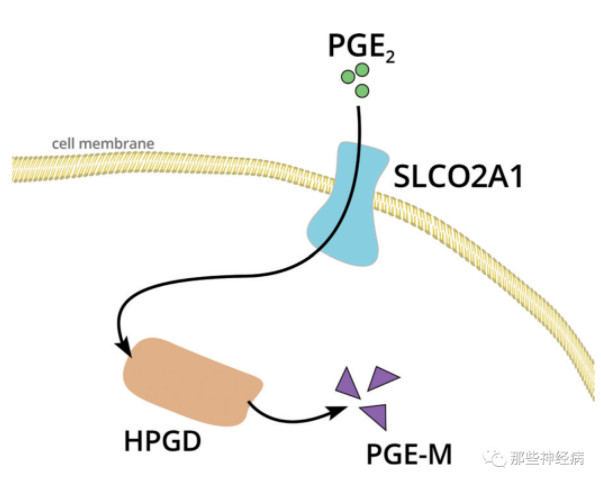
目前认为与PGE2代谢障碍有关。前列腺素转运体(PCT)将PGE2转运入细胞,然后由15-PGDH代谢生成前列腺素M(PGM)排出体外。PGT及15-PGDH分别由SLCO2A1基因和HPGD基因编码。因此SLCO2A1基因或HPGD基因突变均可导致前列腺素降解障碍,引起PGE2水平升高,PGE2堆积,导致PDP。
HPGD基因
HPGD基因位于染色体4q33-q34区,共包含7个外显子,编码由266个氨基酸组成的15-羟基前列腺素脱氧酶(15-PGDH)。HPGD的纯合和杂合突变是导致原发性厚皮性骨膜病的主要原因之一。
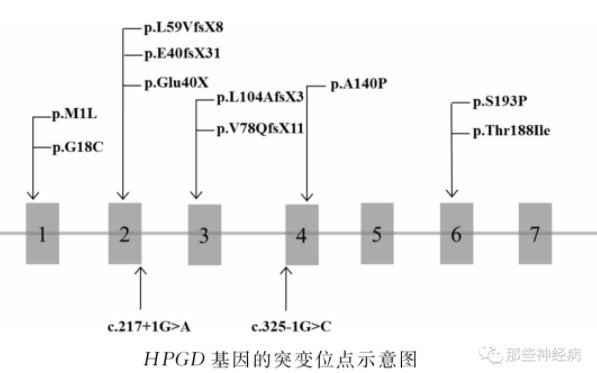
目前已知的HPGD突变共有12个,其中最频繁出现的突变包括错义突变,共有5个,移码突变共4个,1个无义突变和2个剪切位点突变。HPGD的第2外显子检测出4个突变位点,第1、3、4和6外显子均检测到2个突变位点,第5和第7外显子尚未检测出突变。
SLCO2A1基因
2012年,上海张增和章振林教授团队对原发性肥大性骨关节病家系先证者进行全外显子组测序,发现SLCO2A1 基因纯合突变,并在其他家系中得到了验证,在国际上首报了 SLCO2A1是该病的又一致病基因,也是国人的骄傲!

SLCO2A1位于染色体3q21区,包含14个外显子,用于编码前列腺素运输蛋白(PGT), PGT由643个氨基酸组成,是细胞表面阴离子运输蛋白,包含有12个穿膜结构域,7个胞内结构域,6个胞外结构域。
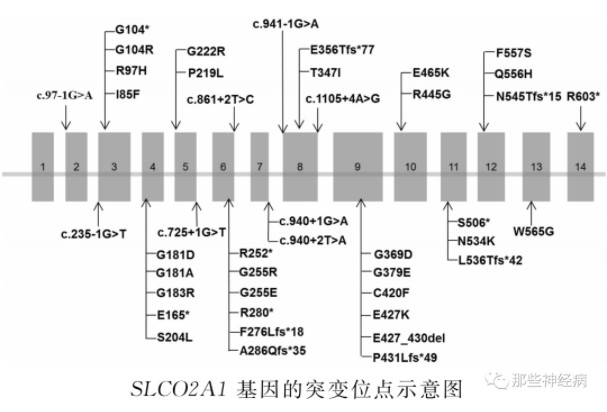
SLCO2A1突变也是导致厚皮性骨膜病的主要原因之一。目前已知的SLCO2A1突变共有43个,其中有8个剪切位点突变,主要集中在第7和第8外显子之间。PGT的突变主要集中在第4、6和9外显子,其中第4外显子上包含5个突变,第6外显子上包含7个突变,第9外显子上包含6个突变,其他外显子上也包含少数突变位点。
基因与PDP的分型
目前的研究结果表明PDP包括:(1)由HPGD缺陷引起的原发性厚皮性骨膜病常染色体隐性性状1 (PHOAR1);(2)由SLCO2A1缺陷所引起的原发性厚皮性骨膜病常染色体隐性性状2 (PHOAR2) 。
尽管PHOAR1和PHOAR2的临床表型很相似,但存在差异:
①这两种PDP其症状开始出现的年龄极端呈现双峰分布,PHOAR1的峰值出现在1岁左右,伴随有高发生率的动脉导管未闭和颅缝缺陷。PHOAR2的峰值却出现在青春期。具有SLCO2A1突变的患者其临床表现显露得比HPGD突变患者晚并且杵状指在青春期才开始显现,皮肤肥厚也在青春期后不久显现。
②在性别的比例上二者存在显著的区别, PHOAR1的患者男女比例接近1:1,但是没有一个女性患者表现出PHOAR2的典型的皮肤或骨骼的特征。
③动脉导管未闭和其他的先天性心脏疾病在PHOAR1患者中普遍发生。但是通过超声心电图发现这些疾病并未出现在PHOAR2患者中。
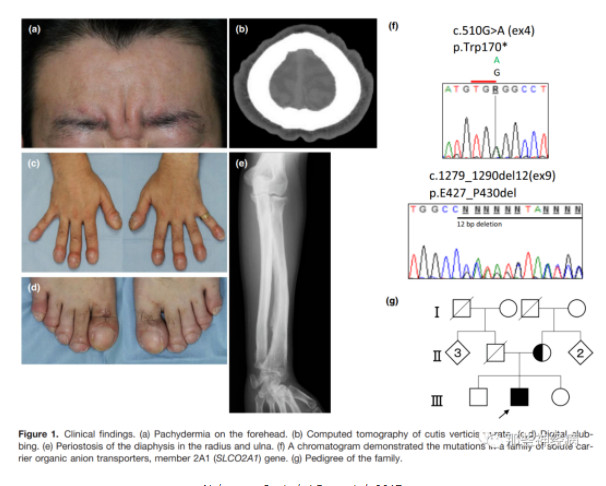
(Nakazawa S, et al. J Dermatol. 2017.)
④皮肤肥厚在PHOAR1和PHOAR2患者中均有出现,但回状头皮和骨髓纤维化只出现在PHOAR2患者中,并且肢端骨质溶解症在PHOAR1患者中更为显著,关节痛、关节损伤和皮肤肥厚的程度SLCO2A1突变的患者比HPGD纯合或杂合突变患者更显著。
治疗
目前PDP还没有根治的特效方法,主要的治疗药物是非类固醇类抗炎药,如阿司匹林、塞来昔布、依托考昔等。
前列腺素内过氧化物合酶2 (PTGS2)是一种催化代谢花生四烯酸的酶,能够将花生四烯酸转化为前列腺素。阿司匹林能够抑制PTGS2,使PGE2的合成受到抑制,从而对PDP起到一定治疗效果。但实验发现低剂量的15-PGDH,有抑制阿司匹林作用。
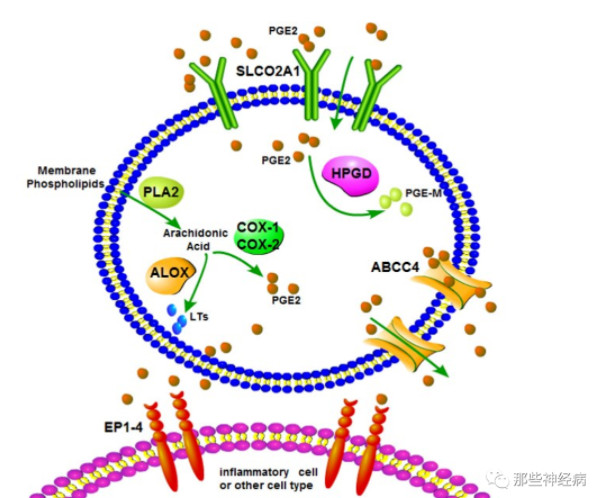
环氧合酶-1(COX-1)和环氧合酶-2(COX-2)在合成PGE2中起着很大的作用。舒林酸,一种能代谢为舒林酸硫化物的前药,是COX-1和COX-2的双重抑制剂。塞来昔布是一种COX-2的选择性抑制剂,这两种药均在一定程度上抑制PGE2的合成,从而缓解原发性厚皮性骨膜病的症状。
来源:那些神经病(王乾成)
查看更多