查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:东部战区总医院 国家肾脏疾病临床医学研究中心 全军肾脏病研究所 杨柳 谢红浪 刘志红
主诉及现病史
患者女性,20岁,因“尿检异常伴贫血、血小板低10天,肌酐高5天”入院。
2015年4月29日,患者无诱因出现面部及双下肢浮肿,就诊于外院,查尿蛋白9175mg/24h(尿量1500ml),隐血2+,白蛋白(ALB)21.9g/L,球蛋白(GLO)、肝酶正常,血肌酐(Scr)67.1μmol/L,血红蛋白(Hb)79g/L,血小板(PLT)68×109/L,IgG低,抗核抗体(ANA)、抗双链DNA(dsDNA)抗体、抗干燥综合征抗原A抗体(抗SSA抗体)、抗核小体抗体、抗核糖体P蛋白抗体阳性,补体低,予甲泼尼龙(MP)40mg/d静滴3天后血象略改善。
5月3日,患者出现咳嗽、咳痰、发热,体温39℃,无畏寒及寒战,抗感染、对症治疗(具体不详)效果不佳。
5月7日,患者入我院急诊,肺部CT示两肺散在炎症伴胸腔积液,降钙素原0.92ng/ml,诊断为肺部感染,静滴头孢他啶抗感染1天。病程中曾肩部肌肉酸痛、面部红斑、光过敏,偶有胸闷、呼吸困难,无头痛、腰痛、尿频、尿急、尿痛、口干、眼干、口腔溃疡,体重下降约3kg。
既往史、个人史及家族史
既往史及个人史无特殊,月经正常,未婚未育,1姑母患肾炎,母亲患“抑郁症”
体格检查
体温37.1℃,血压120/76mmHg,心率110次/分,双颧部红斑,心率快,律齐,各瓣膜听诊区未闻及杂音或病理性心音,双肺散在干湿啰音,双下肺听诊呼吸音减弱、叩诊呈浊音,腹部查体未见异常,双肾区叩击痛阴性,双下肢无水肿。
实验室检查
尿液 尿常规红细胞++,尿沉渣红细胞计数50万/ml(多形型),白细胞2~4/HP,尿蛋白+++,尿糖、胆红素、酮体阴性,C34mg/L,α2巨球蛋白(α2m)6mg/L,N-乙酰-β-D-氨基葡萄糖苷酶(NAG)52.9U/(g·cr),视黄醇结合蛋白(RBP)44.1mg/L,溶菌酶11.1mg/l,禁饮13h尿渗量344mOsm/(kg·H2O)。钠滤过分数3.58%、肾衰指数4.97。
血常规 Hb51g/L,网织红细胞2.35%,白细胞5.8×109/L,PLT79×109/L。外周血红细胞碎片阴性。
血生化 ALB31.1g/L,GLO19.7g/L,尿素氮(BUN)28.91mmol/L,Scr383.66μmol/L,尿酸(UA)683μmol/L,胱抑素C7.47mg/L,胆红素及转氨酶正常,乳酸脱氢酶(LDH)454U/L,无明显电解质紊乱及酸碱失衡,血脂、血糖正常,C反应蛋白(CRP)53.7mg/L,脑利钠肽(BNP)1180pmol/L,降钙素原(PCT)0.688μg/L,肌钙蛋白T0.101ng/ml,肌钙蛋白I0.73ng/ml。
凝血功能 凝血酶原时间12.4s,活化的部分凝血活酶时间44.1s,国际标准化比值(INR)0.8,凝血时间19.6s,纤维蛋白原334mg/L,D-二聚体0.53mg/L。
免疫学 ANA1︰256,抗ds-DNA抗体、抗中性粒细胞胞浆抗体阴性,抗心磷脂抗体(ACL)-IgG13.94IU/ml、IgM33.92IU/ml、IgA15.24IU/ml,抗β2-糖蛋白1抗体阴性,狼疮抗凝物(LA)正常,抗肾小球基膜(GBM)抗体和抗肾小管基底膜(TBM)抗体阴性,补体C30.497g/L,补体C40.1g/L,IgG5.75g/L,IgA、IgM、IgE正常,类风湿因子、抗“O”阴性。外周血淋巴细胞亚群CD3+411个/μl,CD4+123个/μl,CD8+271个/μl,免疫球蛋白冷沉淀83.43mg/L。抗人球蛋白试验(Coomb's试验)阳性,间接抗人球蛋白试验、血清酸化溶血试验阴性。
内皮细胞功能 血管内皮细胞黏附分子(VCAM)、血栓调节蛋白(TM)、循环内皮细胞及E选择素均正常。血管性血友病因子裂解酶(ADAMTS13)抗体阴性、活性正常。
病原学 多次血培养及痰培养阴性,呼吸道病毒抗体阴性,结核感染T细胞检测阴性,半乳甘露聚糖抗原检测(GM试验)无明显异常,真菌1,3-β-D葡聚糖检测(G试验)阴性。
辅助检查
心电图 大致正常。眼底检查未见明显异常。
肾脏B超 左肾118mm×49mm×59mm;右肾116mm×46mm×58mm,皮质回声增强,皮髓界限不清,集合系统光带分离左7mm,右6mm(2015年5月8日)。
胸部CT 左肺上叶舌段及两肺下叶炎症;双侧胸腔积液伴左肺下叶萎陷;纵隔及双侧腋窝多发小淋巴结(2015年5月8日)。
头颅磁共振成像(MRI) 左颞叶可疑条状血管影。
心脏超声 二尖瓣局部回声略增厚,前叶瓣尖似见点状强回声漂浮,瓣膜开放尚可,关闭欠佳,轻度反流;左心室内径49mm;左室射血分数(LVEF)60%(2015年5月12日)。(图1A)
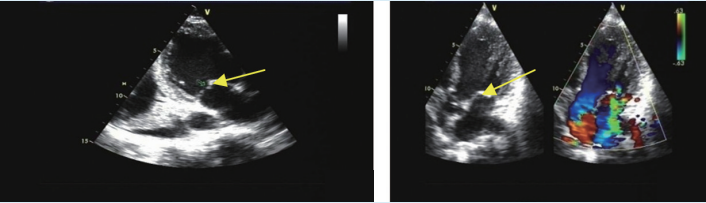
图1 A 二尖瓣局部回声略增厚,前叶瓣尖似见点状强回声漂浮(2015年5月12日),B 心脏彩超示二尖瓣钙化 并重度关闭不全(2015年7月1日)。
2015年5月8日
患者入院后静滴MP(40mg/d)控制原发病、莫西沙星(0.4g/d)抗感染。反复发热,体温最高38.8℃,伴咽痛、流涕,尿量1200ml/24h,尿色正常,5月9日起尿量迅速减少、BNP及Scr升高(图2)。
5月10日
患者无尿,开始连续性血液净化治疗(CRRT)、换比阿培南0.3g/8h继续抗感染。因血液系统损害严重,于5月12日予MP(0.5g/d)治疗3天。治疗10天后,患者体温正常,仍间断流涕,查CT示肺部病变无明显改善,5月25日予人免疫球蛋白冲击治疗5天(15g/d×5d),后Coomb's试验转阴,PLT升至118×109/L。
6月18日
患者BNP仍4138pmol/L,血压正常,持续无尿,予激素减量。返回当地血液透析3次/周,每次脱水2kg,体重下降5kg。6月27日患者心慌、胸闷渐加重,夜间不能平卧,频繁咳嗽、咳黄痰、气喘、咯血,复查CT示两肺弥漫炎症,PCT1.530μg/L、BNP4138pmol/L,考虑心功能不全伴肺部感染,予静滴比阿培南抗感染、行CRRT脱水3200ml后胸闷好转、咯血减轻。N端脑尿钠肽前体(NT-ProBNP)>35000pg/ml,脑利钠肽前体(PRO-BNP)2686.60pg/ml,复查ACL-IgG升至25.36IU/ml。改为血液透析4次/周,血压控制正常、外周无浮肿情况下仍反复胸闷。
7月1日
患者复查心脏彩超,二尖瓣见点片状强回声,瓣膜开放尚可,关闭欠佳,关闭时略错合,左心室内径50mm,左室壁各节段运动幅度减低;左心功能减低;二尖瓣钙化并重度关闭不全(图1B);轻度主动脉瓣反流;LVEF34%。
7月29日
行“二尖瓣置换术”,术中见二尖瓣叶边缘增厚,钙化样赘生物附着。术后BNP明显下降(图2),继续普通透析3~4次/周,华法林1.25mg/d抗凝,尿量渐恢复至1000ml/24h,监测尿蛋白持续3~3.2g/24h,少量镜下血尿。后于8月复查ACL转阴。出院后静滴环磷酰胺(CTX)共1.6g(0.4g/月×4次)。
10月27日
患者尿蛋白降至0.4~1g/24h。透析间期尿量逐渐增加,BNP持续下降,透前Scr、BUN下降,予下调透析频次。
2016年6月
尿量增至1500ml/24h,摆脱透析。2017年8月尿蛋白阴性,Hb92g/L,PLT94×109/L,Alb正常,Scr320.89μmol/L,心脏超声LVEF63%。
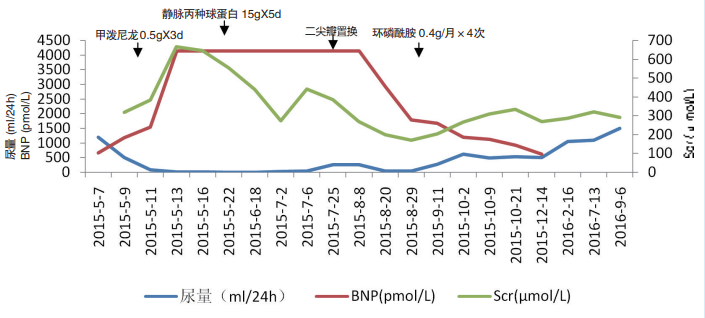
图2 患者尿量、BNP及Scr变化
系统性红斑狼疮(SLE)伴抗磷脂抗体综合征(APS)[累及心脏、肾脏、血液系统、皮肤,狼疮疾病活动性指数(SLE-DAI)12分],非典型疣状心内膜炎(Libman-sacks心内膜炎),急性心功能不全,纽约心脏病学会(NYHA)分级Ⅲ级,急性肾皮质坏死(图3),急性肾损伤3期(肾脏替代治疗中),肺部感染。
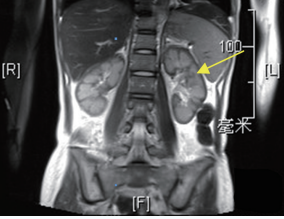
图3 肾脏MRI示肾皮质坏死(肾皮质及 肾柱信号减低,皮髓分界不清)
抗磷脂抗体综合征
APS是在有抗磷脂抗体(APL)实验室证据的同时,出现静脉或动脉血栓形成或特定病理性妊娠,通常根据病因分为原发性和继发性APS,后者多见于系统性红斑狼疮。APS临床表现包括心瓣膜病、网状青斑、血小板减少、肾动脉狭窄、肾静脉血栓、血栓性微血管病和神经系统损害等,实验室检查包括抗心磷脂抗体(ACL)、抗β2-糖蛋白Ⅰ(β2GPI)抗体、抗磷脂酰丝氨酸抗体等阳性。体内血浆蛋白与磷脂结合后暴露或产生表位,形成针对性抗体APL。APL可直接导致血小板活化、黏附内皮,亦可直接活化血管内皮细胞,致单核细胞与活化血小板结合增加,引起组织因子、趋化因子和生长因子表达,促进血栓形成。
目前认为即使存在APL,也需要吸烟、长期制动、妊娠、感染等“二次打击”触发APS。研究表明感染后细菌脂多糖及病毒糖蛋白模拟内源性β2GPI结构,通过激活Toll样受体-4(TLR-4)路径活化免疫系统,诱发、加重APS,多个脏器受损后器官间交互作用可致病情恶化。APS治疗主要包括普通肝素、低分子肝素、华法林及阿司匹林,合并SLE者可受益于硫酸羟氯喹。如APL阳性者一周内出现三个及以上器官、系统受累,且至少一个器官经组织学证实存在小血管闭塞,则称为“灾难性”APS,需在抗凝、糖皮质激素基础上行血浆置换和丙种球蛋白治疗。
本例患者SLE诊断明确,ACL阳性,起病合并呼吸道细菌感染及病毒感染,内脏损害表现为急性肾皮质坏死及Libman-sacks心内膜炎。推测其在SLE背景下,经感染、炎症等因素“二次打击”后,体内APL激活血管内皮细胞、单核细胞及血小板,形成微血栓,引发血小板减少及心肾损害。SLE心脏瓣膜受累率达60%~74%,ACL阳性者Libman-sacks心内膜炎发生率较ACL阴性患者高3倍,常见表现为直径1~4mm疣状赘生物形成,呈菜花样或扁平状,多发于瓣膜交界处或边缘。患者多于心脏听诊、超声心动图或尸检中被发现,严重瓣膜返流者有呼吸困难、端坐呼吸等心功能不全表现。在血流动力学稳定的前提下,主要采用糖皮质激素和抗凝剂治疗。糖皮质激素能减轻炎症反应,但亦可促进组织纤维化及瘢痕形成。由于血栓风险增加,应长期抗凝预防,如出现严重瓣膜失功,需及时手术。
心肾综合征
心脏和肾脏中一个器官急性或慢性功能障碍可诱发另一器官急性或慢性功能损害的临床综合征称为心肾综合征(cardiorenal syndrome,CRS),朗科 (Ronco)等根据可能的心肾交互作用,将CRS分为5种亚型,即Ⅰ型CRS(急性心肾综合征)、Ⅱ型CRS(慢性心肾综合征)、Ⅲ型CRS(急性肾心综合征)、Ⅳ型CRS(慢性肾心综合征)和Ⅴ型CRS(继发性心肾综合征),病程不同阶段可呈不同亚型。
本患者病初ACL致Libman-sacks心内膜炎及急性肾皮质坏死,急性失代偿性心功能不全加重急性肾损伤(AKI),AKI亦可引起容量负荷增多,加重心脏负担,造成心功能进一步恶化,但心瓣膜置换术后患者心功能明显改善,提示其发病机制以Ⅰ型CRS为主,即为血流动力学变化、神经内分泌系统激活及免疫炎症反应介导所致。治疗Ⅰ型CRS首选袢利尿剂,对于失代偿性心力衰竭患者,积极体液清除可改善预后;血管紧张素转换酶抑制剂(ACEI)或血 管紧张素Ⅱ受体阻滞剂(ARB)有助于改善心衰症状;治疗急性失代偿性心衰可考虑血管舒张剂和正性肌力药;血液净化治疗能有效进行液体管理、清除尿毒症毒素、纠正电解质紊乱、改善利尿剂抵抗,以免激活神经内分泌系统。
本例患者确诊为Libman-sacks心内膜炎后,因二尖瓣重度关闭不全导致心功能不全,综合其一般情况及瓣膜病变性质,为避免过度抗凝引起出血,予生物瓣膜进行二尖瓣置换。
术后监测BNP水平持续下降,心功能逐渐恢复。随访期间经积极肾脏替代治疗、口服利尿剂及ACEI,伴随心功能改善,肾功能亦有所恢复,尿量逐渐增至正常。随访过程中以环磷酰胺治疗原发病后心肾功能进一步改善。
本例系统性红斑狼疮伴抗磷脂抗体综合征患者,在肺部感染等“二次打击”情况下,继发心瓣膜病变、急性肾皮质坏死等危及生命的并发症,导致严重的心脏、肾脏、血液等多个重要脏器功能损害。经过积极的抗感染、肾脏替代、瓣膜置换及免疫抑制治疗,心脏和肾脏功能得以改善。

来源:《中国医学论坛报》2020年10月29日A3、A8版
查看更多