查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





点击进入专题:
作者:复旦大学附属华山医院神经内科 血管组 刘心雨 洪澜
急性缺血性脑卒中(Acute ischemic stroke,AIS)的治疗方法主要包括改善脑血循环和神经保护治疗。随着目前组织窗影像评估研究的不断发展,再灌注治疗时间窗不断被延长,但仍有大部分卒中患者遗留残疾,而在血管再通基础上进行有效的神经保护治疗被认为有机会进一步改善患者临床预后。但近二十年来,大量理论上及动物实验中表现出较好效果的神经保护治疗并未能在随后的临床试验中取得有效治疗效果[1]。
这些试验的失败存在许多方面的原因,包括患者缺血区域的异质性及药物剂量、治疗时间窗的转变等,而在这些变量中,实验的严谨性是可以被人为控制的。
为了最大程度地测试神经保护治疗的动物实验效果并提高临床试验成功的可能性,美国国家神经系统疾病和中风研究所(National Institute of Neurological Disorders and Stroke, NINDS)在2016年召开研讨会,资助成立了卒中临床前评估网络(Stroke Preclinical Assessment Network, SPAN)。该网络包括六个独立实验室、一个中央协调中心以及NINDS,对有治疗前景的候选药物进行严谨的临床前评估,以便在未来的临床试验研究中获得进一步的成功。
2023年2月8日,来自耶鲁大学医学院的Lauren H Sansing教授公布了SPAN的主要研究成果。

SPAN是一项随机、对照、盲法、多实验室研究,动物通过实验室、性别以及动物模型等进行随机。
研究中共纳入6种神经保护治疗药物或方法:
1. Rho激酶抑制剂法舒地尔
2. 远隔缺血适应(Remote ischemic conditioning,RIC)
3. 多聚二磷酸腺苷核糖聚合酶抑制剂维利帕尼
4. 重组人源化抗人白介素 6(IL-6)受体单克隆抗体托珠单抗
5. 强效自由基清除剂尿酸
6. 神经鞘氨醇1-磷酸受体调节剂芬戈莫德
研究终点:
主要终点:
1. 角落测试(Corner test)结果
次要终点:
1. MRI所示梗死体积
2. 其他行为学测试结果,如网格行走(grid walk)
所有参与的研究实验室对同等数量的雄性和雌性幼鼠、年轻大鼠、老龄小鼠、饮食诱导肥胖小鼠和自发性高血压大鼠进行了标准的一过性大脑中动脉闭塞手术。实验动物在结束手术再灌注时予以神经保护治疗,术后进行行为学评估并获取核磁影像(magnetic resonance imaging, MRI),所有的核磁影像都通过自动分割分析划定梗死体积以及受损区域后上传至中心数据库。
基于治疗效果的临床意义,该研究在多臂多阶段统计方法中定义了有效性(高于50%)和无效性(少于15%)界值,在四个连续阶段的任一阶段显示无效后则放弃该干预。
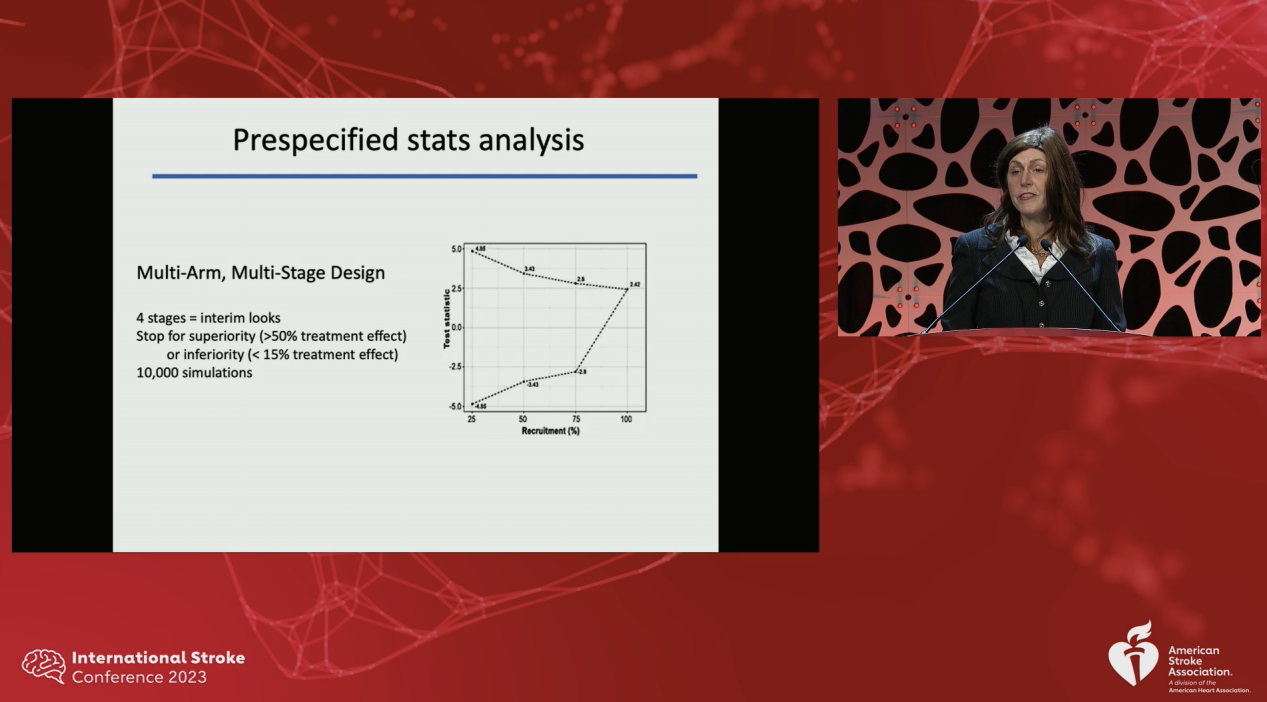
SPAN共纳入了2651只动物,最终共1872只动物完成研究(包含幼鼠713只,年轻大鼠200只,老龄小鼠213只,饮食诱导肥胖小鼠355只,自发性高血压大鼠391只,其中雌鼠共935只)。经过第一及第二阶段后,还剩三种治疗方法继续进行实验,经历过第三及第四阶段后,仅剩一种治疗方式,即再灌注治疗时静脉注射16 mg/kg的尿酸达到了主要终点。次要终点的结果将在后续的会议中展示。

SPAN研究通过了最严谨的设计与执行,用多中心临床试验的思路进行动物研究,显示出了非凡的数据质量,这项研究可用于类似的临床前的、多实验室研究,有助于提高动物实验向临床转化的可行性及可重复性,有利于后续临床试验的准备[2]。
再灌注治疗是缺血性卒中急性期首选治疗方法,但仍然仅有部分高级卒中中心可对患者进行再灌注治疗。而神经药物保护治疗在各个层级的医疗中心得到广泛的应用,减轻脑组的织缺血性损害。卒中治疗学术产业圆桌会议(Stroke Treatment Academic Industry Roundtable,STAIR)在神经保护疗法长期未取得实质性进展的现状下成立,也使神经保护治疗初见曙光[3, 4]。而借助于SPAN研究的初步成果,可以期待未来看到更多神经保护剂的有效动物实验成果向临床转化。
参考文献
[1] O'COLLINS V E, MACLEOD M R, DONNAN G A, et al. 1,026 experimental treatments in acute stroke [J]. Annals of neurology, 2006, 59(3): 467-77.
[2] WRIGHT C B, BOSETTI F, JANIS L S, et al. Organizational Update: NINDS Stroke Research Strategies for Large Vessel Occlusion and Neuroprotection [J]. Stroke, 2021, 52(1): e1-e2.
[3] XU J, WANG A, MENG X, et al. Edaravone Dexborneol Versus Edaravone Alone for the Treatment of Acute Ischemic Stroke: A Phase III, Randomized, Double-Blind, Comparative Trial [J]. Stroke, 2021, 52(3): 772-80.
[4] HILL M D, GOYAL M, MENON B K, et al. Efficacy and safety of nerinetide for the treatment of acute ischaemic stroke (ESCAPE-NA1): a multicentre, double-blind, randomised controlled trial [J]. Lancet, 2020, 395(10227): 878-87.
查看更多