查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





当地时间2021年8月12日,《细胞·癌症》(Cancer Cell)杂志(影响因子31.74分)正式发表了广东省人民医院吴一龙教授团队领衔开展的ARTEMIS-CTONG1509研究。该研究是首个在中国携带表皮生长因子受体(EGFR)突变的非小细胞肺癌(NSCLC)患者中进行的随机、开放、多中心Ⅲ期研究,对比了贝伐珠单抗联合厄洛替尼与厄洛替尼单药治疗的疗效和安全性,深入探索了EGFR-酪氨酸激酶抑制剂(TKI)与抗血管生成药物的联合治疗策略。
是什么原因引发吴一龙教授团队系统地开展了这一研究?本次发布的研究数据又提示了哪些要点?研究背后蕴含了哪些故事?为此,本报科研背后专栏特别邀请吴一龙教授团队,为我们讲述研究详情、分享研究背后的故事与思考。
35%~50%!在亚洲竟然有高达这样比例的肺癌患者携带EGFR突变,而对不幸罹患EGFR突变NSCLC患者的“幸运”,莫过于研究明确证实,这类患者使用TKI类靶向治疗比标准化疗疗效更好、副作用更低。吴一龙教授指出,EGFR-TKI靶向治疗对于EGFR突变阳性NSCLC来说是一线治疗首选,这已经是近年来治疗晚期肺癌的临床基本共识。
然而,绝大多数接受靶向药物治疗的患者,都会在治疗或长或短之后,面临治疗耐药这一窘境,导致疾病发生进展。此外,不同临床特征、不同突变亚型的患者在靶向治疗药物中的获益程度也不同。
对此,吴一龙教授表示,针对这些患者仍有可以进一步提高的空间和临床需求,如何提高疗效,尤其是如何提高在EGFR-TKI单药中获益相对较小的特殊人群的疗效,是临床需要直面解决的问题。吴一龙教授曾说道:“癌症的一种治疗策略基本确定后,第二个阶段就是对该治疗策略的优化,而优化的治疗策略能让患者活得更长、活得更好。”
ARTEMIS-CTONG1509研究对比了贝伐珠单抗联合厄洛替尼与厄洛替尼单药治疗的疗效与安全性,并探索了两组患者获得性耐药的特点。主要研究终点为独立审查委员会(IRC)评价的无进展生存期(PFS)。吴一龙教授特别指出,这是一项在中国人群中进行的Ⅲ期研究,能够有效地提供中国患者的临床数据,相信临床研究结果能够更好地指导中国肺癌临床实践。
结果表明,与厄洛替尼单药治疗相比,贝伐珠单抗联合厄洛替尼治疗能够显著地延长患者的PFS期,中位PFS期(ITT,IRC)为17.9个月对11.2个月[风险比(HR)=0.55,95%可信区间(CI)为0.41~0.73],P< 0.001(图1)。
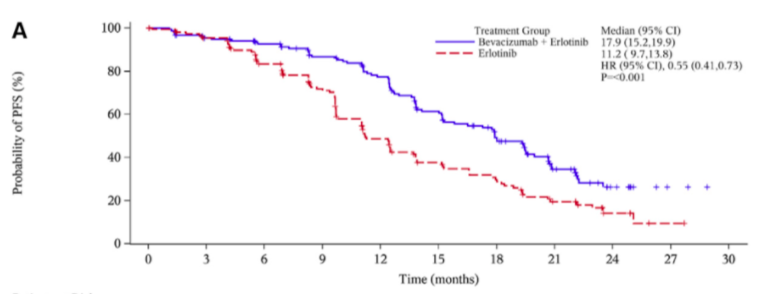
图1 两组患者PFS期的KM曲线
其中值得注意的是,21外显子L858R点突变的患者在联合治疗中的获益大于厄洛替尼单药治疗组,同时其获益程度也超过19外显子缺失突变患者从联合治疗中的获益(图2~图3);在基线时存在脑转移的患者中,厄洛替尼和贝伐珠单抗联合治疗也显著延长了PFS期,总生存期(OS)也有延长趋势。

图2 19外显子缺失突变的两组患者的KM曲线
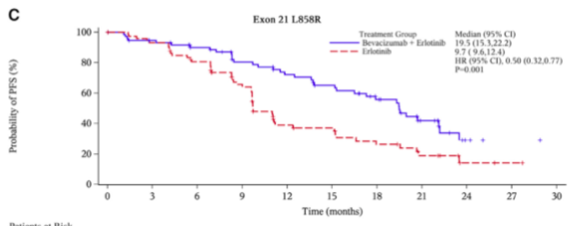
图3 21外显子L858R点突变的两组患者的KM曲线
研究证实了贝伐珠单抗联合厄洛替尼在EGFR突变的中国晚期NSCLC患者中,具有显著的临床获益和可控的安全性风险。“由此,贝伐珠单抗联合厄洛替尼可作为晚期、转移性或复发的EGFR突变阳性NSCLC患者的一线治疗选择。”吴一龙教授充满希望地指出。
一波三折,团队为了保障研究影响力越挫越勇
谈到研究背后的故事,吴一龙教授讲述了研究自2015年启动至今,经历的各种“波折”。
本研究在2015年设计、启动的时候,同期日本学者也设计、启动了一个探讨同样问题、相同思路的Ⅲ期临床试验。吴一龙教授略感遗憾的讲道:“尽管我们尽全力追赶研究启动时因克服多重困难落后的进度,日本研究仍然在我们的数据还没有成熟的时候抢先在2018年6月召开的美国临床肿瘤学会(ASCO)大会上公布了结果,成了全世界首个厄洛替尼联合贝伐珠单抗对比厄洛替尼单药的Ⅲ期临床试验。”
随后,ARTEMIS-CTONG1509研究数据在2018年底基本成熟后,也通过研究团队与多家支持方在不到3个月的时间内、以几乎无法复制的速度,赶上了2019年美国临床肿瘤学会(ASCO)投稿的最后一班车,但遗憾的是,由于本研究主要数据跟日本研究结果高度一致,ASCO并没有把本研究选为大会口头报告(oral)。
于是,吴一龙教授带领团队做了一个重要决定——撤稿,继续深入挖掘本研究的临床数据特色。团队很快补充了转化性研究结果,随即转战2019年欧洲肿瘤内科学会(ESMO)年会,终于被ESMO选为大会oral,由周清教授代表研究团队在大会中发布了中国研究的临床数据特色以及转化性研究成果,让中国研究闪亮登上ESMO的舞台,让中国之声唱响国际。
生物标志物探索性研究,让我们更加深入耐药机制与基因变化
聚焦本次公布的研究数据,其中也包括生物标志物方面的探索性研究数据。
研究团队通过对治疗前组织、血液、以及治疗后血液动态监测显示,两组患者基线突变谱相似,在进展时都出现了包括EGFR T790M,致癌基因的融合、扩增,MAPK/PI3K通路以及细胞周期通路的基因变异。在联合组中,52%的患者存在未知的耐药机制,而单药组中这一比例为36%。
EGFR突变的动态变化在两组中表现出相似的模式。与基线相比,两组首次随访时,EGFR敏感变异突变比例均有所下降,突变清除率也非常相似;而在进展时,两组的EGFR敏感变异突变比例和丰度均有所上升。数据也表明,在EGFR TKI治疗过程中,无论是否联合贝伐珠单抗,都不会改变EGFR突变的分子动力学变化。
回顾过去,吴一龙教授明确表示,肺癌是严重威胁生命健康的疾病,我国学者通过不懈努力在过去的20年里取得了较大的进步,患者的生存期和生活质量都得到了大幅改善。但不可否认的是,当前仍然有很多难题摆在临床学者面前,患者仍存在巨大的未被满足的治疗需求。
展望未来,我们将继续致力于新靶点探索、新药研发、新模式建立、难点热点问题攻关等,重点在于以生物标志物指导下的肺癌精准治疗和免疫治疗,以期实现将肺癌变成一个慢性病的目标,为我国肺癌患者带来更多获益。
本研究全国Leading PI吴一龙教授

吴一龙教授
肿瘤学教授,博士生导师,IASLC杰出科学奖获得者
2018-2020年临床医学领域全球高被引科学家
2020年世界肺癌大会(WCLC )主席
广东省人民医院(GDPH)终身主任
广东省肺癌研究所(GLCI)名誉所长
广东省肺癌转化医学重点实验室主任
吴阶平基金会肿瘤医学部会长
中国医师协会精准医学专委会副主任委员
广东省临床试验协会(GACT)会长
中国胸部肿瘤研究协作组(CTONG)主席
广东省医学会肺部肿瘤学会主任委员
中国临床肿瘤学会前任理事长,现指导委员会主任委员
本研究牵头单位广东省人民医院PI周清教授

周清教授
肿瘤学博士,主任医师,博士研究生导师
广东省人民医院惠福分院院长
广东省肺癌研究所副所长
广东省肺癌转化医学重点实验室副主任
广东省人民医院肿瘤中心肺三科主任
国际肺癌协会(IASLC)国际事务委员会(International Affairs Committee)委员
中国临床肿瘤学会(CSCO)副秘书长
广东省临床试验协会(GACT)/中国胸部肿瘤研究协作组(CTONG)副会长兼秘书长
中国抗癌协会第一届国际医疗交流分会副主任委员
中国女医师协会第二届临床肿瘤专业委员会副主任委员
广东省女医师协会肺癌专业委员会主任委员
广东省基层医药学会肺癌专委会主任委员
广东省临床试验协会/中国胸部肿瘤研究协作组(Chinese Thoracic Oncology Group, CTONG)
广东省临床试验协会/中国胸部肿瘤研究协作组(Chinese Thoracic Oncology Group, CTONG)成立于2007年,目前有41家成员单位,都是在中国肺癌临床研究领域十分优秀的医疗单位,还有40多家医疗单位作为参加单位参加了CTONG发起的临床试验。
自成立以来,CTONG开展了65项国内多中心临床试验,多项研究成果发表在《临床肿瘤学杂志》(Journal of Clinical Oncology)、《柳叶刀肿瘤学》(Lancet Oncology)杂志、《柳叶刀呼吸医学》(Lancet Respiratory Medicine)杂志、《胸部肿瘤学杂志》(Journal of Thoracic Oncology)等。部分研究成果被写入国际、国内肺癌指南。例如围术期靶向治疗策略、脑转移治疗策略等。
本次发表的ARTEMIS-CTONG1509研究是CTONG在2015年启动的国内多中心临床试验,研究结果被2019年ESMO年会选做大会的oral,并被写入中国临床肿瘤学会(CSCO)《原发性肺癌诊疗指南》(2020年版)当中。
广东省人民医院 周清教授审核
中国医学论坛报 刘芊整理
查看更多