查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






上期答疑
如患者一旦发生腹膜透析相关性腹膜炎,要尽可能保留透析导管吗?
参考答案:
腹膜透析相关性腹膜炎的治疗目的应该是迅速控制感染以及保护腹膜功能,而不是挽救腹膜透析导管。如出现抗感染治疗效果不佳,要尽早拔出腹膜透析导管。
点击回顾:
撰稿专家
叶星华
首都医科大学附属北京朝阳医院急诊科
一
概述

腹腔感染是指腹腔内部发生的感染性疾病[1]。腹腔是指位于腹部的腔隙,包括胃、肠、肝、胆囊、脾、胰腺等器官。腹腔感染可以是细菌、病毒、真菌或寄生虫等病原体引起的感染。
脓毒症(sepsis)是指机体对感染反应失调而导致的危及生命的器官功能障碍,其可导致脓毒性休克或多器官功能障碍[2]。脓毒症是急诊常见的急危重症,其病死率可高达40%[3]。脓毒症可发展为严重脓毒症(severe sepsis)和脓毒症休克(septic shock),可导致器官功能不全及循环障碍,病死率高[4-5]。脓毒症可以由任何部位的感染引起,而腹腔感染是临床常见的感染部位之一。
二
病因与发病机制

腹腔感染导致脓毒症/脓毒症休克的病因可以有很多种,如手术后感染、腹腔器官穿孔、腹腔脓肿等。常见的腹腔感染疾病包括腹膜炎、阑尾炎、胆囊炎、胰腺炎等。
脓毒症的危险因素包括以下几个方面:年纪(年幼或高龄)、免疫系统受损、糖尿病或肝硬化病史、长期于重症监护室治疗、创伤、侵入性治疗(例如静脉内导管或气管插管)、长期服用糖皮质激素等。
脓毒症的根本发病机制尚未明了,涉及到复杂的全身炎症网络效应、基因多态性、免疫功能障碍、凝血功能异常、组织损伤以及宿主对不同感染病原微生物及其毒素的异常反应等多个方面,与机体多系统、多器官病理生理改变密切相关,脓毒症的发病机制仍需进一步阐明。
2.2.1 细菌内毒素:研究表明细菌的内毒素可以诱发脓毒症,脓毒症病理生理过程中出现的失控的炎性反应、免疫功能紊乱、高代谢状态及多器官功能损害均可由内毒素直接或间接触发[6]。
2.2.2 炎症介质:脓毒症中感染因素激活机体单核巨噬细胞系统及其他炎症反应细胞,产生并释放大量炎性介质。脓毒症时,内源性炎性介质,包括血管活性物质、细胞因子、趋化因子、氧自由基、急性期反应物质、生物活性脂质、血浆酶系统产物及血纤维蛋白溶解途径等相互作用形成网络效应并引起全身各系统、器官的广泛损伤。同时某些细胞因子,如肿瘤坏死因子(TNF)-α等可能在脓毒症的发生、发展中起到重要作用[7]。
2.2.3 免疫功能紊乱:脓毒症免疫障碍特征主要为丧失迟发性过敏反应、不能清除病原体、易感医源性感染。脓毒症免疫功能紊乱的机制,一方面是作为免疫系统的重要调节细胞T细胞功能失调,炎症介质向抗炎反应漂移,致炎因子减少,抗炎因子增多;另一方面则表现为免疫麻痹,即细胞凋亡与免疫无反应性,T细胞对特异性抗原刺激不发生反应性增殖或分泌细胞因子[8]。
2.2.4 肠道细菌/内毒素移位:20世纪80年代以来,人们注意到应激发生时导致的机体最大的细菌及内毒素储存库-肠道发生功能失调,进而引起的肠道细菌/内毒素移位所致感染与随后发生的脓毒症及多器官功能不全密切相关[9]。研究表明,严重损伤后的应激反应可造成肠黏膜屏障破坏,肠道菌群生态失调及机体免疫功能下降,从而发生肠道细菌/内毒素移位,触发机体过度炎症反应与器官功能损害[10]。
2.2.5 凝血功能紊乱:凝血系统在脓毒症的发病过程中起着重要作用,它与炎症反应相互促进、共同构成脓毒症发生、发展中的关键因素。内毒素和TNF通过诱发巨噬细胞和内皮细胞释放组织因子,可激活外源性凝血途径,被内毒素激活的凝血因子XII也可进一步激活内源性凝血途径,最终导致弥漫性血管内凝血(DIC)[11-12]。
2.2.6 基因多态性:临床上常见受到同一致病菌感染的不同个体的临床表现和预后截然不同,提示基因多态性等遗传因素也是影响人体对应激打击易感性与耐受性、临床表现多样性及药物治疗反应差异性的重要因素[13-16]。
三
临床表现及分型

3.1.1 腹腔感染的临床表现
由于感染的部位及发展过程不同,腹腔感染的临床表现各不相同。典型的临床表现是发热、呕吐、腹痛、腹泻、腹部压痛及反跳痛,腹肌紧张,腹腔引流物为脓性等。由特定部位疾病所引起的腹腔感染常产生特有的征象:如憩室炎患者常有左下腹部疼痛及便秘,发热和白细胞增多,有时可触及包块;阑尾炎的典型症状为脐周或上腹部疼痛,且常为绞痛,疼痛转移到右下腹;如果阑尾穿孔形成弥漫性腹膜炎,则有腹膜炎表现。
3.1.2 脓毒症的临床表现
患者常存在明确或可疑的感染,并具备如下表现:
① 寒战、发热(体温>38.3 ℃),或低体温(体温<36 ℃);
② 心率>90次/min,或大于不同年龄正常值的两个标准差;
③ 气促,呼吸>20次/分或过度通气,动脉血二氧化碳分压(PaCO2)<32mmHg;
④ 精神状态的改变;
⑤ 明显水肿或液体正平衡(24小时超过20 ml/kg);
⑥ 高血糖症且无糖尿病史。
严重脓毒症的临床表现除了上述的脓毒症症状,还伴有由其导致的器官功能障碍(如心血管、肺、脑和肾的功能障碍)及组织灌注不足。常伴有低血压、乳酸酸中毒、少尿、急性意识状态改变等。
脓毒性休克的临床表现为出现脓毒症症状并伴有由其所致的低血压,虽经液体治疗仍无法逆转。主要表现为意识障碍(如焦虑不安、反应迟钝或神志不清)、脉搏细速、四肢湿冷、少尿或无尿等。
炎症反应指标:
① 白细胞增多:白血胞(WBC)>12000/μl;
② 白细胞减少:WBC<4000/μl;
③ WBC正常但幼稚白细胞总数超过10% ;
④ 血浆C反应蛋白>正常两个标准差;
⑤ 血浆降钙素原>正常两个标准差。
腹水检查
① 腹水常规:腹水的颜色对疾病的诊断有一定的意义,渗出物多为浅黄色薄层,由于病因不同,渗出物颜色也不同。血性腹水多见于恶性肿瘤,乳糜性腹水多见于淋巴系统疾病。
② 腹水生化:蛋白质的含量是鉴别渗出物和漏出物的关键。一般认为腹水或血清蛋白比小于0.5的主要是漏出物,大于0.5的主要是渗出物。
③ 腹水细胞:一般情况下,漏出液中的细胞数量小于100×10^6/L,主要是淋巴细胞和间皮细胞。
④ 腹水中肿瘤标记水平:由于CA-125可由肿瘤细胞分泌,其在腹水中的水平大多能提示肿瘤。血液中CA-199、CEA和其他肿瘤标志物也有类似的意义。
⑤ 腹水细菌培养:明确感染病原菌,并通过药敏结果指导临床抗生素的使用。
影像学检查
① 腹部X线及CT:明确感染灶的部位、毗邻脏器的相关变化,甚至是肠壁的炎症、水肿,膈上、膈下的积液或积气。
② 腹部B超:明确感染灶的不问,可以探测脓肿,也便于床旁检查,引导脓肿的穿刺引流。
器官功能障碍指标:
① 低氧血症:动脉血氧分压(PaO2)/吸氧浓度(FiO2)<300 mmHg;
② 急性少尿:即使给予足够的液体复苏,仍然尿量较少;
③ 血肌酐>44.2 μmol/L(0.5 mg/dl);
④ 凝血功能异常;
⑤ 肠梗阻:肠鸣音消失;
⑥ 血小板减少:血小板(PLT)<10000/μl;
⑦ 高胆红素血症。
组织灌注指标:
② 毛细血管再灌注能力降低或瘀斑形成。
对于感染或疑似感染的患者,当脓毒症相关序贯器官衰竭[sequential(Sepsis-related)Organ Failure Assessmengt,SOFA]评分较基线上升≥2分可诊断为脓毒症。SOFA评分标准如下:
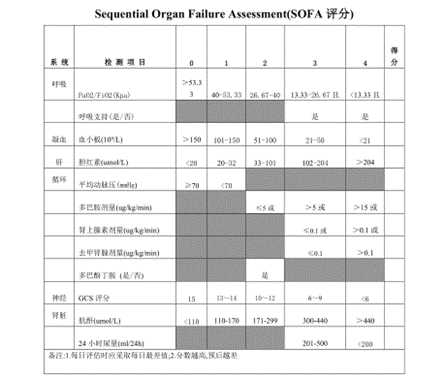
由于SOFA评分操作起来比较复杂,临床上常使用床旁快速SOFA(quick SOFA,qSOFA)标准识别重症患者,如果符合qSOFA标准中的至少2项时,再结合脏器功能障碍评定结果,初步判断脓毒症情况。qSOFA标准如下:
① 呼吸频率≥22次/分
② 意识改变
③ 收缩压≤100 mmHg
严重脓毒症和脓毒性休克诊断标准
脓毒症伴由其导致的器官功能障碍和/或组织灌注不足,下述任意一项:
① 体征及临床症状
脓毒症所致低血压;
即使给予足够的液体复苏,尿量仍<0.5 ml/(kg·h)至少2小时;
非肺炎所致的急性肺损伤且PaO2/FiO2<250 mmHg;
肺炎所致急性肺损伤且PaO2/FiO2<200 mmHg;
② 实验室检查
乳酸大于正常值;
血肌酐<176.8 μmol/L(2.0 mg/dl);
胆红素<34.2 μmol/L(2 mg/dl);
PLT<100000μl;
凝血障碍(国际标准化比值>1.5)。
四
治疗

在脓毒症中由于血管收缩舒张功能异常和通透性增加,机体在早期就出现了血容量降低,组织器官出现低灌注状态,因此及时进行有效液体复苏成为脓毒症治疗的关键措施。
4.2.1 获取生物学证据
尽可能在使用抗生素之前留取生物学标本,进行细菌/真菌培养,标本包括血液、痰液、尿液、腹水、伤口分泌物等标本,培养结果有助于进行针对性的使用抗生素治疗。但并非脓毒症所有的生物学标本培养都会有阳性结果。
4.2.2 使用抗生素
由于早期不可能很快获得细菌培养的结果,因此脓毒症早期应尽快给予经验性抗生素治疗。一旦获得细菌培养结果,应根据药敏结果结合临床情况尽快改为靶向治疗,使用有效的窄谱抗生素。合理进行经验性抗生素治疗和靶向治疗,是避免抗生素滥用和发生抗生素耐药的重要措施。
4.2.3 祛除感染源
在脓毒症治疗的同时,即应该积极寻找引起感染的原因,如涉及外科感染(如化脓性胆管炎、脓肿形成、肠梗阻、化脓性阑尾炎等),应及时手术干预,清除病灶或进行引流;如为医源性材料感染(如静脉导管、导尿管或植入人工器材等)应及时取出材料并作微生物培养。
血管活性药物的应用最好在便于进行血流动力学监测的ICU内进行。
严重脓毒症和脓毒症患者往往存在肾上腺皮质功能不全,因此对于经液体复苏后仍需给予升压药物维持血压的患者,可以考虑给予小剂量的糖皮质激素治疗,通常选择氢化可的松,每日剂量在200-300 mg范围。
对严重脓毒症患者在出现急性肺损伤/急性呼吸窘迫综合征(ALI/ARDS)时,应及时进行机械通气治疗以缓解组织缺氧状态,并且建议选择低平台压、小潮气量通气、允许性高碳酸血症的保护性肺通气策略。
脓毒症患者存在胰岛素抵抗情况,而循证医学证实脓毒症患者的血糖过高是其不良预后的危险因素,因此应把脓毒症患者的血糖应控制在合理的水平(<8.3 mmol/L),但同时应注意防止患者发生低血糖,因此应加强血糖监测。
对于出现脏器功能衰竭的脓毒性休克患者,除外出血风险等禁忌后,可以给予rhAPC,但同时应密切监测其凝血功能状态。由于后期的大型临床对照研究未能再次证实rhAPC的疗效,目前rhAPC的应用尚存争议。此外,可给予适当镇静,加强肾脏、肝脏等脏器支持,防止出现应激性溃疡、深静脉血栓、DIC等并发症等治疗。
五
预防

治疗和预防脓毒症最有效的方法是以脓毒症的发病机制为基础进行治疗和预防,但是遗憾的是目前脓毒症的发病机制仍未完全阐明,在这种情况下,针对发病原因应做好临床各方面的预防工作,努力降低诱发感染的危险因素对脓毒症的治疗和预防有着重要作用。随着医学研究的进步,大样本、多中心的临床随机对照研究会给脓毒症的治疗带来更多的循证医学证据,未来脓毒症机制的阐明一定会为脓毒症的治疗和预防带来新的希望。
六
总结

脓毒症病情凶险,病死率高,大约有9%的脓毒症患者会发生脓毒性休克和多器官功能不全,重症监护室中一半以上的死亡是由脓毒性休克和多器官功能不全引起的,脓毒症成为重症监护病房内非心脏病人死亡的主要原因。研究表明,出现脏器器官衰竭、休克、多重感染、严重的潜在疾病的患者预后较差。


未经许可,禁止转载
往期推荐
查看更多