查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





刚刚结束的2024WCLC大会上,肺NEC领域有哪些新进展?


NEC是一类侵袭性极强的异质性肿瘤,属于神经内分泌肿瘤(NEN)家族,可发生于多种器官,肺部是最常见的原发器官[1]。肺NEC主要分为肺大细胞神经内分泌癌(LCNEC-L)和小细胞肺癌(SCLC)。其中,SCLC是肺NEC中最常见的类型,占所有原发性肺癌的15%-20%,5年总生存(OS)率不足15%[2];而LCNEC-L极为罕见,仅占所有原发性肺癌的2%-3%,平均5年OS率约为35%[2];且对于广泛期SCLC和晚期转移性LCNEC-L患者,5年OS率进一步降低至 0-5%[3,4],预后亟需改善。
随着精准医学的持续发展,关键分子靶点的发现及相应新药物的开发为肺NEC的诊治管理带来了新希望。刚刚结束的2024 世界肺癌大会(WCLC)公布了肺神经内分泌癌(NEC)领域的诸多进展,以T细胞衔接器、抗体药物偶联物(ADC)为代表的新药不断在肺NEC治疗中传来捷报,为肺NEC领域带来了最前沿的诊疗和研究进展“盛宴”。
大放异彩:T细胞衔接器药物精准靶向DLL3靶点,展现肺NEC治疗潜能
➤ DeLLphi-301:Tarlatamab治疗既往经治SCLC的长期随访数据 [5]
Tarlatamab是一种能够同时结合DLL3/CD3的T细胞衔接器,DeLLphi-301是一项2期、开放标签研究,探索了Tarlatamab治疗既往经治SCLC的疗效和安全性。本次WCLC公布了DeLLphi-301研究长期随访数据。
研究结果显示,在Tarlatamab 10 mg组(n=100),既往经治SCLC患者中位PFS为4.3个月,中位OS为15.2个月,OS数据在铂敏感和铂耐药人群之间较为相似。长期耐受性良好,16%患者因治疗相关AE(TRAE)中断给药,4%患者因TRAE停药[4],长期随访中未显示出新的安全性信号。
图1. Tarlatamab治疗SCLC的OS结果
➤ DeLLphi-301:Tarlatamab治疗既往经治SCLC的长期随访数据 [5]
Obrixtamig(BI 764532)是一种新型IgG样T细胞衔接器,通过同时结合T细胞上的CD3和肿瘤细胞上的DLL3发挥抗肿瘤作用。NCT04429087是Obrixtamig开展的一项正在进行的I期首次人体、开放标签、剂量递增临床试验,用于治疗局部晚期/转移性DLL3表达阳性的SCLC、LCNEC-L或epNEC,本次WCLC大会主要报告了LCNEC-L人群的更新数据。
数据截止至2024年2月21日,共纳入168例患者,其中10例LCNEC-L患者接受≥90μg/kg有效剂量组治疗可评估,客观缓解率(ORR)和疾病控制率(DCR)分别达到70%和90%。数据截止时,7例应答患者中有5例(71%)仍在接受治疗,应答持续时间(DoR)数据暂未成熟。
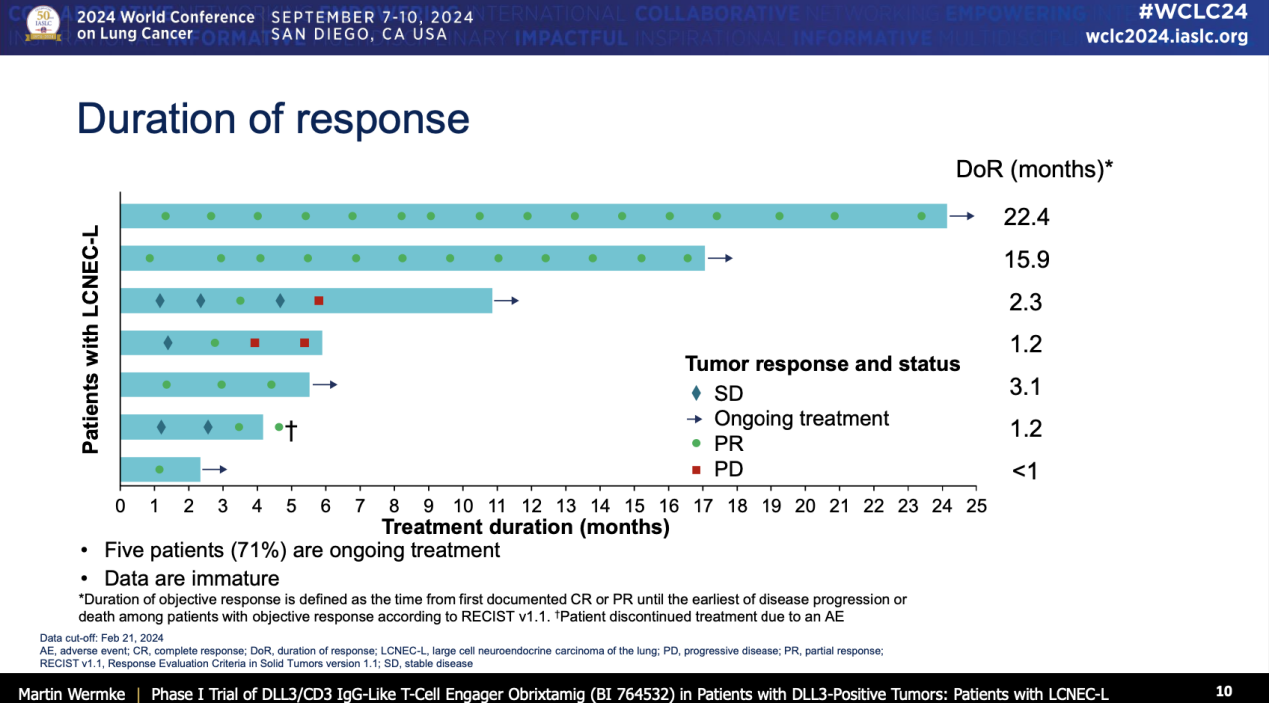
值得注意的是,案例报告显示,一例59岁女性LCNEC-L患者经Obrixtamig治疗的缓解持续时间(DoR)达到22.1个月,目前治疗仍在进行中。
图3. BI 764532治疗LCNEC-L的个案报告结果
安全性方面,LCNEC-L患者未出现剂量限制性毒性(DLT),不良事件(AE)发生情况与总人群一致;且未达到最大耐受剂量(MTD)。
➤ HPN328-4001:脑转移对靶向DLL3的T细胞衔接器MK-6070治疗SCLC安全性和疗效的影响[7]
HPN328-4001是一项正在进行中的 1/2 期临床研究,探索了DLL3/CD3 T细胞衔接器 MK-6070治疗既往经治SCLC患者的疗效和安全性。此次大会更新了患者基线脑转移情况对MK-6070安全性和疗效的影响。
结果显示,在≥1.215 mg有效剂量组,MK-6070在有脑转移病史患者(n=28)及无脑转移病史患者(n=24)中均展示出较好的抗肿瘤活性。与无脑转移患者相比,有脑转移患者展现出更高的ORR(36% vs 18%)、颅外(EC)-ORR(50% vs 18%)、DCR(64% vs 50%)。CNS进展事件仅在有脑转移病史患者中观察到。安全性特征在两组患者之间没有明显差异,TRAE发生率接近(93% vs 100%),免疫效应细胞相关神经毒性综合征(ICANS)发生率在有脑转移病史患者中略高(11% vs 4%)。
图4. MK-6070治疗SCLC的疗效
百家争鸣:ADC药物蓬勃发展,为肺NEC治疗带来更多选择
➤ Ideate-lung 01:Ifinatamab deruxtecan(I-DXd)治疗广泛期SCLC(ES-SCLC)[8]
I-DXd是一种靶向B7-H3的ADC药物,Ideate-lung01是一项2期研究,探索了12 mg/kg vs 8mg/kg剂量I-DXd治疗既往经治ES-SCLC患者的疗效和安全性,此次大会公布了研究中期分析结果。
结果显示,12 mg/kg剂量组展现出优于8mg/kg剂量组的疗效数据,在12 mg/kg剂量组(n=42),ORR为54.8%;中位DOR为7.9个月;中位PFS为5.5个月;中位OS为11.8个月。两个剂量组均在基线伴脑转移患者中展现出较好的颅内缓解率。安全性方面,12 mg/kg剂量组报告的TEAE发生率高于8 mg/kg剂量组,最常见的不良反应包括胃肠道症状及血液毒性,报告的药物相关ILD多为1-2级。
图5.I-DXd治疗ES-SCLC的疗效
➤ARTEMIS-001:HS-20093治疗ES-SCLC的疗效和安全性[9]
HS-20093是一种靶向B7-H3的ADC药物,ARTEMIS-001 研究是一项多中心、开放标签的I期研究,旨在研究 8.0mg/kg vs 10.0mg/kg的HS-20093(GSK5764227)在晚期实体瘤中的安全性和有效性,本次WCLC大会报告了ES-SCLC队列的数据。
结果显示,8.0 mg/kg (n=31) vs 10mg/kg(n=25)剂量下,患者的ORR分别为 61.3% vs 50.0%;DCR分别为80.6% vs 95.5%;中位DoR分别6.4 vs 8.9个月;中位PFS分别为5.9 vs 7.3个月;中位OS分别为9.8个月 vs 未达到。B7-H3表达情况与ORR之间暂未观察到关联性。安全性结果与既往报告相一致,8.0 mg/kg剂量组展现出更轻微的血液学毒性。
图6. HS-20093治疗SCLC的疗效
➤ TROPiCS-03:Sacituzumab govitecan(SG)二线治疗ES-SCLC[10]
Sacituzumab govitecan(SG)是一种针对Trop-2靶点的ADC药物,TROPiCS-03(NCT03964727)研究是一项开放标签、多队列、II期试验,旨在验证SG在转移性或局部晚期实体瘤中的疗效。本次WCLC大会报告了ES-SCLC队列纳入更多患者并进行更长时间随访的最新结果。
数据截止至2024年3月8日,中位随访时间为12.3个月。43例ES-SCLC患者接受SG二线治疗的ORR为41.9%;中位DOR为4.7个月(95%CI:3.5-6.7);中位PFS为4.40个月(95%CI:3.81-6.11);中位OS为13.60个月(95%CI:6.57-14.78)。铂耐药 vs 铂敏感患者的ORR分别为35.0%和47.8%。100%患者发生了任何级别的TRAE,其中74.4%为≥3级,未发生TRAE导致研究治疗停止。
图7. SG治疗ES-SCLC的疗效
➤ NCT05154604:SHR-A1921治疗晚期SCLC[11]
SHR-A1921是一种靶向Trop-2的ADC药物,NCT05154604研究是一项首次在人体进行的、包括剂量逐步增加、剂量逐步扩展和有效性逐步扩展的I期临床试验,旨在探索SHR-A1921治疗ES-SCLC的疗效和安全性。
截至2024年2月19日,中位随访5.3个月,17例ES-SCLC患者接受SHR-A1921治疗的ORR为33.3%,DCR为66.7%,中位DoR为4.4个月,中位PFS为3.8个月。同时,SHR-A1921安全性良好,35.3%的患者发生了3-4级TRAE,无患者因TRAE导致治疗中止或死亡。
图8. SHR-A1921治疗ES-SCLC的疗效
专家点评
肺NEC(如SCLC和LCNEC-L)是一种侵袭性较强、进展迅速,预后差且易复发的恶性肿瘤,既往治疗方案有限。SCLC一线标准治疗目前以EP联合免疫治疗为主,二线及以后以化疗、抗血管生成TKI、免疫治疗为主;而LCNEC-L一线标准治疗以EP化疗为主,二线及以后治疗选择十分有限(以化疗为主)[12,13]。近年来,随着肺NEC疾病认识的不断深入,以及治疗药物的持续研发,肺NEC的治疗取得了一定进展,如DLL3、TROP-2和B7H3等治疗靶点相继涌现,以T细胞衔接器、ADC为代表的创新药物有望打开新的治疗思路,为临床医生提供更多有效的治疗手段[5-11,14]。
结合本次WCLC大会所公布的最新研究进展,靶向DLL3靶点的T细胞衔接器类药物具有双重特异性,既能够同时与T细胞上的CD3复合物结合,也能与肿瘤上的DLL3靶抗原结合,在SCLC中均取得了非常亮眼的疗效数据。值得注意的是,DeLLphi系列研究结果提示,TcE在SCLC后线治疗的疗效似乎与化疗敏感或耐药无关[5],同时多款靶向DLL3的TcE在SCLC后线展现出可控的安全性,HPN328-4001研究显示对有脑转移的SCLC患者比无脑转移患者展现出更好的抗肿瘤效果,这些新药有望为SCLC伴或不伴脑转移患者带来了全新的治疗选择[14]。基于肺NEC的高度异质性,未来需进一步探索创新的联合治疗模式,对可能获益人群进行细分,开发出更多有效的靶点,建立全新治疗标准,重塑当前的治疗格局。
而ADC 作为一种精准化疗方案,兼具单抗的靶向性与化疗的有效性。目前我们已经看到靶向B7H3和TROP-2的多款ADC在小样本经治SCLC患者中展现出初步疗效。与当前SCLC的标准二线治疗方案相比,ADC药物的安全性良好,尤其是ILD的发生率较低[8],对于既往经治后进展的ES-SCLC患者,可能会是非常有前景的后线治疗药物,未来值得进行深入探索。
由于LCNEC-L相对罕见,大多数证据来自小型回顾性研究,其治疗策略参考SCLC和NSCLC,主要以含铂化疗为主,后线缺乏大型前瞻性RCT研究建立规范化治疗方案,存在着较大治疗需求空间[15]。令人欣喜的是,obrixtamig作为一款靶向DLL3的TcE 在LCENC-L中展现出了较佳的疗效和可控安全性,有个案显示持续缓解时间超过22月,为LCNEC-L的治疗指引了新的方向,带来了全新的治疗选择。期待未来Obrixtamig(BI 764532)能够在LCNEC-L中开展更多高质量、大样本量的临床研究,提供更多循证学依据,造福更多肺NEC患者。
未来随着更多新型药物的研发和探索,同时不断积累高级别循证医学证据,有望为晚期肺NEC患者带来更多治疗选择。

李艳 教授
主任医师,博士,博士后,硕士生导师;
重庆市中青年医学高端人才
重庆大学附属肿瘤医院1110计划高端后备人才
中国南方肿瘤协作组(CSWOG)结直肠癌青年委员会 委员
中国临床肿瘤学会(CSCO)胰腺癌专委会 委员
中国临床肿瘤学会(CSCO)中西医结合委员会 委员
重庆市医药生物技术协会罕见病和疑难病专委会 副主委
重庆市医药生物技术协会精准诊疗专委会 副主委
重庆市医药生物技术协会分子靶向治疗专委会 常务委员
重庆市抗癌协会分子靶向治疗专委会 委员
四川省国际医学交流促进会肿瘤分子靶向专委会 委员
近年来共发表SCI论文20余篇;主持和参与重庆市科委重点、面上项目、科卫联合高端人才项目、重庆市博士后特别资助项目、CSCO肿瘤研究基金共13余项;牵头撰写LCNEC诊治、肺癌化疗共识2部。
1.Sara Stumpo, et al. J Clin Med. 2023 Dec 15;12(24):7715.
2.Jessica F Williams, et al. Histopathology. 2022 Nov;81(5):556-568
3.Liling Huang, et al.. BMC Cancer. 2023 Apr 5;23(1):312.
4.Byers Lauren Averett, et al.Cancer, 2015, 121: 664-72.
5.Jacob Sands, et al.2024 WCLC.Abstract#OA10.03
6.Martin Wermke, et al.2024 WCLC.Abstract#OA10.05
7.Noura J, et al.2024 WCLC.Abstract#OA10.06
8.Charles M. Rudin, et al.2024 WCLC.Abstract#OA04.03
9.J. Wang, et al.2024 WCLC.Abstract#OA04.06
10.Afshin Dowlati, et al.2024 WCLC.Abstract#OA04.04
11.Jie Wang, et al.2024 WCLC.Abstract#OA04.05
12.Owonikoko, et al. J Thorac Oncol 2012
13.Alvarado-Luna and Morales-Espinosa. Transl Lung Cancer Res 2016
14.Rudin CM, et al. J Hematol Oncol. 2023; 16: 66.
Elisa Andrini , et al. J Clin Med. 2022 Mar 7;11(5):1461
文章审批号:SC-CN-15840
有效期至:10/9/2025
仅供相关医药专业人士进行医学科学交流
↓↓↓
查看更多