查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





一般资料:患者男性,41岁,于2020年7月就诊。
主诉:原发性肝癌介入治疗5个月后肝癌复发
现病史:患者2020年2月因“右上腹疼痛”就诊,查甲胎蛋白(AFP)>1210ng/ml,腹部CT示右肝肿瘤破裂出血,当地医院遂给予介入+射频消融治疗,术后规律复查,2020年7月28日复查腹部CT时发现肝癌复发。
既往史:乙肝病史,具体时间不详,未行药物治疗。
肿瘤标记物(2020年7月28日):AFP>60500ng/ml(↑)。
腹部增强CT(2020年7月28日):肝轮廓右侧不规则形稍低密度团块影,密度欠均,大小约16.3cm×7.4cm,如图1所示。
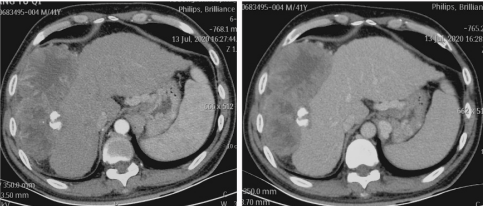
图1 治疗基线腹部CT影像(左右分别为动脉期及平扫影像)
临床诊断:1.原发性肝细胞肝癌,BCLC C期,CNLC Ⅲa期;2.慢性乙型病毒性肝炎。
治疗方案:患者肿瘤负荷较大,既往有肝肿瘤破裂病史,予患者仑伐替尼8mg QD治疗。
影像学及疗效评价:腹部CT(2020年8月25日):肝轮廓右侧不规则形稍低密度团块影,密度欠均,大小约18.0×8.1cm,如图2所示;AFP>60500ng/ml;考虑仑伐替尼单药效果不佳,肿瘤较前略增大。

图2 单药靶向治疗后腹部CT影像(左右分别为动脉期及平扫影像)
第二阶段治疗:替雷利珠单抗+靶向+局部放疗
治疗方案:予患者仑伐替尼8mg QD+替雷利珠单抗200mgQ3W+局部放疗(放射线:6MV-X线,处方剂量95%PGTV:30Gy/2Gy/15f,每天一次,每周五次)。
影像学及疗效评价:腹部CT(2020年12月):肝轮廓右侧占位,病变密度较前减低,大部液化,体积略小,如图3所示;AFP 479ng/ml;根据mRESCIT标准,影像学评估患者达到完全缓解(CR),可实现手术切除坏死病灶。
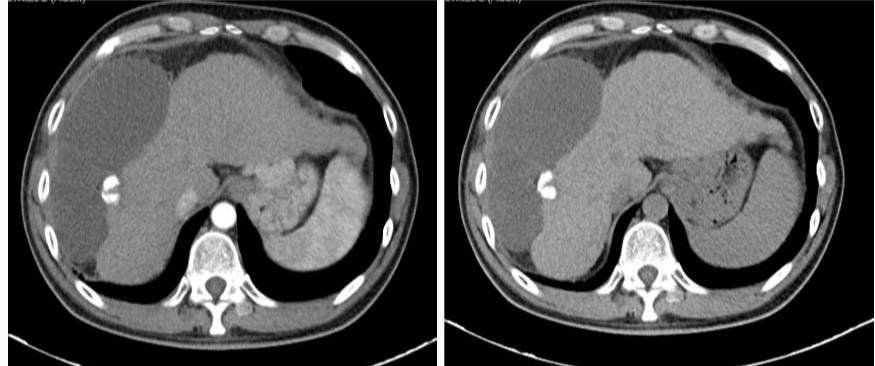
图3 联合治疗后腹部CT影像(左右分别为动脉期及平扫影像)
安全性评价:口服仑伐替尼后出现轻度腹泻、轻度手部皮疹,未见其余毒副反应。
本例患者中年男性,因“上腹部疼痛”就诊并确诊为原发性肝癌伴肿瘤破裂出血,经介入+射频消融治疗5个月后肝癌复发,表现为巨大复发性肝癌,结合既往病史及辅助检查结果,明确诊断为:1.原发性肝细胞肝癌,BCLC C期,CNLC Ⅲa期;2.慢性乙型病毒性肝炎。考虑患者肿瘤负荷巨大,肿瘤破裂引起肝外局限转移,直接手术切除很难完整切除,也基本无法保障切缘阴性,同时切面渗血风险较高,拟先行免疫治疗3.0治疗,降低肿瘤负荷,形成完整包膜,保障肿瘤可以完整切除后再行手术切除。患者一线接受单药靶向治疗后,病灶仍持续增大,故调整为免疫+靶向+局部放疗方案,患者4个月后病灶明显缩小,AFP明显下降,根据mRESCIT标准,影像学评估患者达到完全缓解(CR),成功实现肝癌降期转化。综合评估后,可实现手术切除坏死病灶。治疗过程AFP动态变化如图4所示。
图4 治疗期间AFP动态变化
我国是乙肝大国,也是肝癌高发国家,原发性肝癌患者占全世界50%以上,肝癌的发病率及死亡率均排在恶性肿瘤前列[4]。高发、难治是中国肝癌的突出特点。目前,手术治疗是早期肝癌的主要治疗方式,然而,绝大多数患者发现时就被诊断为不可切除或转移性肝癌,失去了根治性手术机会,治疗方式十分有限;另一方面,即便接受了手术治疗的患者,仍可能会出现疾病进展[5, 6]。正如本文分享的患者病例,患者初诊时已出现肿瘤破裂出血,当地医院评估后予患者应用了局部治疗,但患者仍在术后5个月即出现了巨大的复发病灶,针对该患者的后期治疗选择及预后均不容乐观,但这也是临床中无法忽视的肝癌治疗现状。
在过去两年时间里,肝癌的系统治疗发生了巨大的变化,新型治疗手段不断涌现、联合治疗逐渐取得突破、降期转化治疗使得更多晚期肝癌患者获得手术机会,继靶向治疗之后,以程序性死亡受体-1(PD-1)及其配体PD-L1的抗体为代表的免疫检查点抑制剂为进展期肝癌的二线治疗提供了新的方案[7]。但结合2019年CheckMate 459及KEYNOTE-240研究结果,PD-1抗体单药在肝癌的治疗价值仍然有限[8]。单一靶向治疗虽起效快,用药精准,但无法实现对肿瘤的广泛打击,临床表现为治疗起效时间短,临床获益窗口期短;而免疫单药治疗(以PD-1抗体为例),在肝细胞癌的客观有效率仅20%左右[9]。基础研究结果发现免疫与靶向治疗的联合,能更好地改善肿瘤患者的免疫微环境,激活CD8+ T细胞活性,两者联合的治疗优势在多项小样本临床研究中被报道[9-10]。在61名晚期肝细胞肝癌的研究中发现,免疫联合靶向治疗的客观缓解率(ORR)达44.8%,疾病控制率(DCR)达82%以上。
本例患者单药靶向治疗一个月后影像学提示肿瘤较前增大,肿瘤标志物未下降,提示该单药方案未能很好控制患者病情。结合上述研究,考虑到患者巨大肝癌病灶需及时得到控制,我们在此基础上,为患者加用了替雷利珠单抗及局部放疗,在治疗4个月后,根据mRESCIT评估标准,影像学评估达到CR,可以实现手术切除坏死病灶。
本例患者应用的替雷利珠单抗是我国百济神州自主研发且为目前唯一成功对Fc段进行特殊基因工程改造的PD-1单抗,在临床前研究中所显示,独特结构优化使之具有避免抗体依赖性细胞介导的吞噬作用(ADCP)、Fab段彻底持久阻断PD-1/PD-L1结合、半衰期长、抗肿瘤活性强等四大主要药学优势。这些优势是前期系列研究成功的基础,亦为未来探索更加广阔的临床应用前景提供了方向。
近期,替雷利珠单抗用于不可切除肝癌二线及以上治疗的全球、多中心、Ⅱ期临床研究——RATIONALE 208研究公布了最新数据,替雷利珠单抗单药方案在后线治疗中显示了可喜的有效性,中位OS达13.2个月,比肩国际同类药物既往数据。同时部分患者能够实现深度缓解,获得完全缓解(CR);近80%的疾病缓解患者PFS超过一年,提示患者人群一旦起效,则不易耐药,抗肿瘤作用稳定而持久。而基于RATIONALE 208研究结果,替雷利珠单抗已于2021年6月22日获得国家药品监督管理局(NMPA)批准用于至少经过一种全身治疗的肝细胞癌的治疗。
替雷利珠单抗在晚期肝癌领域的治疗探索还有更广泛的布局,其在单药一线治疗、联合靶向治疗等多领域的临床研究均在积极开展中,期待未来更多临床证据的积累,可以为晚期肝癌患者增加获益,描绘一个美好可期的未来。
参考文献:
[1]
[2] ZOU H, ZHU C Z, WANG C, et al. Recurrence of Barcelona Clinic Liver Cancer Stage A Hepatocellular Carcinoma After Hepatectomy [J]. Am J Med Sci, 2017, 354(3): 262-7.
[3] VIBERT E, SCHWARTZ M, OLTHOFF K M. Advances in resection and transplantation for hepatocellular carcinoma [J]. Journal of hepatology, 2020, 72(2): 262-76.
[4] 吴周姜丽, 李凯, 张楷, et al. 单独或联合免疫疗法治疗肝癌的研究进展[J ].中华肝脏病杂志 .Chinese Journal of Hepatology [J]. 2020, 28(6): 471-4.
[5] YAMASHITA T, KUDO M, IKEDA K, et al. REFLECT-a phase 3 trial comparing efficacy and safety of lenvatinib to sorafenib for the treatment of unresectable hepatocellular carcinoma: an analysis of Japanese subset [J]. Journal of gastroenterology, 2020, 55(1): 113-22.
[6] LLOVET J M, MONTAL R, SIA D, et al. Molecular therapies and precision medicine for hepatocellular carcinoma [J]. Nat Rev Clin Oncol, 2018, 15(10): 599-616.
[7] SIM H W, KNOX J. Hepatocellular carcinoma in the era of immunotherapy [J]. Curr Probl Cancer, 2018, 42(1): 40-8.
[8] FINN R S, RYOO B Y, MERLE P, et al. Pembrolizumab As Second-Line Therapy in Patients With Advanced Hepatocellular Carcinoma in KEYNOTE-240: A Randomized, Double-Blind, Phase III Trial [J]. Journal of Clinical Oncology, 2020, 38(3): 193-+.
[9] RODERBURG C, BERRES M L, WREE A, et al. Excellent Response to Anti-PD-1 Therapy in a Patient with Hepatocellular Carcinoma Intolerant to Sorafenib [J]. Visc Med, 2019, 35(1): 43-6.
[10] GE S, HUANG D. Systemic therapies for hepatocellular carcinoma [J]. Drug Discov Ther, 2015, 9(5): 352-62.

中国医学论坛报编辑|金金 整理
查看更多