查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





在精准医疗迅速发展的时代,NTRK基因融合作为一类重要的致癌驱动因素,备受临床关注。NTRK基因融合不局限于某些组织类型,在身体的各个部位都可能发生。NTRK基因融合一些最常见肿瘤类型(肺癌和肠癌等)中较为少见,发生率通常低于5%,而在少数罕见肿瘤(唾液腺癌和分泌性乳腺癌等)中频发(高于80%)[1]。针对NTRK融合的靶向药物研发进展迅速,拉罗替尼基于临床试验的积极结果写入国内外权威临床指南,并于2022年获得NMPA批准用于治疗NTRK基因融合的局部晚期或转移性实体瘤成人和儿童患者,为NTRK基因融合肿瘤患者带来了新的治疗选择。本文将结合今年的研究进展,分析拉罗替尼治疗NTRK基因融合肿瘤成人患者的最新临床数据,以期为临床实践提供更多参考依据。
大放异彩,NTRK基因融合肿瘤成人患者治疗进展
NTRK基因融合肿瘤成人患者数据

图1. 肿瘤缓解
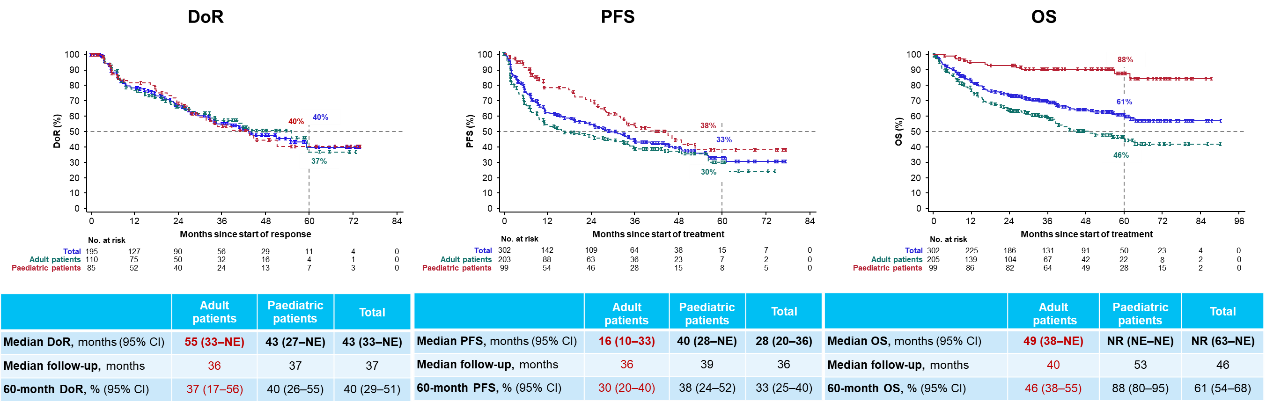
图2. DoR,PFS,OS
在2024 ESMO年会也报告了拉罗替尼作为一线治疗用于既往未接受系统治疗的局部晚期或转移性TRK融合肿瘤患者的最新疗效和安全性[3],在IRC可评估的59例成人患者中,拉罗替尼一线治疗的ORR达68% (95% CI:54-79),数据截止时,中位DoR为59个月,5年DoR率为34%;中位PFS为61个月,5年PFS率为56%;中位OS尚未达到,5年OS率为67%。在安全性方面,拉罗替尼治疗的不良事件是可控的,治疗相关不良事件(TRAEs)多为1/2级。随着随访时间的延长,拉罗替尼持续为患者提供快速且持久的缓解,延长生存获益,并保持良好的安全性,逐步为TRK融合肿瘤患者的治疗增加循证医学证据。
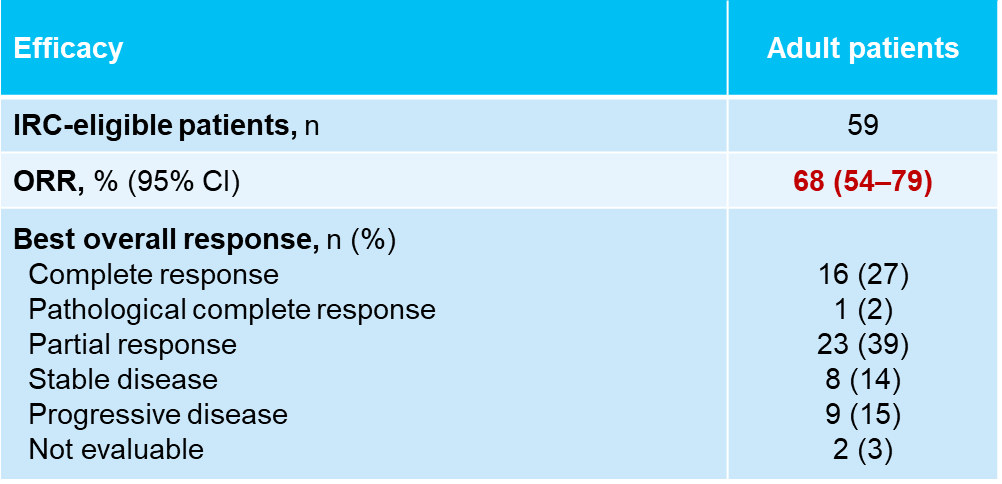
图3. 肿瘤缓解
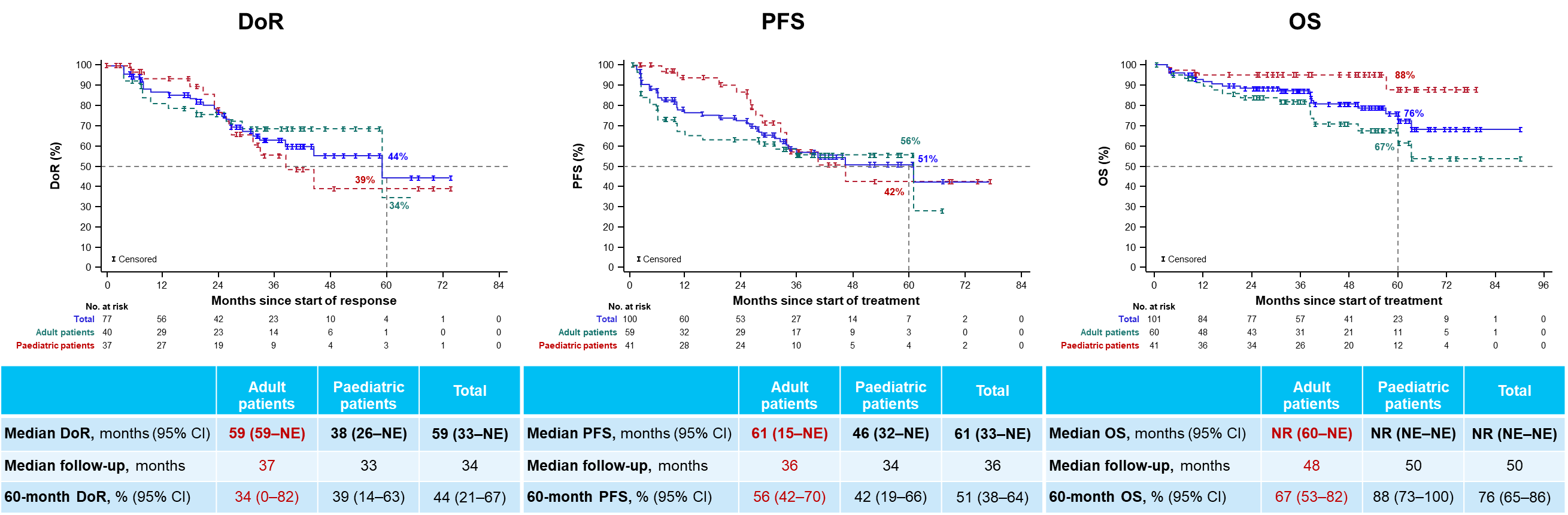
图4. DoR,PFS,OS
NTRK基因融合肺癌患者
肺癌是我国发病率和死亡率最高的恶性肿瘤[4],随着精准医疗的快速发展,在肺癌中发现了多种致癌驱动基因,其中NTRK基因融合已被确认为肺癌的重要致癌驱动因素。针对NTRK基因融合靶向药物的出现,为这类患者的临床诊疗带来了新的转机。2024 WCLC大会报告了拉罗替尼治疗TRK融合肺癌患者的最新结果[5] ,这项研究纳入了2项拉罗替尼关键试验(NCT02576431和NCT02122913)的数据,共32例NTRK融合阳性NSCLC患者,其中12例基线时伴中枢神经系统(CNS)转移,研究结果显示,接受拉罗替尼治疗的肺癌患者,中位至缓解时间仅为1.8个月(范围:1.5-7.3),IRC评估的ORR为66%,中位DoR为34个月,中位PFS为22个月,中位OS为39个月,进一步验证了拉罗替尼可为NTRK融合阳性肺癌患者带来的快速且持久的临床获益。此外,对于基线伴CNS转移的患者,IRC评估的ORR为67%(95% CI:35%-90%),与整体人群数据相当,证明了拉罗替尼出色的颅内疗效。
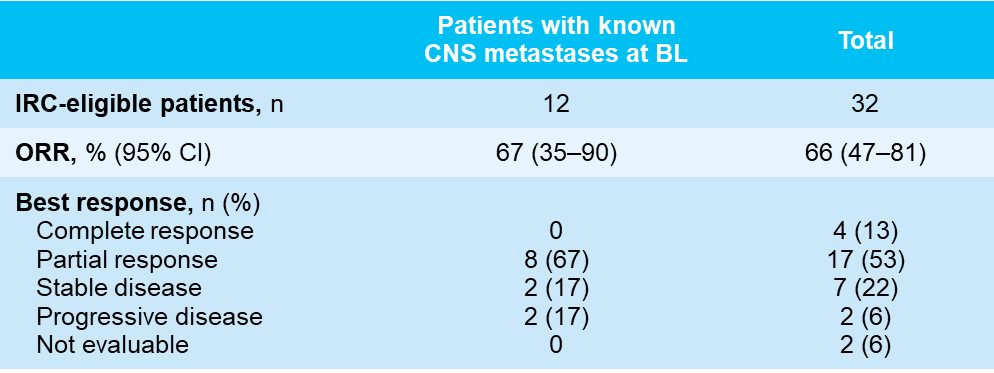
图5. 肿瘤缓解
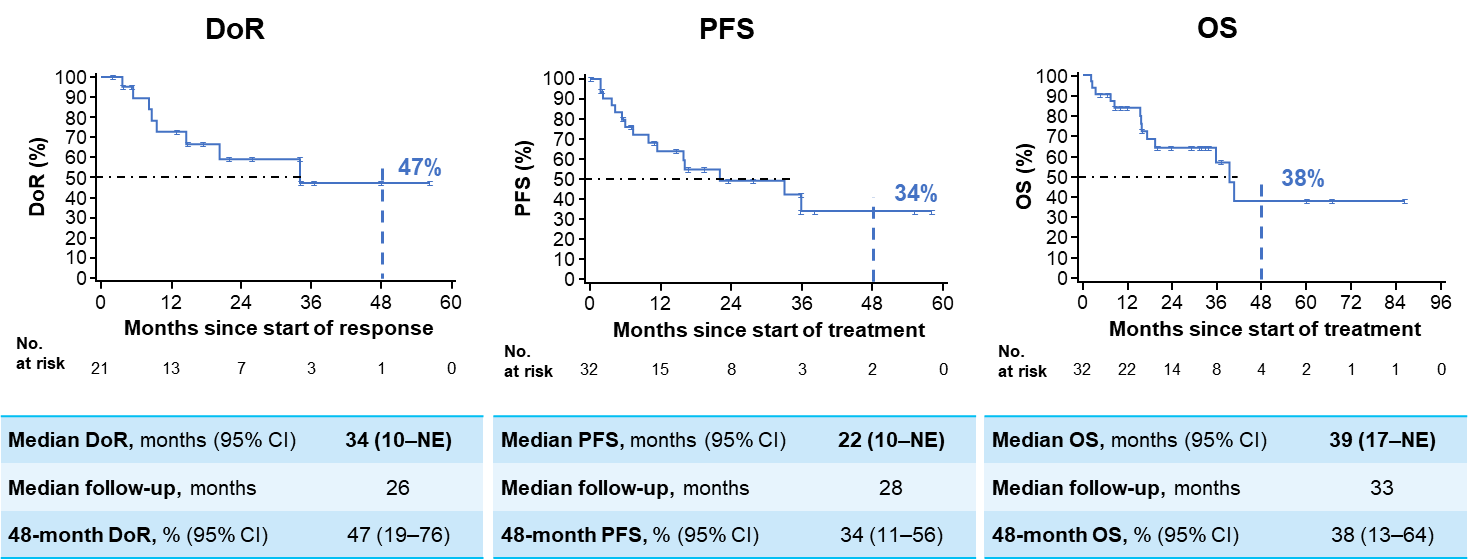
图6. DoR,PFS,OS
NTRK基因融合甲状腺癌患者
甲状腺癌(TC)已成为全球范围内增长迅速的疾病负担,其发病率近年来急剧上升。分化型甲状腺癌(DTC)约占TC患者的90%左右,放射性碘是转移性DTC的主要治疗手段之一,但仍有部分DTC患者为放射性碘难治性。TRK抑制剂拉罗替尼的出现,为TC患者提供了更多治疗选择。2024 ATA大会报告了拉罗替尼治疗TRK融合TC患者的疗效和安全性分析的更新结果[6],研究共纳入31例TRK融合TC患者进行IRC疗效评估分析,其中包括24例DTC患者和7例未分化型甲状腺癌(ATC)患者。在所有TC患者中,拉罗替尼治疗的中位至缓解时间为1.9个月(范围:1.6-16.2),ORR为65% (95%Cl:45-81),其中DTC和ATC患者的ORR分别为79%和14%。数据截止时,中位DoR为41个月,4年DoR率为32%;中位PFS为44个月,4年PFS率为42%;中位 OS尚未达到,4年OS率为72%。安全性分析显示,拉罗替尼治疗的TRAEs主要为1-2级,没有患者因TRAEs而停药。这些长期随访数据再次证明了拉罗替尼在兼顾疗效和安全性方面的可靠性。

图7. 肿瘤缓解
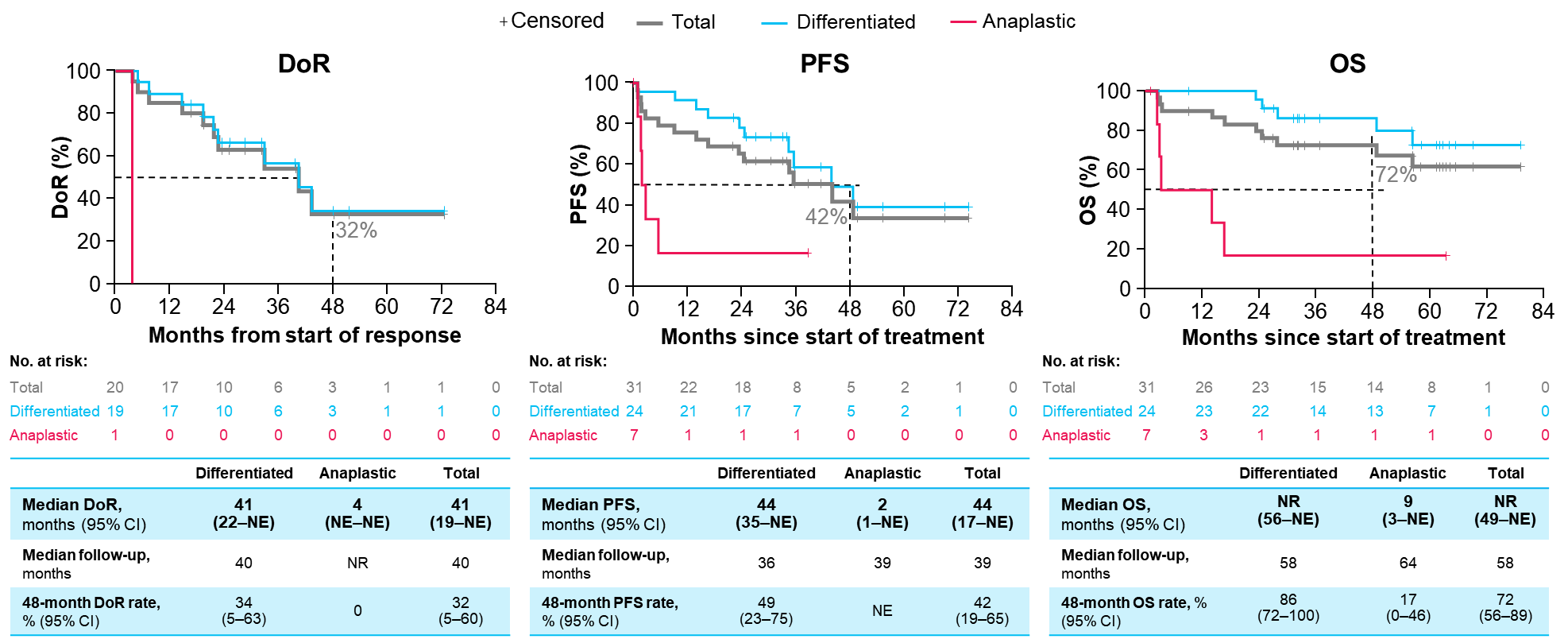
图8. DoR,PFS,OS
NTRK基因融合消化道肿瘤患者
消化道肿瘤是我国常见的恶性肿瘤之一,其中结直肠癌发病率最高,排在第二位。NTRK基因融合在消化道肿瘤中的总体发生率小于1%,但由于我国人口基数庞大,其病患总数仍不容小觑。既往研究数据已证实拉罗替尼在消化道肿瘤中的实力,在今年的ASCO GI大会上,报告了拉罗替尼治疗TRK融合胃肠道肿瘤患者的更新数据[7]。在最新的研究分析中,共纳入NAVIGATE(NCT02576531)研究中44例接受拉罗替尼治疗的转移性TRK融合胃肠道肿瘤患者,其中包括25例结直肠癌(CRC)患者。在所有IRC可评估患者中,拉罗替尼治疗的中位至缓解时间为1.8个月(范围:1.7-11.1),ORR为28%(95% Cl:15-44),其中CRC患者的ORR为44%(95% CI:24-63)。拉罗替尼治疗消化道肿瘤患者的中位DoR为27.3个月,中位PFS为6.1个月,中位OS为12.5个月,其中CRC患者的中位OS长达29.4个月。拉罗替尼治疗的大多数不良事件是可控的,TRAEs多为1-2级。更新的研究数据进一步证实了拉罗替尼对于TRK融合胃肠道肿瘤患者是一种快速有效的治疗选择。
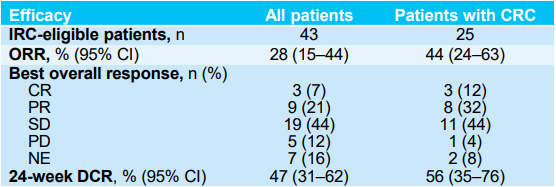
图9. 肿瘤缓解
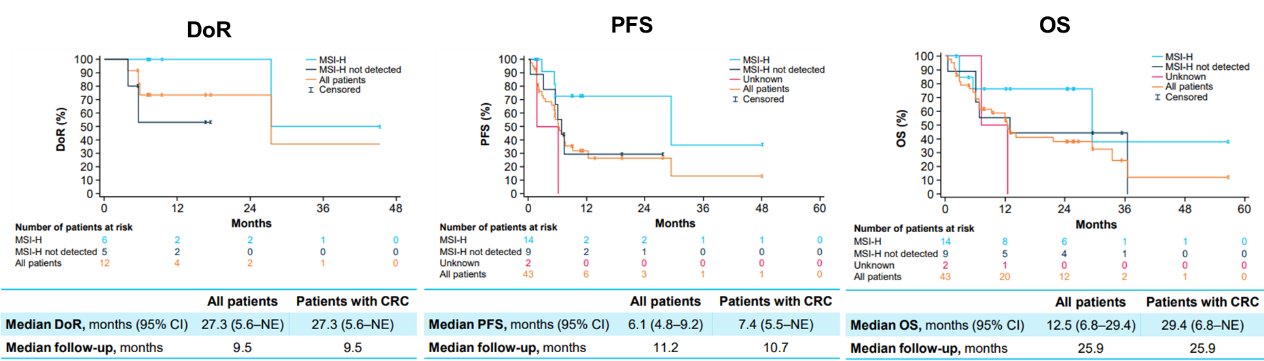
图10. DoR,PFS,OS
张锐 副主任医师
医学博士,副主任医师,副教授 主要从事介入呼吸病学,擅长大咯血血管栓塞、肺部肿瘤灌注化疗、气道疾病介入诊断和治疗。主持国家自然科学基金项目1项,以第一或通讯作者发表SCI论文8篇,参编专著教材2部。
重庆市咯血中心秘书
中华医学会结核病分会互联网医疗专委会委员
中国老年学和老年医学学会老年呼吸与危重症医学分会委员
重庆市医师协会呼吸医师分会肺血管病和肺血管介入学组委员
重庆市医院协会血栓与止血管理专业委员会青年委员
重庆市医学会放射肿瘤治疗学分会放射免疫治疗学组委员
重庆市中西医结合学会肺结节精准治疗专业委员会委员
张锐教授:
在肿瘤精准治疗的前沿领域,NTRK基因融合抑制剂的出现无疑是一颗璀璨的明珠,为实体瘤患者带来了新的希望。NTRK基因融合,这一独特的分子标志物,像是一把精准的钥匙,能够打开癌症精准诊断的大门。通过检测NTRK基因融合,医生们能够为癌症患者提供更加精准的疗效评估、预后预测以及靶向药物治疗方案的选择。精准治疗,检测先行。在临床诊疗中,NTRK基因融合的识别不仅有助于明确诊断,还能够为患者量身定制最适合的治疗方案,从而提高治疗效果,延长患者生存期。尤其是在我国首部NTRK融合基因临床诊疗共识出台后,所有晚期成人实体瘤和儿童实体瘤患者均被建议进行NTRK融合基因检测,并且根据不同癌种的特性采取不同的检测策略[8]。这标志着我国在肿瘤精准治疗领域迈出了重要一步,为临床医生提供了更加明确的指导和规范,有助于提高NTRK基因融合的检测率和诊断准确性,让更多的患者能够从精准治疗中获益,开启个体化治疗的新篇章。
精准治疗的前提是精准检测。NTRK基因融合的识别对于癌症的精准诊断至关重要,是实现精准治疗的关键第一步。通过检测NTRK基因融合状态,医生能够为患者提供更加准确的诊断和预后评估,制定最适合的治疗方案。在晚期成人实体瘤和儿童实体瘤患者中,NTRK融合基因的检测尤为重要。我国首部NTRK融合基因临床诊疗共识的提出,为临床实践提供了明确的指导和规范。该共识建议所有晚期成人实体瘤和儿童实体瘤患者均应进行NTRK融合基因检测,并根据不同癌种的特性采取不同的检测策略[8]。这一共识的出台,有助于提高临床医生对NTRK基因融合的认知和重视程度,推动基因检测技术的发展和应用,为患者提供更加精准的诊断和治疗。我国首部NTRK融合基因临床诊疗共识的发布,填补了国内在这一领域的空白,为临床医生提供了权威的指导和参考。共识明确指出,NTRK基因融合检测对于癌症的精准诊断、疗效评估、预后预测以及靶向药物治疗方案的选择具有重要意义。因此,共识建议所有晚期成人实体瘤和儿童实体瘤患者均应进行NTRK融合基因检测,并根据不同癌种的特性采取不同的检测策略[8]。这一建议不仅有助于提高NTRK基因融合的检测率和诊断准确性,还能够促进精准治疗在临床上的广泛应用,为患者带来更多的希望和机会。
随着国内基因检测技术的不断研发和规范,以及临床学者对NTRK基因融合的认知和重视程度的不断提升,未来这类罕见靶点的患者能够尽早获得精准诊疗。基因检测技术的不断进步,为NTRK基因融合的检测提供了更加可靠和高效的技术支持。同时,临床学者对NTRK基因融合的研究和认识也在不断深入,为精准治疗的实施提供了更加坚实的理论基础。通过提高检测率和诊断准确性,能够让更多的NTRK基因融合患者得到及时的精准诊断和治疗。这不仅有助于提高患者的治疗效果和生存率,还能够改善患者的生活质量,为患者及其家庭带来新的希望和曙光。
拉罗替尼作为跨癌种靶向治疗的先行者,其显著的疗效和良好的安全性已经在临床应用中得到了充分的验证。拉罗替尼不仅能够为患者提供快速且持久的病情缓解,延长患者的生存获益,而且在安全性方面表现出色,治疗相关不良事件多为1级或2级,患者耐受性良好。随着随访时间的不断延长,拉罗替尼持续为患者带来希望和福音,其在肿瘤精准治疗领域的价值愈发凸显。为了确保真正具有NTRK基因融合的患者得到及时的精准诊断,提高NTRK检测率势在必行。这需要临床医生、科研人员、检测机构等各方的共同努力,加强合作与交流,推动NTRK基因融合检测的普及和应用。同时,也需要加强对患者的宣传和教育,提高患者对NTRK基因融合检测的认识和重视,让更多的患者能够主动参与到精准治疗的过程中来,共同为战胜癌症而努力。只有这样,才能让拉罗替尼等精准治疗药物造福更多NTRK基因融合患者,为人类健康事业做出更大的贡献。
拉罗替尼是全球首个不限瘤种、高选择性单靶点、首个且唯一含新生儿适应证的TRK抑制剂,展现了基于基因突变的个性化治疗方案的巨大潜力,为肿瘤治疗带来了全新的理念和希望。基于拉罗替尼在临床试验中展现的显著疗效和可靠安全性,2022年拉罗替尼已获得NMPA批准用于NTRK基因融合肿瘤患者,是首个且唯一含新生儿适应证、唯一上市双剂型的NTRK基因融合靶向药。在今年持续更新研究中,拉罗替尼依旧不负众望,不断传递出令人振奋的临床获益,同时表现出良好的安全性,能够保障患者长期稳定的用药,为NTRK基因融合肿瘤患者带来高质量生存的希望。
2024 年 ESMO 年会上,披露了拉罗替尼作为一线治疗药物,用于既往未接受系统治疗的局部晚期或转移性 TRK 融合肿瘤患者的最新疗效与安全性数据 [3]。在经 IRC 评估的 59 例成人患者里,拉罗替尼一线治疗的客观缓解率(ORR)达 68%(95% CI:54-79)。截至数据全球截点,中位持续缓解时间(DoR)为 59 个月,5 年 DoR 率为 34%;中位无进展生存期(PFS)为 61 个月,5 年 PFS 率为 56%;中位总生存期(OS)暂未达到,5 年 OS 率为 67%。从安全性来看,拉罗替尼治疗所产生的不良事件在可控范围之内,其中治疗相关不良事件(TRAEs)大多为 1 级或 2 级。随着随访时间的不断延长,拉罗替尼持续为患者带来快速且持久的病情缓解,延长其生存获益,并且一直保持着良好的安全性,也逐渐为 TRK 融合肿瘤患者的治疗积累了更多的循证医学证据。
值得关注的是,拉罗替尼纳入2025年国家医保目录,将进一步提高药物的可及性,减轻患者的经济负担,为更多患者带来福音。
NTRK基因融合已成为跨年龄和组织类型且有靶向药物可用的“钻石”靶点,虽然NTRK基因融合在多个常见瘤种中的发生率较低,但由于中国庞大的肿瘤患者人群基数,具有该融合突变的患者数量仍然不可忽视。拉罗替尼开启了广谱抗癌时代,打破传统治疗的局限性,根据肿瘤患者基因特征,个体化制定精准靶向治疗方案。拉罗替尼治疗NTRK基因融合肿瘤患者的长期随访数据持续证实了拉罗替尼在兼顾疗效和安全性方面的显著优势。为了确保真正具有NTRK基因融合的患者得到及时的精准诊断,提高NTRK检测率势在必行,让更多NTRK基因融合患者更早地开始应用拉罗替尼。而拉罗替尼从获批到纳入国家医保药品目录,加速药物可及,降低患者用药经济负担,使临床医生有更多选择为患者制定更高效的治疗策略。
查看更多