查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





《CSCO非小细胞肺癌诊疗指南2023》已于本月召开的CSCO指南会上正式发布。为促进新版指南的理念推广与策略应用,本报特邀请同济大学附属上海市肺科医院肿瘤科主任周彩存教授解读新版指南更新重点,分享驱动基因阳性患者的治疗更新。
CSCO指南更新要点
本次NSCLC指南更新主要在于靶向治疗与免疫治疗的应用策略与治疗药物更新。
对于适宜手术的早期患者,新增术后辅助免疫治疗(阿替利珠单抗,基于IMpower 010研究)和术前新辅助免疫治疗(纳武利尤单抗,基于CheckMate 816研究)作为Ⅰ级推荐;对于Ⅳ期驱动基因阴性的非鳞癌患者,新增特瑞普利单抗联合培美曲塞和铂类、紫杉醇聚合物胶束联合铂类方案为Ⅰ级推荐;对于Ⅳ期驱动基因阴性的鳞癌患者,增加斯鲁利单抗/派安普利单抗联合(白蛋白)紫杉醇和卡铂、紫杉醇聚合物胶束联合铂类方案作为Ⅰ级推荐。
对于IV期驱动基因阳性的患者,新增多种常见靶点(EGFR)及少见靶点的一线治疗药物,其中靶向治疗药物的更新大部分位于少见靶点领域,包括对既往Ⅰ级推荐的检测靶点ALK融合、ROS1融合、RET融合等的治疗药物更新,以及对本次升级为Ⅰ级推荐的检测靶点BRAF V600突变、NTRK融合基因的靶向治疗药物更新。此外,新版指南还强化了肺癌新辅助治疗后病理评估的重要性,并上调了部分分子分型检测的推荐级别。
检测先行:分子分型检测指导治疗决策
在推荐检测的种类上,既往指南要求对非鳞癌的组织标本进行EGFR、ALK、ROS1、RET融合及MET14外显子跳跃突变的分子检测(Ⅰ级推荐),新版指南将BRAF V600突变,NTRK融合基因检测由Ⅱ级推荐升至Ⅰ级推荐。
靶向治疗:晚期驱动基因阳性NSCLC患者指南更新
EGFR敏感突变NSCLC的一线治疗中,新增了三代TKI伏美替尼作为Ⅰ级推荐,基于其显著的PFS改善和进入国家医保目录带来的药物可及性提高。FURLONG研究显示[1],伏美替尼一线治疗对比吉非替尼可显著延长中位无进展生存期(mPFS)(20.8个月 vs 11.1个月,HR=0.44)。
对于EGFR ex20ins而言,指南更新将莫博赛替尼作为后线治疗的Ⅰ级推荐,是基于其治疗含铂化疗期间或之后进展的EGFR ex20ins突变患者的Ⅰ/Ⅱ期临床研究数据:中位生存时间(mOS)为24.0个月,mPFS 7.3个月,客观缓解率(ORR)为28%,且安全可控[2]。
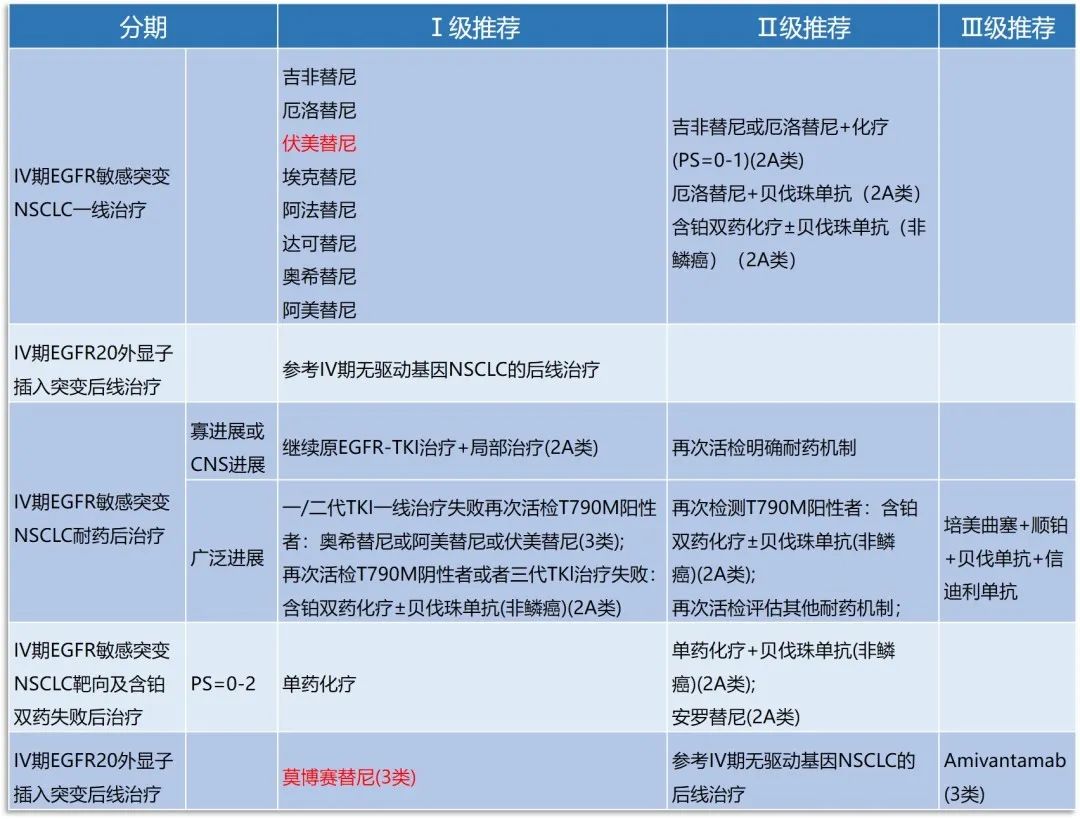
在“三代同堂”的ALK-TKIs中,布格替尼、洛拉替尼和恩沙替尼作为一线治疗及后线治疗的Ⅰ级推荐被写入指南更新,阿来替尼则作为唯一的“优先推荐”位居ALK阳性NSCLC一线治疗的Ⅰ级推荐榜首,这与其有效性、安全性、药物可及性、大量临床用药体验等多方面优势的综合叠加密切相关。
现有的ALK-TKIs中,一代TKI克唑替尼是使用经验最丰富的药物,但PFS获益和颅内病变控制是该药的短板。三代TKI洛拉替尼在耐药突变的覆盖和颅内病灶治疗上具有优势,但中枢神经系统(CNS)不良反应如抑郁、认知障碍等同样是临床面临的难点。二代药物阿来替尼则在具备一定程度使用经验的同时,拥有良好的血脑屏障(BBB)穿透力。ALESIA研究显示[3],其对于亚裔患者而言疗效优异,一线治疗PFS获益显著延长(一线mPFS首次突破40个月,长达41.6个月),且安全性良好。除此之外,获批后近5年的临床应用经验亦显示,阿来替尼的不良反应更为少见且可控,且对于需要合并用药的患者而言,其药物相互作用也更为少见。
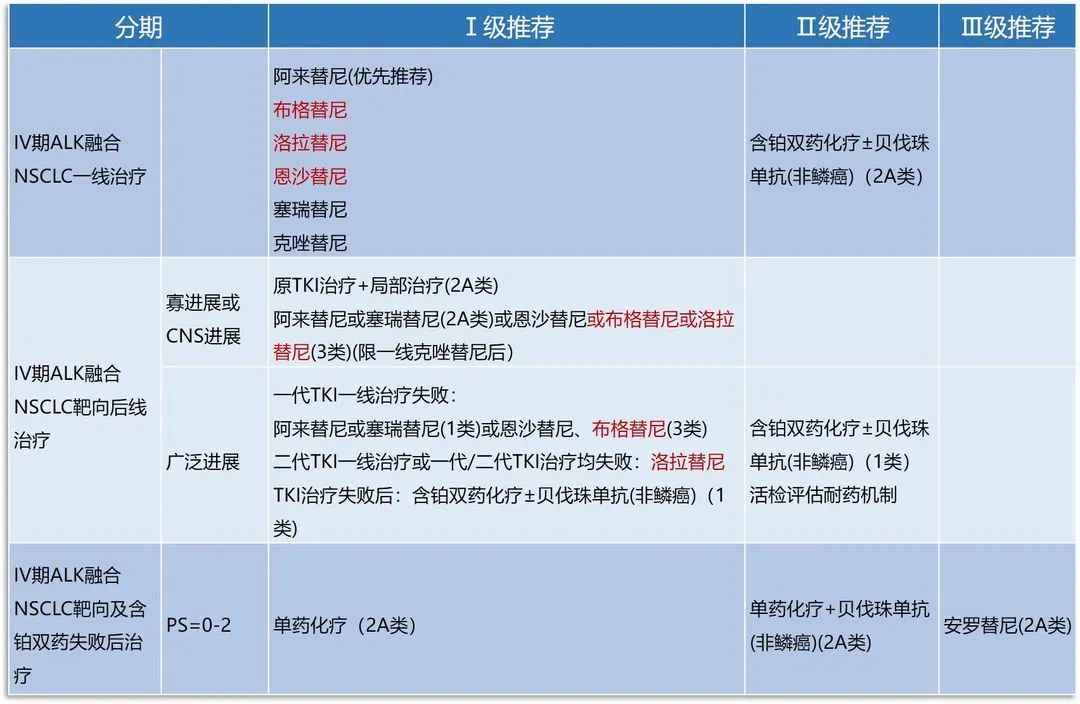
在NSCLC的众多少见靶点中,ROS1基因融合因其“多种实体瘤可见”的特点和突变阳性患者较高的CNS转移率而热度颇高。本次指南更新上调恩曲替尼为一线治疗Ⅰ级推荐。
恩曲替尼是国内首个获批的具有明确CNS疗效的ROS1抑制剂,更是能覆盖ROS1/NTRK等多靶点的TKI抑制剂。STARTRK-1,STARTRK-2和ALKA-372-001三项临床研究的汇总分析显示[4],恩曲替尼治疗局部晚期或转移性ROS1阳性NSCLC患者的ORR为77.0%,mPFS为19.0个月,中位缓解持续时间(DoR)为24.6个月。更值得关注的是,恩曲替尼优秀的BBB穿透能力使其具备突出的颅内缓解率(55.0%)和预防性脑保护作用,从而解决了一代ROS1抑制剂面临的脑转移难题。
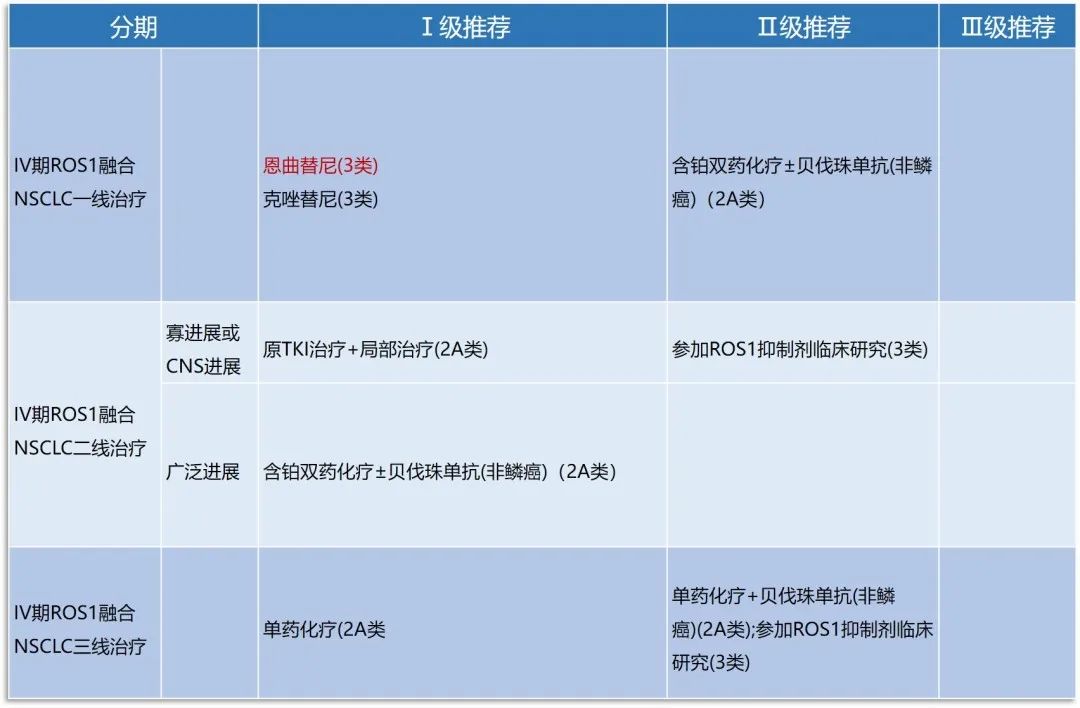
本次指南更新上调恩曲替尼、拉罗替尼为Ⅳ期NTRK融合NSCLC一线治疗的Ⅰ级推荐。
一项发表于NEJM上纳入55例NTRK融合实体瘤患者的研究显示[5]:拉罗替尼治疗ORR为75%,1年时的研究者评估提示71%的患者应答持续,55%的患者保持无进展。
ARTRK-1,STARTRK-2和ALKA-372-001三项临床研究的汇总分析显示[6],恩曲替尼治疗NTRK融合实体瘤患者的ORR为57.0%,mPFS为11.2个月,DoR为10.4个月,颅内ORR为50.0%,亚组数据也进一步呈现了恩曲替尼在中国人群中的安全性及有效性。
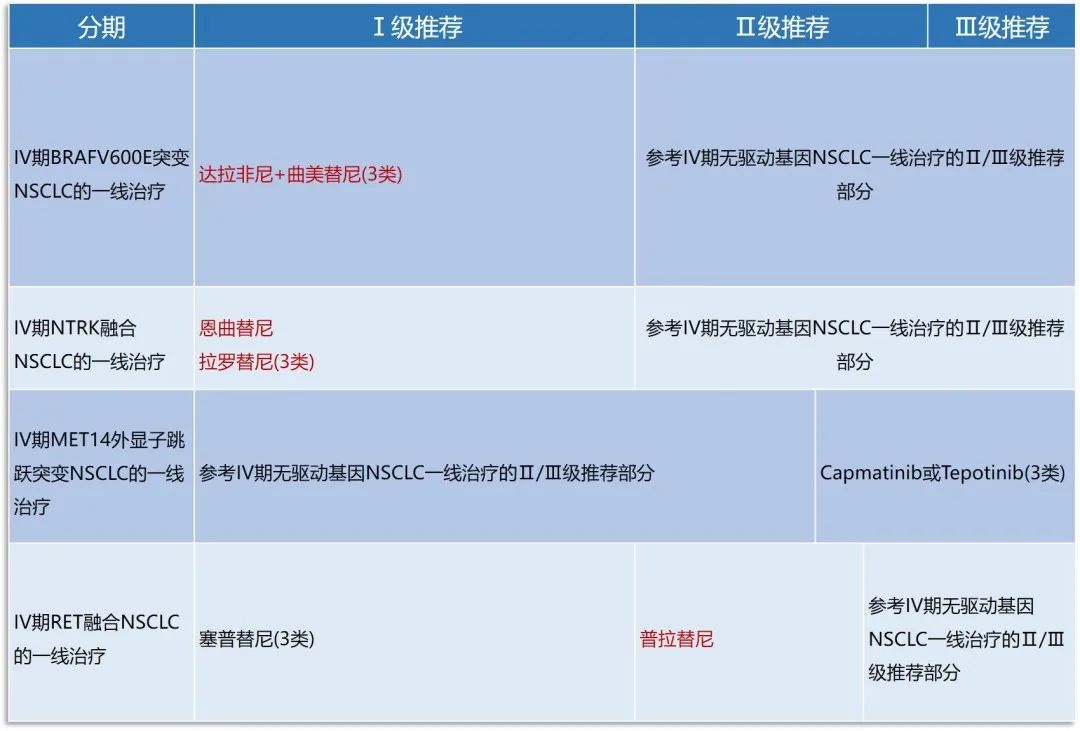
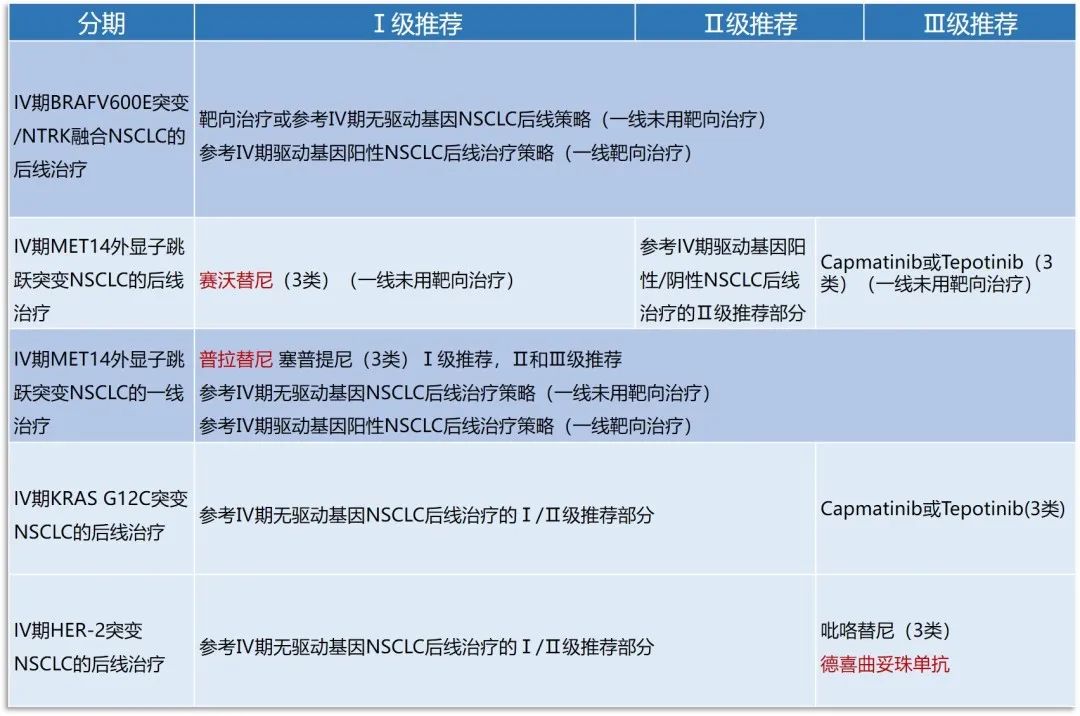
近年来国内外针对少见靶点的临床研究接连实现突破,针对BRAF V600/MET14外显子/RET/KRAS G12C突变的多种药物已获得美国FDA或NMPA批准上市,HER2突变NSCLC的靶向治疗也逐渐迎来曙光。
一项达拉非尼联合曲美替尼用于一线治疗的Ⅱ期临床研究显示[7],其ORR为64%,mPFS为10.9个月,mDoR为10.4个月。目前NMPA已批准达拉非尼联合曲美替尼治疗BRAF V600突变的晚期NSCLC并纳入医保。本次指南更新也将其纳入Ⅰ级推荐。
而针对MET14外显子突变、RET融合和KRAS G12C突变的晚期NSCLC患者,相关Ⅱ期临床研究[8]、ARROW研究[9]、KRYSTAL 01研究[10]等也分别呈现出了赛沃替尼、普拉替尼及Adagasib带来的临床获益。本次更新中,赛沃替尼和普拉替尼被列入Ⅰ级推荐,Adagasib因未在国内上市因此仅作为Ⅲ级推荐。
德喜曲妥珠单抗在HER2突变晚期NSCLC的治疗中也显示出了良好的抗肿瘤活性,研究显示其ORR、mPFS、mOS分别为55%、8.2个月和17.8个月[11],本次经专家组投票上调为Ⅲ级推荐。
CSCO指南会以每年一次的频率召开,聚焦中国患者群体与本土化策略,发布更适合中国国情、更具普及性的常见恶性肿瘤诊疗指南。NSCLC领域近年来的热点之一当属少见靶点相关研究,不但驱动基因的检测方法致力于推陈出新, 治疗药物也在创新与突破中持续更新迭代,在刷新PFS与OS数据的同时也为患者带来了更长生存。然而少见突变因其临床发生率低,在检测与治疗上仍然面临着多种问题。未来希望临床实践能更多地着眼于少见靶点规范化诊疗流程,助力分子检测与药物研发向前迈进,从而为更多患者提供兼具生存时间与生活质量的多角度获益。
参考文献:
[1] Shi Y, et al. Furmonertinib (AST2818) versusgefitinib as first-line therapy for Chinese patients with locally advanced or metastatic EGFR mutation-positive non-small-cell lung cancer (FURLONG): a multicentre,double-blind, randomised phase 3 study. Lancet Respir Med. Published on Jun 2, 2022.
[2] Zhou C, et al. Treatment Outcomes and Safety of Mobocertinib in Platinum-Pretreated Patients With EGFR Exon 20 Insertion-Positive Metastatic Non-Small Cell Lung Cancer: A Phase 1/2 Open-label Nonrandomized Clinical Trial. JAMA Oncol. 2021;7(12):e214761.
[3] Peters S, et al. Alectinib versus Crizotinib in Untreated ALK-Positive Non-Small-Cell Lung Cancer. N Engl J Med. 2017;377(9):829-838.
[4] Drilon A, et al. Entrectinib in ROS1 fusion-positive non-small-cell lung cancer: integrated analysis of three phase 1-2 trials. Lancet Oncol. 2020;21(2):261-270.
[5] Planchard D, et al. Dabrafenib plus trametinib in patients with previously treated BRAF(V600E)-mutant metastatic non-small cell lung cancer: an open-label, multicentre phase 2 trial.
[6] Doebele RC, et al. Entrectinib in patients with advanced or metastatic NTRK fusion-positive solid tumours: integrated analysis of three phase 1-2 trials. Lancet Oncol. 2020;21(2):271-282.
[7] Planchard D, et al. Dabrafenib plus trametinib in patients with previously treated BRAF(V600E)-mutant metastatic non-small cell lung cancer: an open-label, multicentre phase 2 trial. Lancet Oncol. 2016;17(7):984-993.
[8] Lu Shun, et al. Phase II study of savolitinib in patients (pts) with pulmonarysarcomatoid carcinoma (PSC) and other types of non-small cell lung cancer(NSCLC) harboring MET exon 14 skipping mutations (METex14+).2020 ASCO[3]Sequist LV,Han JY, Ahn MJ,et al. LancetOncol.2020;21(3):373-386.
查看更多