查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





中国是肝癌高发国家,据国家癌症中心发布的2015年恶性肿瘤数据显示,肝癌新发病例37万,位居第四,死亡病例高达32.6万,位居第二。中国肝癌患者分期较晚,且多伴有肝脏基础疾病,预后较差,传统的手术、局部治疗等方法效果并不好,靶向治疗的进展也止步不前,免疫治疗成为了肝癌患者的新希望。由百济神州自主研发的创新PD-1抑制剂替雷利珠单抗(百泽安®)在肝癌领域展现强劲抗肿瘤效应,目前已经在二线肝细胞癌(HCC)Ⅱ期临床研究中获得喜人成绩,并获得国家药品监督管理局(NMPA)附条件批准用于治疗至少经过一种全身治疗的HCC患者。此外,替雷利珠单抗单药及联合靶向药物的一线治疗HCC的研究也正在积极开展中,期待能够为更多肝癌患者带来生存获益。本期分享1例BCLC分期C期无法手术HCC患者的治疗经历,该患者从替雷利珠单抗联合方案中显著获益。(点评专家:严盛教授;分享专家:周波教授)
周 波 教授
浙江大学医学院附属第二医院肝胆胰外科
副主任医师,浙江大学医学博士
擅长:肝脏肿瘤和胰腺肿瘤的微创治疗,对肝胆胰外科疾病如肝脏肿瘤、肝内外胆管结石、肝内外胆管肿瘤和胰腺肿瘤、肝硬化和门静脉高压症、脾脏疾病、肝门部胆管癌的诊断和治疗有丰富的临床经验。
科研教学:先后主持和参加国家自然科学基金、浙江省科技计划项目和浙江省教育厅一般科研项目等工作,在SCI收录杂志和国内一类期刊发表论文20余篇。
一般资料:患者男性,47岁。
主诉:右上腹间歇性疼痛2个月。
既往史、个人史/家族史:无特殊。
ECOG PS评分:1分。
查体:无明显阳性体征。
实验室检查(2020年6月):白细胞计数4.5×109/L,血红蛋白157 g/L,红细胞4.9×1012/L,血小板计数10×109/L,总胆红素 30.6 μmol/L,谷丙转氨酶46 U/L,谷草转氨酶44 U/L,AFP 132.1 ng/mL。
肝脏增强MRI(2020年6月18日):右肝叶巨大肿块,最大截面约93×76 mm,伴门脉右支癌栓形成;肝硬化,脾大,少量腹腔积液(图1)。
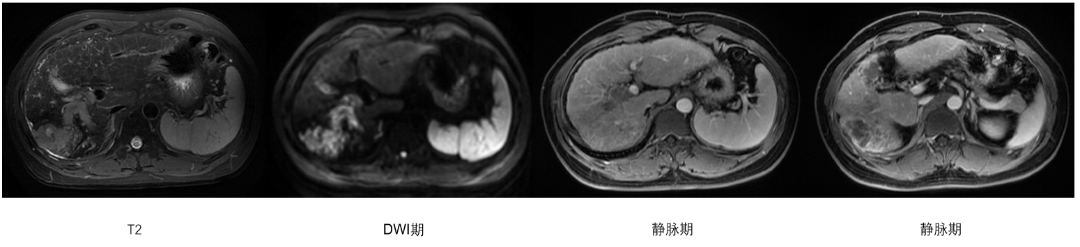
图1 2020-06-18肝脏增强MRI
全腹增强CT(2020年6月19日):肝右叶肝癌,肿瘤累及右侧膈肌伴少量肝周积液,门脉右支及远端分支广泛癌栓(图2)。
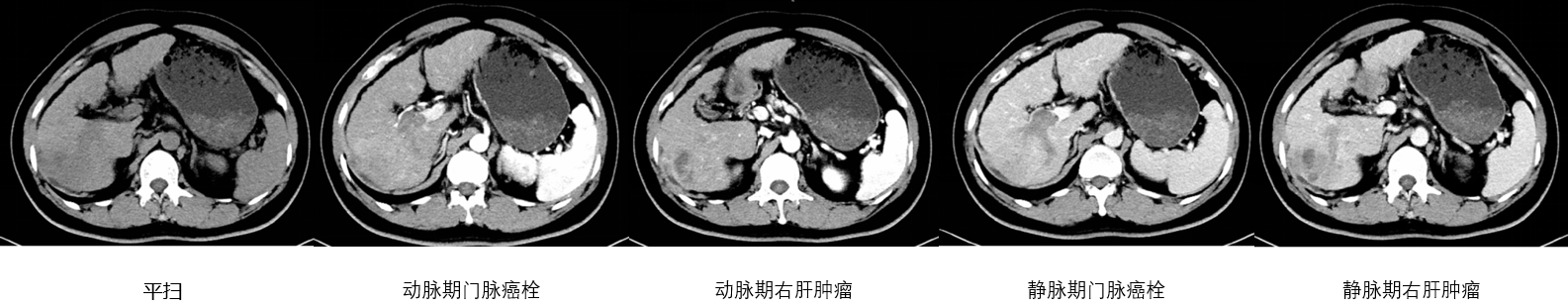
图2 2020-06-19全腹增强CT
诊断:肝细胞肝癌(BCLC分期C期,Child-Pugh分级A级),门静脉癌栓(PVTT)分型(MVI情况)Ⅱ型。
治疗方案:经患者充分知情同意并签署知情同意书后,于2020年6月19日予以1次立体定向放射治疗(SBRT),同时应用“替雷利珠单抗200mg ivgtt q3w + 仑伐替尼8mg po qd”治疗,共6周期。
影像学及疗效评价:患者先后于2、4周期后进行随访检查(图3),AFP分别为24.6 ng/mL、13.64 ng/mL,病灶大小分别为76×53 mm、74×51 mm,疗效评价达为持续部分缓解(PR)。
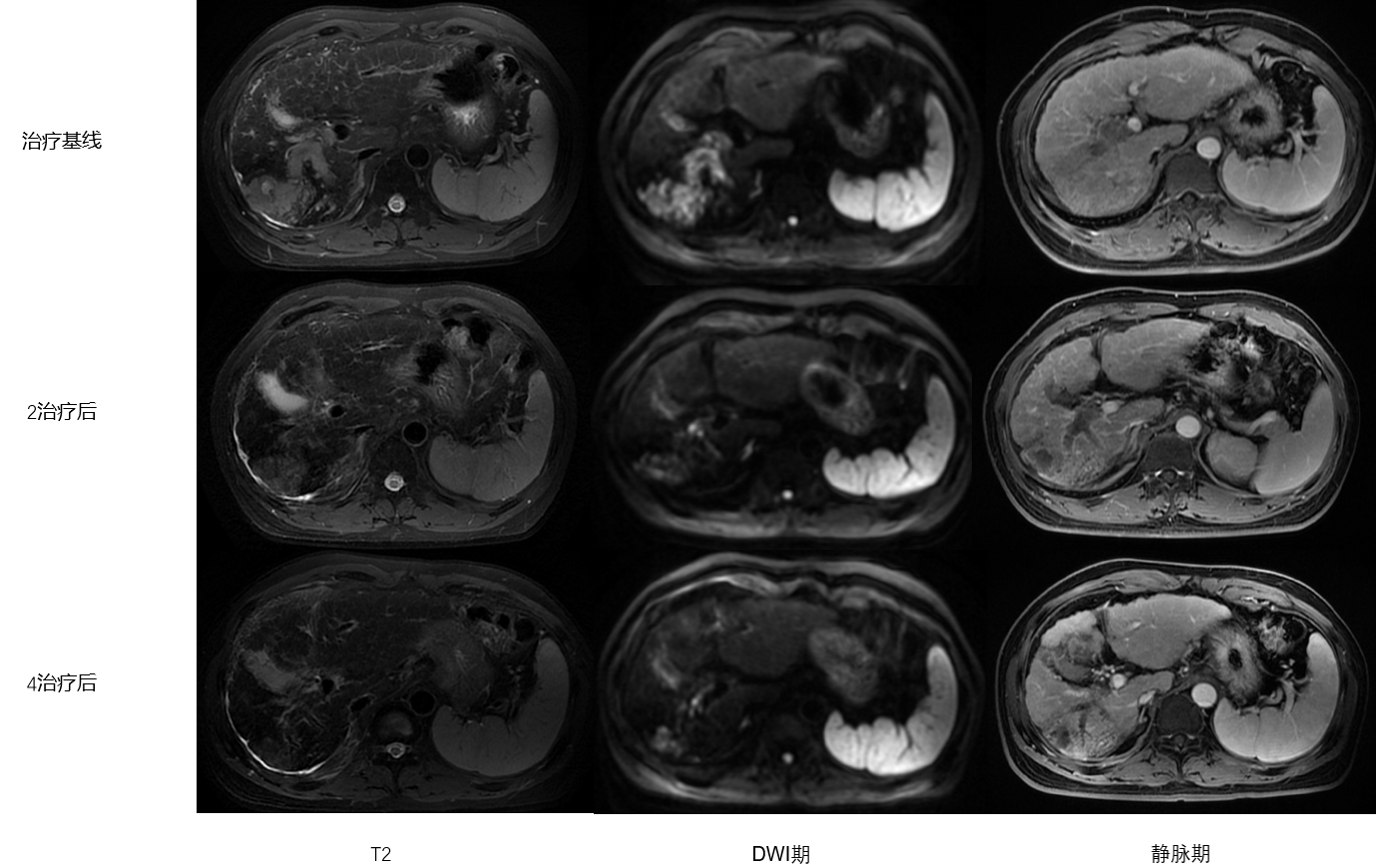
图3 治疗期间肝脏病灶动态变化

图4 患者AFP水平变化
2020年10月入院接受肝移植,肝移植后患者出现了AFP短暂升高,未接受特殊治疗,逐渐降至正常。
本例患者为中年男性,因“右上腹间歇性疼痛2个月”就诊。结合症状、既往史和影像学,明确为HCC(BCLC分期C期,Child-Pugh分级A级),伴有Ⅱ型PVTT。经过临床综合考量后,予以患者放疗联合6周期系统治疗后,病灶持续缩小,疗效评估持续PR,达到肝移植标准,并进行肝移植手术。
严 盛 教授
浙江大学医学院附属第二医院肝胆胰外科&肝移植中心副主任
主任医师,博士生导师。
擅长:各类肝胆胰肿瘤及其他疾病的外科手术治疗;擅长微创外科,熟练掌握腹腔镜肝脏、胰腺手术及脾切断流等高难度腔镜手术;擅长动脉、胆道的显微外科重建与修复;开展临床同种异体胰岛移植及自体胰岛移植项目。
1999年毕业于浙江大学七年制临床医学系,获得外科硕士学位;2001-2004年留学德国汉诺威医学院,主攻腹部外科及器官移植学,并获得德国医学博士学位;2007年于浙江大学获得外科学博士学位;2007年于瑞士日内瓦大学医院,主要研究胰腺及胰岛移植;并作为中国-加拿大Albert合作项目访问学者,在加拿大Edmonton研习胰岛移植技术,同年在浙江大学建立胰岛分离实验室。长期从事肝胆胰外科的临床及基础研究工作,有着丰富的临床诊治经验,先进的外科治疗理念及手术技巧。
HCC是中国高发肿瘤,发病率位于所有恶性肿瘤第4位,死亡率高居第2位[1]。肝癌的外科治疗是肝癌患者获得长期生存最重要的手段,主要包括肝切除术和肝移植术。研究显示,我国初诊肝癌患者大部分是BCLC C期(55%),约30%BCLC C期患者会接受手术治疗,更多的患者因肿瘤巨大、肿瘤多发和剩余肝体积不足而无法行根治切除[2]。对于不可切除肝癌,《原发性肝癌诊疗规范(2019)》指出,术前 TACE、外放射等治疗可能促进肿瘤降期从而使部分患者获得手术切除的机会,降期后切除的肝癌患者可能获得较好的长期生存效果[3]。肝癌的降期/转化治疗已逐步被认可并成为不可切除肝癌的重要治疗目标,但是目前仍需要更多高级别的临床证据,以期形成规范化的实施标准。
近年来,免疫联合靶向治疗成为肝癌领域的研究热点,大型随机对照研究(IMbrave150研究)证实PD-1抑制剂联合抗血管生成药物能够显著延长晚期HCC患者生存,并成为国内外指南中晚期肝癌一线治疗的推荐方案[4]。从机制角度来看,抗血管生成治疗可以改善肿瘤的微环境,增强PD-1/PD-L1抑制剂抗肿瘤的敏感性,继而发挥得协同抗肿瘤效果[5]。此后,多项真实世界研究再次证实了免疫检查点抑制剂+靶向药物在HCC患者中的高有效率(ORR),为肝癌转化治疗带来希望。一项PD-1抑制剂联合TKI的真实世界研究显示,经过转化治疗后,18.3%的不可手术或晚期HCC患者转化为可切除HCC[6]。
替雷利珠单抗是一款人源化IgG4抗PD-1单克隆抗体,通过改造Fc段,最大限度地减少与巨噬细胞表面Fcγ受体结合的能力,从而消除了抗体依赖的细胞介导的吞噬作用(ADCP),保护T细胞的功能活性,理论上可增强免疫治疗的有效性[7]。此外,替雷利珠单抗的Fab段与PD-1的结合面与PD-1/PD-L1结合面重叠高达82%,能更大程度阻断PD-1与PD-L1的结合,发挥强大的抑制作用[8]。替雷利珠单抗在肝癌等巨噬细胞数量较多的肿瘤中,具有更出色的T细胞激活效应[9]。
替雷利珠单抗在肝癌中的抗肿瘤效果在多项临床研究中得到验证。在RATIONALE 001研究中,替雷利珠单抗单药二线治疗晚期肝癌患者的ORR高达18.8%,DCR高达56.3%[10]。继RATIONALE 001肝癌队列的出色数据,另一项全球多中心Ⅱ期RATIONALE 208研究继续探索替雷利珠单抗在至少经过一种全身治疗的HCC患者中的疗效和安全性。研究显示,中位无进展生存期(mPFS)达2.7个月,中位总生存期(mOS)为13.2个月,近80%客观缓解患者能够持续病情缓解超过一年[11]。基于RATIONALE 208研究的结果,国家药品监督管理局(NMPA)已附条件批准替雷利珠单抗用于治疗至少经过一种全身治疗的HCC患者。替雷利珠单抗对比索拉非尼一线治疗晚期HCC的全球Ⅲ期临床研究RATIONALE 301已完成入组,期待能够为替雷利珠单抗在肝癌领域的应用再添证据。
该例患者初诊时为BCLC分期C期HCC,肿瘤较大,且伴有Ⅱ型PVTT,不适宜接受切除手术治疗。经患者充分知情同意后,给予患者局部与系统治疗联合的转化降期治疗方案,肿瘤得以控制,获得PR疗效,其后成功接受肝移植手术,获得了良好生存获益,提示伴PVTT不能手术的肝癌患者予以免疫+靶向+放疗,具有快速杀灭肿瘤活性细胞的可能。
该例患者的治疗经过提示免疫联合治疗方案在晚期肝癌伴PVTT转化治疗中安全有效,可以快速有效缩瘤,并持续降低AFP水平,可作为不可切除晚期肝癌患者的一线治疗选择之一,是未来肝癌免疫治疗的探索新方向。替雷利珠单抗联合仑伐替尼一线治疗晚期HCC的Ⅱ期临床研究以及联合Sitravatinib治疗肝癌及胃癌/胃食道交界处癌中的I/Ⅱ期研究也正在开展中,期待会为替雷利珠单抗联合靶向治疗提供更多思路。
参考文献
[1] Zhou M, Wang H, Zeng X, et al. Mortality, morbidity, and risk factors in China and its provinces, 1990-2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet, 2019, 394(10204): 1145-1158.
[2] Park JW, Chen M, Colombo M, et al. Global patterns of hepatocellular carcinoma management from diagnosis to death: the BRIDGE Study. Liver Int. 2015, 35(9):2155-66.
[3] 原发性肝癌诊疗规范(2019版)
[4] Palle PR, Finn RS, Qin S, et al. Patient-reported outcomes with atezolizumab plus bevacizumab versus sorafenib in patients with unresectable hepatocellular carcinoma (IMbrave150): an open-label, randomised, phase 3 trial. Lancet Oncol. 2021, 22(7):991-1001.
[5] Zongyi Y, Xiaowu L. Immunotherapy for hepatocellular carcinoma. Cancer Lett. 2020, 1;470:8-17.
[6] 2020 ASCO, Abstract e16690.
[7] Arlauckas SP, et al. In vivo imaging reveals a tumor-associated macrophage-mediated resistance pathway in anti-PD-1 therapy. Sci Transl Med. 2017, 9(389): 3604.
[8] Yingcai Feng, Yuan Hong, et al. The molecular binding mechanism of tislelizumab, an investigational anti-PD-1 antibody, is differentiated from pembrolizumab and nivolumab.
[9] Zhang T, et al. The binding of an anti-PD-1 antibody to FcγRΙ has a profound impact on its biological functions. Cancer Immunol Immunother. 2018;67(7): 1079-1090.
[10] BGB-A317-001, NCT02407990.
[11] M. Ducreuc et al. 2021 ESMO GI Abstract O-1.
查看更多