查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





患者,男性,60岁。因“反复右外耳道溢液1 年余,加重1 月”于2018年5月30日入院。
患者1年余前开始反复出现右外耳道清亮溢液,无发热,无流脓,无头痛。于某专科医院就诊,头颅CT发现鼻咽部软组织占位,遂先后于2017年5月8日和11月30日两次行鼻咽肿块切除术,两次鼻咽肿块切除术后病理报告为:
1. (2017年5月8日)鼻咽部黏膜及肉芽肿组织慢性炎。部分区域鳞形上皮不规则增生伴不典型增生,出血、坏死;
2. (2017年11月30日)鼻咽肉芽肿组织急慢性炎,伴大片坏死及炎性渗出,被覆鳞形上皮不规则增生,坏死组织中见霉菌丝样轮廓,破碎死骨组织中见大量菌落及少量菌丝样物。两次术后均用头孢曲松2.0 g qd抗感染治疗近1月,外耳道溢液明显减少后停抗感染治疗。入院前1月,患者外耳道溢液再次发作并加重,颜色转为淡黄色,微混浊,伴有张口受限,外院予氯霉素及地塞米松混合滴耳,头孢曲松2.0 g qd抗感染治疗,无明显好转。遂于我科门诊就诊,并收住入院。既往17年前有鼻咽癌放疗病史,规则随访,肿瘤无复发。
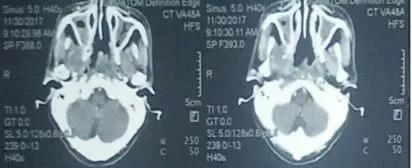
2017-11-30 鼻窦 CT示鼻咽、颅底、蝶窦弥漫性软组织团块,伴周围侵犯、颅底骨质广泛破坏。左蝶窦底、鼻咽部见强化团块。
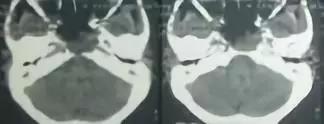
2018-5-18耳轴位CT,病灶较2017-11 -30稍减少,伴中颅底骨质广泛破坏,双侧慢性中耳乳突炎、双侧多发鼻窦炎。
(一)入院后病情分析
患者既往有鼻咽癌放疗病史,本次起病前1年内行2次鼻咽肿物切除术,术后病理提示感染性病变,予以头孢曲松静滴抗感染治疗,病情有所好转。本次发病右耳溢液由清亮改变为黄色浑浊。患者鼻咽癌病灶及鼻咽手术均可造成鼻咽部及中耳局部生理屏障破坏,局部抵抗力下降,从而诱发感染。结合入院前影像学检查,患者肿瘤复发及新发肿瘤的可能性小,感染性疾病可能性大。故入院诊断:右耳化脓性中耳炎;鼻咽癌放疗后。但病原菌不明确。
本次再次出现外耳道渗液,外院头孢曲松会失效原因考虑:患者病程较长, 考虑慢性中耳炎,且有两次手术史,病原菌除链球菌、流感嗜血杆菌外还需要考虑铜绿假单胞菌、大肠埃希菌以及其他少见病原菌的混合感染。故入院再次留取病原学标本后开始予以哌拉西林/他唑巴坦4.5 g 静滴q8h 抗感染。另外,第二次术后病理“坏死组织中见霉菌丝样轮廓,破碎死骨组织中见大量菌落及少量菌丝样物”,建议患者借原病理白片至我院病理科会诊,加做PAS、六胺银、抗酸染色等特殊染色。
完善其他辅助检查:
1.血常规:白细胞计数4.02x10^9 /L,中性粒细胞56.8%,红细胞计数3.6x10^12 /L↓,血红蛋白100 g/L↓,淋巴细胞 32.3%,血小板计数259x10^9 /L,血沉:34 mm/h↑;
2.外耳道溢液真菌涂片+培养阴性;外耳道溢液革兰染色涂片+细菌培养阴性;外耳道溢液抗酸染色涂片未找到抗酸杆菌;
3.血G试验、GM试验、T-SPOT、隐球菌乳胶凝集定量试验阴性;
4.淋巴细胞亚群分型正常;
5.补体、IgG4、免疫球蛋白、C 反应蛋白均正常范围内;
6.ANA、ENA、dsDNA、ANCA、抗心磷脂抗体、抗肾小球基底膜抗体均阴性。
哌拉西林/他唑巴坦4.5g 静滴q8h 抗感染治疗3天后,右侧外耳道溢液略有减少,仍有黄色略浑浊液体。此时患者外院手术病理白片送至我院病理科会诊结果回报:(鼻咽)黏膜溃疡伴鳞状上皮增生;另见少量骨质呈虫蚀状破坏,其周围及内部见大量小球状、细丝状微生物。特殊染色PAS(+),六胺银染色(+),抗酸染色(-),提示放线菌感染可能。因放线菌生长缓慢,培养困难,一般需要15~20天才能形成肉眼可见菌落。故诊断通常依据组织病理。
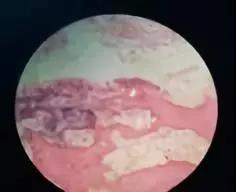
2018-06-05 外院病理片我院会诊意见:(鼻咽)黏膜溃疡伴鳞状上皮增生;另见少量骨质呈虫蚀状破坏,其周围及内部见大量小球状、细丝状微生物。特染PAS(+),银染(+),抗酸(-),病理提示放线菌感染可能。
故该病例最终诊断
1. 右侧化脓性中耳炎:放线菌感染;
2. 鼻咽癌放疗后、伴中颅底骨质破坏。
遂根据病理调整治疗方案为哌拉西林/他唑巴坦4.5g q8h联合莫西沙星0.4g po qd,外耳道溢液症状消失。患者白细胞下降,遂调整为亚胺培南1 g q8h 抗感染,患者未再发热,无溢液。患者于6月28日出院,口服改为多西环素 0.1 g bid治疗。7月19日改阿莫西林/克拉维酸钾0.375g po tid+阿莫西林0.5 g po tid。8月2日电话随访,患者7月30日,当地医院复查鼻咽部CT,鼻咽腔内软组织病灶较前缩小。目前仍交替口服阿莫西林克拉维酸钾和多西环素维持治疗中。
(一)放线菌病对头孢曲松大多敏感,为什么本次患者发病后头孢曲松治疗效果欠佳?
放线菌病首选青霉素类药物。临床很多放线菌病几乎都是混合感染的一部分,特别是合并放线共生放线杆菌、腐蚀埃肯菌、类杆菌属或是链球菌属的感染;且Actinomycetes europaeus和Actinomycetes graevenitzii 等放线菌对头孢曲松具有耐药性。
(二)继续单用哌拉西林/他唑巴坦,延长时间是否也可看到疗效?
多数放线菌对青霉素类药物敏感,若患者可以耐受哌拉西林他唑巴坦,无相关不良反应,继续哌拉西林他唑巴坦治疗,可能亦可以看到疗效。但本病治疗时间长,总疗程一般为6~12个月。
(三)怎样提高诊断成功率?
放线菌病诊断比较困难,且容易误诊,目前确诊靠组织培养和病理。若临床怀疑放线菌病,应与微生物实验室联系,将培养平板多保留时间延长至3周左右。
(四)针对混合感染的经验治疗,方案如何选择?
根据患者原发病种类、诱发因素、免疫状况、流行病学资料、可能的病原菌及本地区的细菌药敏情况尽早开始经验性治疗,可联合使用具有协同作用的药物。另外,应尽早行病原菌培养和药敏试验,并根据结果调整用药。
放线菌是一种革兰阳性非抗酸厌氧丝状杆菌,可正常寄居在人体的口腔、上呼吸道、胃肠道及泌尿生殖道,是条件致病菌,当人体抵抗力降低或伴细菌感染时便可发病。
放线菌病是人畜共患病,其特点是病程较为缓慢,呈渐进性,以农民及野外作业者多见。
感染性疾病的病原诊断非常重要。除了传统的涂片染色和培养以外,应根据临床情况选用组织病理、免疫学试验和分子测序等实验室方法作为补充,特别是临床疑似为某些培养难度高阳性率低的病原感染时。本例病例最终根据病理诊断为放线菌病,抗放线菌治疗后临床症状体征缓解。
放线菌病特点:肉芽肿、脓肿、组织纤维化和瘘管形成;并排出带有硫磺样颗粒的脓液。
放线菌病的组织病理:早期局部有白细胞浸润,形成小脓肿,穿破形成窦道,各窦道可互通。放线菌一旦被激活,体内筋膜、胸膜、横膈、骨骼等均不能阻止其发展。化脓区附近可有慢性肉芽组织增生,可有淋巴样细胞、浆细胞、组织细胞及成纤维细胞等浸润,局部组织还可呈玻璃样变性,致硬板样,脓肿内可见“硫磺颗粒”,HE染色中央呈均质性,周围有栅栏状短棒样细胞。
放线菌病在无药敏试验结果支持时,首选青霉素G或氨苄西林,次选多西环素或头孢曲松,克林霉素或红霉素亦有效。
作者:山东省曲阜市人民医院 张峰
秦晓华 华山医院抗生素研究所
本文首发自华山抗生素所
查看更多