查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





一般资料:患者彭某,女,63岁。
主诉:体检发现左肺下叶病变1周。
现病史:患者1周前在当地体检发现左肺下叶背段约3.6*3.7*3.4cm3的圆形软组织密度影,于5.11就诊,行PET-CT报告显示:左肺下叶背段可见团块状软组织病变,大小约4.1*3.6*3.9cm3,考虑为恶性病变,肺癌可能性大;左侧锁骨上区、纵隔(2R、4R、4L、5、6组)、双肺门及胸12水平腹膜后多发肿大淋巴结,呈不同程度FDG代谢异常增高,考虑为转移性淋巴结;右肺门肿大及钙化淋巴结压迫右肺中叶支气管致狭窄伴阻塞性炎性病变;心包积液。
既往史:无特殊。
个人史:无特殊不良嗜好,ECOG评分1分。
PET-CT:①左侧下叶背段团块状软组织病变,大小约4.1*3.6*3.9cm3,边缘见毛刺,呈放射性摄取显著异常增高,SUV最大值约20.2。②左侧锁骨上区、纵隔、双肺门及胸12水平腹膜后多发肿大淋巴结,呈不同程度FDG代谢异常增高,考虑为转移性淋巴结;心包积液。

图2-1 2021年5月11日PET-CT检查
颈部超声:左侧锁骨上区淋巴结与血管关系密切,穿刺风险大。
肺穿刺活检:5月13日行经皮肺穿刺活检,提示鳞癌。
基因检测:基因检测EGFR(-),ALK(-),ROS1(-),PD-L1表达55%。化验检查提示肿瘤标志物多项明显升高,其余各项实验室检查未见明显异常,各项辅助检查无特殊异常。心包穿刺:提示血性心包积液,病理提示心包积液中查见肿瘤细胞。
诊断:肺癌(左下肺 鳞癌cT2bN3M1a Ⅳa期)。
治疗方案:通过MDT会诊确定治疗方案为白蛋白紫杉醇135mg/m2+顺铂75mg/m2+替雷利珠单抗200mg 6周期,之后行替雷利珠单抗单药维持治疗。
治疗经过:2021年5月13日至2021年8月25日行白蛋白紫杉醇135mg/m2+顺铂75mg/m2+替雷利珠单抗200mg治疗4周期,患者因化疗胃肠道副反应大,不愿继续化疗,遂于2021年9月22日开始替雷利珠单抗200mg单药维持治疗,1次/3周,计划维持1年。目前患者状况良好,维持治疗过程中无明显不适,各项实验室检查无明显异常,肿瘤缩小达到PR,肿瘤标志物恢复正常。
影像学复查及疗效评价:
化疗联合免疫治疗2周期(2021年7月16日),CT显示:①左肺下叶背段可见团片状高密度影,大小约2.0*1.5cm2,左肺下叶背段占位性病变较前有所缩小;纵隔淋巴结部分较前有所缩小。②心包积液较前稍有所减少。
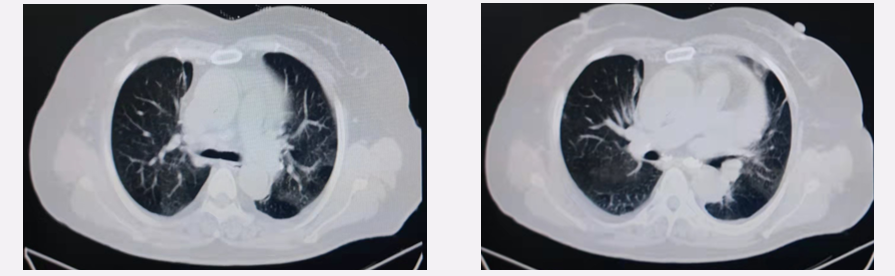
图2-2 2021年7月16日复查CT
化疗联合免疫治疗4周期(2021年10月20日),检查所见:左肺下叶背段可见团片状高密度影,大小约1.8*1.3cm2,左肺下叶背段占位性病变较前略缩小,纵隔淋巴结、左肺中叶、左肺上叶舌段及下叶炎症伴部分肺不张、心包积液较前基本无变化。

图2-3 2021年10月20日复查CT
2022年3月8日,检查所见:左肺下叶背段可见团片状高密度影,大小约1.7*1.3cm2,形态尚规整,左肺下叶背段占位性病变较前略缩小,纵隔淋巴结、右肺中叶、左肺上叶舌段及下叶炎症伴部分肺不张、心包积液较前基本无变化。
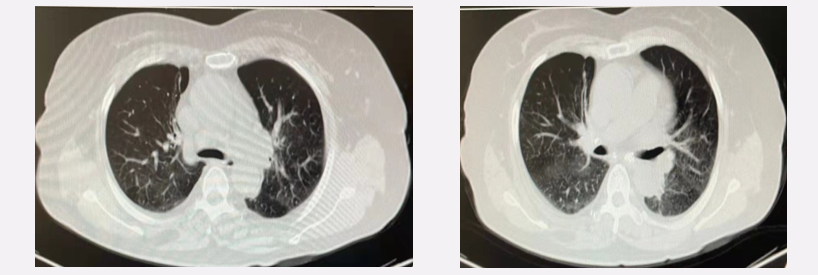
图2-4 2022年3月8日复查CT
治疗前后影像学对照:
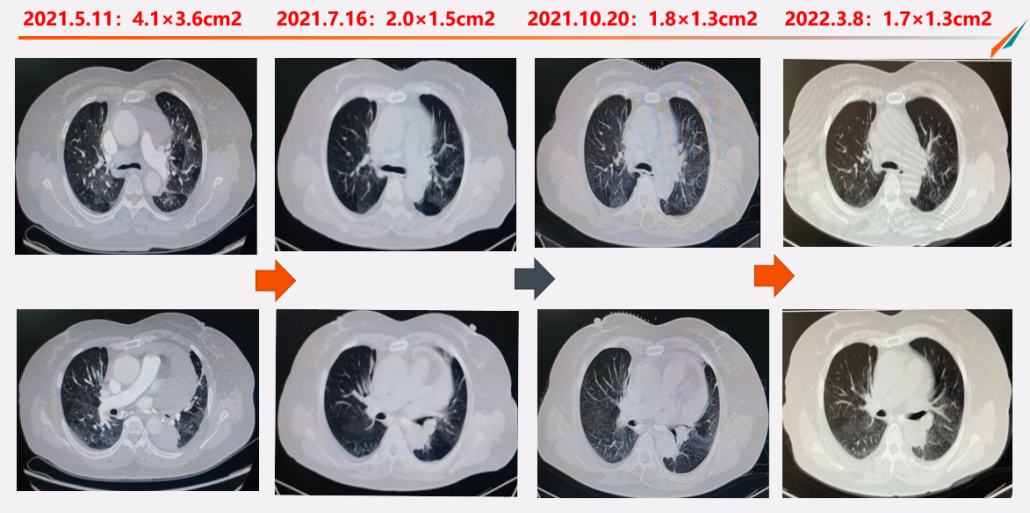
图2-5 治疗前后影像学对照
治疗前后肿瘤标志物对照:
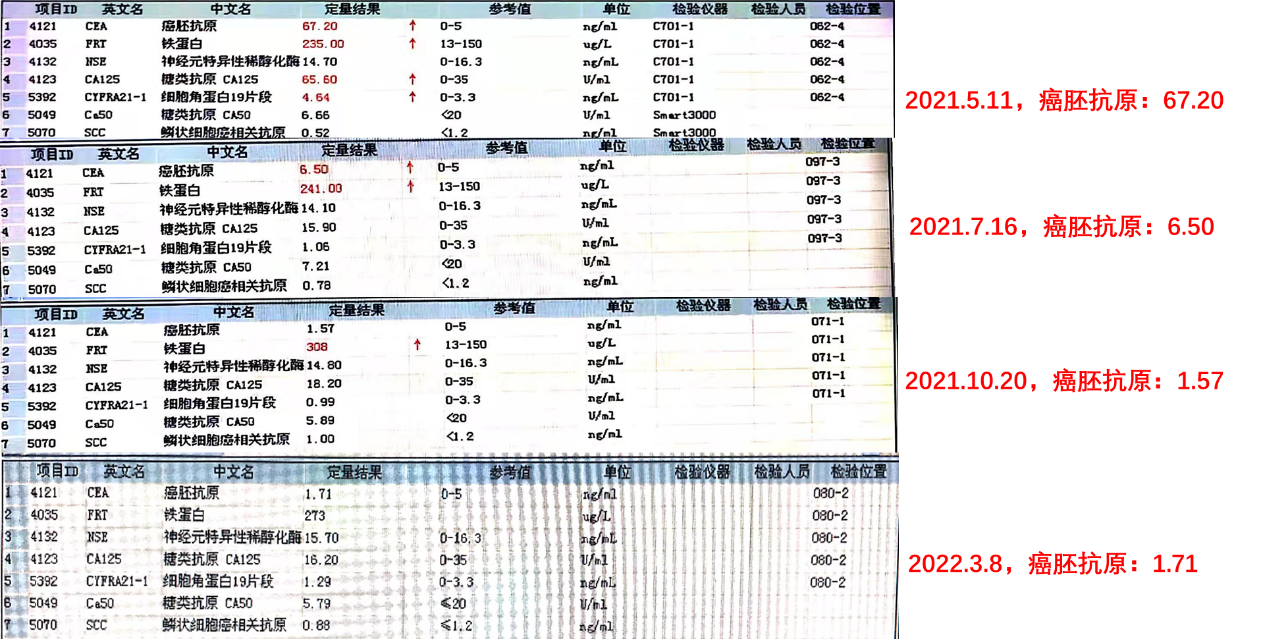
图2-6 治疗前后肿瘤标志物对照
患者老年女性,诊断为左肺下叶鳞癌,全身多处淋巴结转移及恶性心包积液,无手术机会,基因检测EGFR(-),ALK(-),ROS1(-),PD-L1表达55%,肿瘤标志物升高明显,肿瘤活跃度高。经过4周期治疗后,肿瘤明显缩小,疗效达PR。近期随访显示,替雷利珠单抗单药维持治疗至今患者恢复良好,无明显不适。
肺癌是全世界范围内发病率和死亡率第一的恶性肿瘤,每年全球新确诊超过200万例,死亡例数超过170万[1]。NSCLC是肺癌最主要的类型,近年来,基于免疫抑制剂在NSCLC中的临床研究、真实世界案例,免疫抑制剂越来越广泛地用于NSCLC的一线治疗、围术期治疗等,为广大NSCLC患者开启了希望之门。
在众多免疫抑制剂中,我国自研药物替雷利珠单抗的RATIONALE系列研究不断为其在NSCLC的治疗中提供可靠证据。其中RATIONALE 307研究结果显示[2],一线替雷利珠单抗联合紫杉醇/白蛋白紫杉醇+卡铂可为晚期鳞状NSCLC患者带来可观获益,两组mPFS均达7.6个月(化疗组为5.5个月),ORR分别提升至72.5%、74.8%(化疗组为49.6%)。RATIONALE 304研究结果显示[3],替雷利珠单抗联合培美曲塞+卡铂治疗ⅢB~Ⅳ期非鳞状NSCLC患者的mPFS达9.7个月(化疗组为7.6个月),ORR显著提升至57.4%(化疗组为36.9%)。基于上述研究,替雷利珠单抗联合化疗已先后获批晚期鳞状与非鳞状NSCLC一线治疗适应症,该药也是目前国内唯一获批联合白蛋白紫杉醇+卡铂方案用于晚期肺鳞癌的PD-1单抗。此外,替雷利珠单抗亦成功纳入国家医保药品目录。
新辅助免疫治疗的理论基础是免疫抑制剂将原位肿瘤细胞转变为“自体疫苗”,从而激活抗肿瘤免疫反应,同时,活化的T细胞通过血管和淋巴管到达微病灶,引发更大范围的抗肿瘤免疫反应[4]。已有相关研究证实免疫新辅助联合化疗能够为可切除患者带来获益,目前,替雷利珠单抗用于NSCLC辅助/新辅助治疗的Ⅲ期临床研究RATIONALE 315正在进行中[5]。此外,RATIONALE系列研究也证实,NSCLC患者不限于PD-L1表达,均能从替雷利珠单抗联合化疗方案中获益。
病例一患者为右上肺腺癌Ⅲb期,由于EGFR为野生型,不适用于EGFR-TKI靶向药物,PD-L1高表达,可选用PD-1免疫抑制剂。经过MDT会诊,考虑手术难度较大,因而先行替雷利珠单抗联合化疗新辅助治疗,3个周期后明显缩瘤,疗效达PR,为手术创造了更有利的条件。手术顺利完成,术后评价为MPR,之后行替雷利珠单抗单药辅助治疗,全程用药超1年,随访患者无复发征象。
病例二患者为左下肺鳞癌Ⅳa期,PD-L1高表达,已不适于手术治疗,治疗计划为6周期替雷利珠单抗联合化疗,于4周期后复查疗效即达PR,在用药期间,由于化疗带来的胃肠道不适较严重,加之患者不愿继续接受化疗,方案调整为替雷利珠单抗单药维持治疗。后续复查显示患者持续缩瘤、肿瘤标志物持续降低,随访患者至今用药已逾1年,期间患者无严重不良反应。
本期分享的两例NSCLC患者的病情有诸多不同,相同之处是EGFR阴性、PD-L1高表达,替雷利珠单抗+方案分别用于围术期、一线治疗,疗效均达PR,不仅显示出该药对于鳞状、非鳞状两种不同病理分型NSCLC的优异效果,也显示出该药对于可手术、不可手术两种不同分期NSCLC的全能属性。在未来,期待免疫治疗有更多的临床研究能够为真实世界应用提供证据,为更多不同病理分型、不同分期NSCLC患者带来同样可观的获益、带来长生存的希望。

扫描二维码
查看更多精彩
参考文献:
[1] https://www.iarc.fr/faq/latest-global-cancer-data-2020-qa/
[2] Jie Wang , Shun Lu, et al. JAMA Oncol, 2021, 7(5): 709-717.
[3] Forde PM, Spicer J, Lu S, et al. AACR 2021, abstract CT003.
[4] Keung EZ, Ukponmwan EU, et al. Ann Surg Oncol, 2018, 25(7): 1814-1827.
[5] .
查看更多