查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





病例提供者:华中科技大学同济医学院附属同济医院 叶丛
点评专家:华中科技大学同济医学院附属同济医院 董凌莉
病例简介
患者男性,59岁。
主诉
口干眼干、活动后胸闷4年,再发加重2月。
病史
现病史
患者于2014年无明显诱因下出现口干、眼干,伴有活动后胸闷、气促、咳嗽、咳痰,无咯血、胸痛等,于外院行唇腺活检、肺部CT等检查,诊断为干燥综合征(SS)、间质性肺病(ILD),给予泼尼松(50 mg逐渐减量)、硫酸羟氯喹、雷公藤多甙 、环磷酰胺(累计5.8 g )等治疗。
2017年9月患者活动后胸闷、咳嗽较前加重,将激素由每日5 mg加量至30 mg,免疫抑制剂调整为环孢素50 mg bid 、沙利度胺50 mg qn,治疗后胸闷、咳嗽症状较前无好转。
2018年2月患者出现咳嗽、咳黄色痰,伴有间断发热,最高体温为40℃,活动后胸闷较前加重,无胸痛、潮热、盗汗、消瘦、咯血等,来我院呼吸科就诊,查胸部CT提示间质性肺炎(较前2016年6月6日进展)合并感染。给予头孢曲松他唑巴坦+莫西沙星+伏立康唑抗感染治疗。患者未再发热,咳嗽咳痰较前好转,但胸闷较前无明显改善。
为求进一步治疗就诊风湿科,于2018年4月门诊以“SS”收入住院治疗。 起病以来,患者精神、饮食可,睡眠欠佳,大小便尚可,体力下降。
既往史
2016年6月,因甲状腺滤泡状癌行甲状腺全切术,术后予以左甲状腺素钠片治疗。
体格检查
体温:36.7°C,脉搏:76bpm,呼吸:20bpm,血压:102/66 mmHg。神志清楚,精神欠佳,查体合作;全身皮肤黏膜无黄染;浅表淋巴结无肿大,颈软,可见一长约5 cm手术瘢痕;双肺呼吸音粗,双下肺可闻及velcro啰音;心率63bpm,律齐,各瓣膜区未及病理性杂音;腹平软,全腹无压痛及反跳痛,肝脾胁下未触及,双下肢无水肿。
辅助检查
(2014年南昌大学第一附属医院)唇腺活检:下唇唇腺镜检涎腺呈分叶状结构,腺泡间质内灶状淋巴细胞浸润,涎腺小叶间血管扩张、充血;另可见少许横纹肌组织。
胸部CT:两肺间质性肺炎,两下肺胸膜囊状改变,考虑间质纤维化及肺大泡形成。
(2018年4月我院):类风湿全套+风湿全套+免疫全套:ANA 1:320,余阴性;超敏CRP:30.93 mg/L;血沉:13 mm/h。
肺部CT(2016年6月2日,图1):两肺多发囊状透亮区,以两下肺为著;两肺小叶间隔增厚,血管纹理呈网格状改变,以两下肺为著。诊断意见:肺气肿,两肺间质性炎。
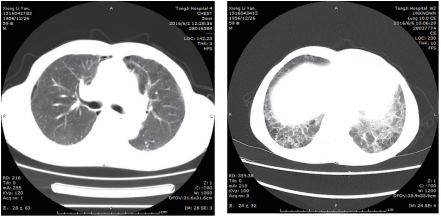 图1 肺部CT(2016-6-2)
图1 肺部CT(2016-6-2)
2018年4月9日肺部CT示双肺间质性肺炎,较前进展(图2)。
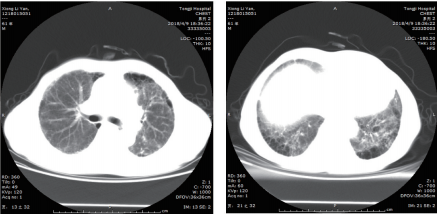 图2 肺部CT(2018-4-9)
图2 肺部CT(2018-4-9)
诊断
1、SS合并ILD
2、甲状腺全切术后
治疗方案及理由
1、免疫抑制治疗
对原发性干燥综合症(pSS)的理想治疗不仅是要缓解患者口、眼干燥的症状,更重要的是终止或抑制患者体内发生的异常免疫反应,保护患者脏器功能,并减少淋巴瘤的发生。pSS的治疗包括3个层次:①涎液和泪液的替代治疗以改善症状;②增强pSS外分泌腺的残余功能,刺激涎液和泪液分泌;③系统用药抑制免疫反应。而本例患者局部干燥症状已基本缓解,但由于累及肺脏是导致患者死亡的危险因素之一,因此,治疗的主要目标为控制肺间质病变。既往研究表明他克莫司具有抗肺纤维化作用,且可改善结缔组织相关间质性肺病(CTD-ILD)的肺功能[Pulm Pharmacol Ther 2016,36(10):46-52]。因此,治疗方案为口服泼尼松(40 mg/d起始并逐渐减量)+他克莫司1 mg q12h。
2、预防药物副作用的辅助治疗
护胃、补钙。
3、甲状腺方面用药
左甲状腺素钠片。
4、抗纤维化治疗
吡非尼酮。由于该患者肺部病变较前进展,有散在的纤维出现,因此联用吡非尼酮。近年来,以吡非尼酮为代表的新型小分子抗纤维化药物在特发性肺纤维化(IPF)的多项国际多中心随机双盲对照研究中被证实可以延缓肺功能恶化,延长无疾病进展生存时间;目前已有个案报道和队列研究的亚组分析显示,应用吡非尼酮有可能改善系统性硬化症( SSc)相关 ILD患者的肺功能[Sarcoidosis Vasc Diffuse Lung Dis 2014,31(3):235-238]。
治疗效果
曾于治疗近3个月时复查肺部CT,间质性肺炎无明显进展。治疗4个月时电话随访,患者症状基本稳定,胸闷喘气未加重。随后每1个月进行电话随访至今,患者症状基本稳定。
病例思考
该患者为中老年男性,有明确的SS及肺间质病变病史。在既往的治疗中患者应用过糖皮质激素、环磷酰胺、硫酸羟氯喹、雷公藤多甙、环孢素、沙利度胺等药物,似乎反应欠佳,出现反复肺部感染及肺间质病变的进展。这其中可能有患者的个人原因(未规律用药)及对药物反应不佳等多种原因。而目前患者的治疗要兼顾原发病(激素+免疫抑制剂)及感染,两者如天平的两端,需要我们权衡利弊寻找平衡,如同钢丝上的舞蹈。环磷酰胺作为一种烷化剂,是现有最有效的免疫抑制疗法之一,但其长期及短期的毒副作用不容忽视。该患者目前肺部病变广泛且近期出现过严重肺部感染,再次使用环磷酰胺有免疫抑制下感染加重的风险。而他克莫司作为钙调磷脂酶抑制剂的一种,目前有研究显示其有抗肺纤维化的作用,这使得他克莫司可能是SS-ILD的又一选择。
专家点评 华中科技大学同济医学院附属同济医院 董凌莉
干燥综合征(Sjögren syndrome,SS)合并ILD的特点及发病情况
SS是一种慢性炎症性疾病,特征为泪腺及唾液腺功能减低,并伴有淋巴细胞浸润外分泌腺(尤其是泪腺和唾液腺)。除了引起干眼(干燥性角膜结膜炎)和口干(口干燥症)之外,SS还可以影响皮肤、肺、心脏、肾、神经及造血系统等腺外器官系统。按照是否伴发有其他结缔组织病又分为原发性干燥综合征(pSS)和继发性干燥综合征(sSS)。ILD是SS的最常见肺部异常。SS-ILD在女性中比在男性中常见,中位发病年龄为60岁。相比于sSS患者,ILD似乎在pSS患者中更常见。但pSS相关ILD的严重程度往往低于sSS相关或其他风湿性疾病相关ILD。
SS合并ILD的治疗
SS相关肺部疾病的治疗策略多是经验性,因为尚未进行相关对照研究。治疗方法基于识别出的肺部病理学表现,以及症状、生理功能障碍的严重程度和放射影像学检查所示病变范围。通常采用口服糖皮质激素启动治疗,免疫抑制剂方面目前有相关的小规模研究应用硫唑嘌呤、吗替麦考酚酯、环磷酰胺和环孢素等药物。他克莫司为钙调磷脂酶抑制剂,既往有报道证实FK506(他克莫司胶囊)可抑制肺部和皮肤胶原的合成及TGF-β1受体表达的作用,具有潜在的抗肺纤维化的作用。目前已有一些小规模的研究及病例报道显示他克莫司在皮肌炎相关的肺间质病变治疗中应用的优势[Rheumatology(Oxford) 2015,54(1):39-44]。
该例患者的特殊性
该患者为中老年男性患者,病史较长,在既往治疗过程中应用过多种免疫抑制治疗,虽pSS基本得到控制,但ILD持续进展,患者在在治疗过程中发生反复的肺部感染,因此,如作者所言,该患者的治疗如同钢丝上的舞蹈。根据2018年中国结缔组织病相关ILD诊疗专家共识,对于结缔组织病缓解而ILD进展的患者,在结缔组织病维持缓解的基础上,需加强针对ILD的治疗,如糖皮质激素联合免疫抑制剂,适时尝试联合吡非尼酮等抗纤维化药物。该患者肺部病变较弥漫且前期合并肺部感染,考虑到长期应用糖皮质激素相关的感染、血糖及血压、骨质疏松的问题不容忽视,而在免疫抑制剂方面,环磷酰胺等药物有较强的免疫抑制作用,有加重感染的风险。目前已有他克莫司在炎性肌病相关的肺间质病变方面的应用,一些临床医生尝试在抗黑色素瘤分化相关基因5(MDA-5)抗体阳性的炎性肌病并合并肺部感染患者中应用他克莫司,并取得了成功[Curr Rheumatol Rep 2012,14(3):264-74]。因此,对该例患者他克莫司可以作为一种新的尝试。
查看更多