查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





2021年欧洲肿瘤内科学会免疫肿瘤学(ESMO IO)年会于2021年12月8日至11日隆重召开。作为世界上最盛大的免疫肿瘤学会议之一,年会将汇集众多世界一流的肿瘤学专家学者,向全世界肿瘤医务工作者分享肿瘤免疫治疗这一热门领域最新进展。
今日北京时间下午5点(日内瓦时间上午10点),由天津医科大学肿瘤医院食管肿瘤微创外科主任姜宏景教授牵头的一项帕博利珠单抗联合新辅助化疗及手术治疗局部晚期食管鳞癌的单中心、单臂II期临床试验KEYSTONE-001的期中分析结果以LBA(Late-breaking Abstract)的形式在ESMO-IO首次公布,并引起业内强烈关注。本次结果由第一作者天津医科大学肿瘤医院食管肿瘤微创外科尚晓滨教授代表研究团队进行大会演讲并接受现场问答。
KEYSTONE研究是由研究者发起的一系列探索帕博利珠单抗应用于中国食管鳞癌围手术期治疗的前瞻性临床研究。其中,KEYSTONE-001研究为单臂、单中心、开放性,预计纳入50例受试者,是全球首个评价帕博利珠单抗联合紫杉醇及顺铂新辅助治疗局部晚期(AJCC III期)食管鳞癌安全性和有效性的前瞻性临床研究,主要研究终点为主要病理缓解(major pathological response,MPR)和安全性。
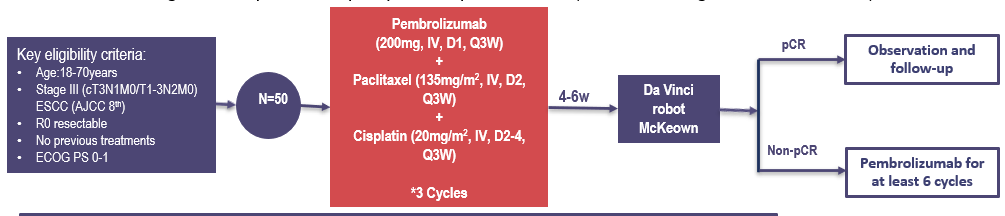
KEYSTONE-001研究设计
截至目前,按照流程29例患者进入期中分析阶段,已完成新辅助治疗后4-6周内接受机器人Mckeown根治术,(其余13例即将手术),结果显示:所有患者均为R0切除,术后病理示帕博利珠单抗联合紫杉醇及顺铂的MPR率高达72.4%(21/29),包括12例病理完全缓解(ypT0N0, 41.1%)和17例达到ypT0(58.6%)的患者。
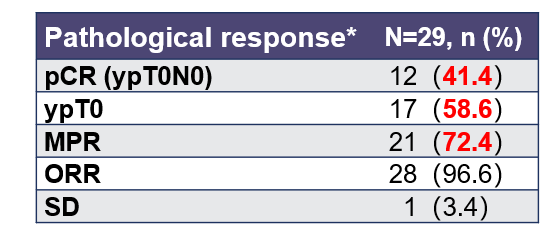
病理缓解情况
新辅助治疗期间的安全性良好,所有患者均如期完成方案规定的3个周期联合治疗,且无3级及以上免疫相关不良反应发生。生活质量评分(EORCT QLQ-C30及EORCT QLQ-OES18)显示新辅助治疗后患者的功能和症状均明显改善。
另外值得庆贺的是,同样由姜宏景教授和中国医学科学院肿瘤医院食管外科主任李印教授共同牵头开展的帕博利珠单抗联合新辅助化疗及手术对比新辅助同步放化疗及手术治疗局部进展期食管鳞癌的多中心、前瞻性、随机、对照Ⅲ期临床试验——KEYSTONE-002的研究设计也在ESMO IO大会以壁报形式展示。
为此中国医学论坛报特邀姜宏景教授接受专访,为读者详尽解析研究结果,并就该研究对于国内当前和未来食管癌诊疗及临床实践意义分享个人观点。
姜宏景 教授
天津医科大学肿瘤医院食管肿瘤微创外科行政主任
主任医师 医学博士
中国抗癌协会食管癌专业委员会秘书长、委员
中华医学会胸心血管外科分会食管疾病学组委员
中国医师协会胸外科医师分会食管外科专家委员会委员
中华全科医师协会全国贲门癌专业委员会常委
天津市抗癌协会食管癌专业委员会副主任委员
天津市抗癌协会肿瘤微创治疗专业委员会副主任委员
天津市医师协会胸外科分会常委
中国医师协会医学机器人医师分会第二届委员会常务委员
多学科综合治疗成为主流
免疫治疗或可为食管癌围术期
增添获益
Q1:对于KEYSTONE-001的试验设计,您当初是如何考虑的?
姜宏景教授:我国食管癌患者约占全世界的一半,严重危害人民健康和生活质量。不同于欧美国家,我国食管癌以鳞癌为主,国外相关研究较少,因此开展基于我国食管癌患者的临床研究至关重要。随着各种瘤种的临床研究不断进展,肿瘤诊疗已逐渐进入以手术为中心的多学科综合治疗模式,然而,食管癌在这一模式中的进展相对缓慢。
CROSS研究对食管癌围手术期的多学科综合治疗模式进行了探索,发表之后使得更多食管癌领域的专家学者开始关注围手术期的综合治疗,包括辅助治疗和新辅助治疗,CROSS研究也因此成为食管癌治疗的里程碑。在此基础上,随着我国NEOCRTEC5010研究和CMISG1701研究在食管癌新辅助领域取得突破,新辅助治疗逐渐成为包括美国国家综合癌症网络(NCCN)指南和中国临床肿瘤学会(CSCO)指南推荐的局晚期食管癌治疗的新标准。
近年来,随着免疫治疗的发展,其在肿瘤进展各个阶段中的治疗优势逐渐被认知,相关研究从二线治疗到一线治疗不断推进,而免疫治疗在食管癌新辅助领域的研究仍较少。同时,既往以CROSS研究和NEOCRTEC5010研究为基础的新辅助同步放化疗方案,对患者术前的身体状态及手术影响较大。因此,天津医科大学肿瘤医院食管肿瘤微创外科团队考虑开展KEYSTONE-001研究,一项针对我国食管癌患者人群特征的单中心、单臂II期临床试验,也是全球首个探索帕博利珠单抗联合紫杉醇及顺铂新辅助治疗局部晚期食管鳞癌的有效性和安全性研究。
KEYSTONE-001研究结果可喜
稳步推进增强研究信心
Q2:在KEYSTONE-001研究的入组过程中,您的体会是什么?
姜宏景教授:研究伊始,由于免疫治疗应用于食管癌时间较短,对该方案的疗效和安全性还缺乏足够的经验。因此,在KEYSTONE-001研究开始阶段,入组速度缓慢,在第一个患者安全度过手术期后才入组下一个患者。然而,随着临床试验的不断推进,患者接受新辅助治疗后,肿瘤体积明显退缩,治疗过程中也表现出良好的安全性,进食、吞咽困难等症状显著改善,身体状态整体回升,我们的信心逐渐提升。截至目前,已有29例患者纳入期中分析,在完成新辅助治疗后4-6周内接受机器人Mckeown根治术,结果显示所有患者均为R0切除,术后病理提示帕博利珠单抗联合紫杉醇及顺铂的主要病理缓解(MPR)率高达72.4%,且治疗期间安全性良好,无3级及以上免疫相关不良反应。
目前来看,这种免疫联合化疗的方式,无论从安全性还是有效性方面,都表现出超预期的结果,值得进一步探索。
KEYSTONE系列研究持续开展
期待新辅助免疫联合化疗
改善患者预后
Q3:KEYSTONE-001的研究结果对于局部晚期食管癌的临床实践有何意义?
姜宏景教授:依据当前诊疗指南,放化疗仍是食管癌新辅助治疗的标准方案。然而,随着临床试验的不断推进,免疫联合化疗的新辅助治疗方案显示出可以降低手术难度、减少不良反应等趋势,有望改善食管癌患者的预后。相信更多循证医学证据的出现,术前免疫联合化疗的新辅助治疗模式具有前景。
此外,KEYSTONE-001的研究结果增强了我们开始KEYSTONE-002研究的信心。KEYSTONE-002研究是一项关于帕博利珠单抗联合化疗新辅助治疗对比新辅助同步放化疗治疗局部进展期食管鳞癌的多中心、前瞻性、随机、对照III期临床试验。不同于KEYSTONE-001研究是单臂研究,KEYSTONE-002研究引入术前同步放化疗作为对照组,研究结果更为可靠。KEYSTONE-002研究计划进行两年,入组342例患者,随机分为治疗组(免疫联合化疗)和对照组(同步放化疗),治疗后进入手术阶段。目前,全国共17家中心有意参与KEYSTONE-002研究,自今年5月起各中心已相继开始申请研究方案和伦理许可。随着工作的推进,已有6家中心获得学术和伦理批准。
基于KEYSTONE-001研究的出色结果,我们对KEYSTONE-002研究充满期待。如果最终研究证明免疫联合化疗的疗效优于同步放化疗,且能有效降低不良反应、减少手术风险,无疑有望改写食管癌新辅助治疗格局,因此KEYSTONE系列研究极具研究前景和价值。
最后,在我们共同期待KEYSTONE-002研究结果的同时,也欢迎更多的同道能参与其中,为广大食管癌患者提供更为前沿的治疗手段,也为改善我国食管癌患者生存预后共同努力。
审批号:MI- PD1-2318-CN
免责声明:
本资讯由默沙东医学团队编辑提供,旨在用于医学专业人士间的学术交流,请勿随意转发或转载。文中相关内容不能以任何方式取代专业的医疗指导,也不应被视为治疗建议。医学专业人士对文中提到的任何药品进行处方时,请严格遵循该药品在中国批准使用的说明书。默沙东不承担相应的有关责任。
查看更多