查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





2019年9月8日,第20届世界肺癌大会(WCLC)召开第2天,来自世界各国的肺癌专家和学者继续针对肺癌和胸部肿瘤领域最新研究成果进行学术探讨和交流,为大家呈现了一场场精彩绝伦的“饕餮设宴”。其中在寡转移疾病专场,专家们具体针对肺部寡转移病灶的临床治疗策略问题进行了深入探讨。众所周知,立体定向放射治疗(SBRT)可能会刺激先天性和适应性免疫以增强机体对免疫治疗的反应。多点位SBRT是治疗转移性肿瘤疾病的新兴模式,对于低肿瘤负荷的患者而言,抗PD-1治疗效果会更佳。因此,在当今免疫治疗时代,SBRT联合免疫治疗会擦出怎样的火花?两者的联合能否进一步提高肺部寡转移患者的疗效,延长预后呢?
研究一
澳大利亚墨尔本大学彼得·麦卡勒姆癌症中心的Shankar Siva教授口头汇报了,对于肺部寡转移病灶帕博利珠单抗(Pembrolizumab)联合立体定向消融放疗(SABR)安全性的研究结果。该研究基于RAPPORT这一前瞻性研究,入组了其中ECOG评分0~1分且至少存在1个肺部寡转移病灶的患者。拟给予每个寡转移灶单次20 Gy放疗,并于结束后5天开始给予8周期帕博利珠单抗免疫治疗,200 mg/次,每3周给药1次。如果评估患者SABR放疗计划不能满足一般剂量限制要求,则更改为:30 Gy/3 fx,但应保证至少1个病灶接受SABR,并于放疗开始后的5~7天给予帕博利珠单抗免疫治疗,用药剂量同前。研究主要观察终点为安全性。

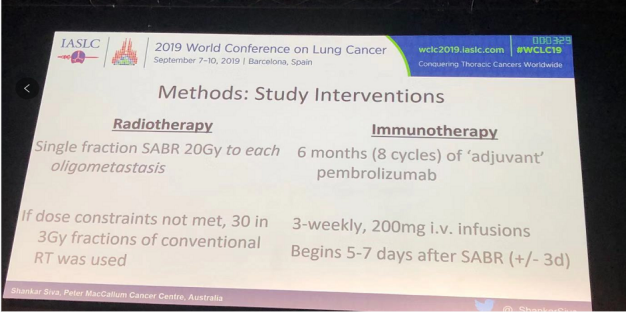
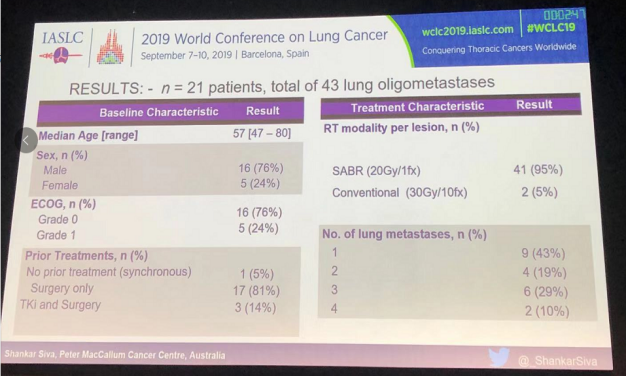
截至数据公布之时,该研究纳入了21例患者,共对43个肺部寡转移病灶进行治疗,其中41个病灶给予了20 Gy/1 fx的放疗模式,仅有2个病灶给予了30 Gy/10 fx的放疗模式。患者的基线特征如下图所示。
 目前,已有12例患者完成了全部8周期帕博利珠单抗免疫治疗,4例患者仍在治疗当中,2例患者因疾病进展退出研究。治疗相关不良事件分析结果表明:在接受帕博利珠单抗治疗3、6及7周期后,3例患者出现3级肺炎并退出研究。4例患者出现了治疗相关的3级不良事件,其中3例与放疗及免疫治疗均相关,1例仅与免疫治疗相关。并且这4例患者中的3例均出现了3级肺炎。此外,3例患者出现了2级治疗相关的不良事件,8例患者出现了1级治疗相关的不良事件。未见4、5级不良事件发生。5例患者未出现任何不良事件。
目前,已有12例患者完成了全部8周期帕博利珠单抗免疫治疗,4例患者仍在治疗当中,2例患者因疾病进展退出研究。治疗相关不良事件分析结果表明:在接受帕博利珠单抗治疗3、6及7周期后,3例患者出现3级肺炎并退出研究。4例患者出现了治疗相关的3级不良事件,其中3例与放疗及免疫治疗均相关,1例仅与免疫治疗相关。并且这4例患者中的3例均出现了3级肺炎。此外,3例患者出现了2级治疗相关的不良事件,8例患者出现了1级治疗相关的不良事件。未见4、5级不良事件发生。5例患者未出现任何不良事件。
该研究的近期疗效分析结果表明:1例患者达到完全缓解(CR),6例为部分缓解(PR),4例为稳定(SD),5例为进展(PD),ORR为44%,DCR为69%。
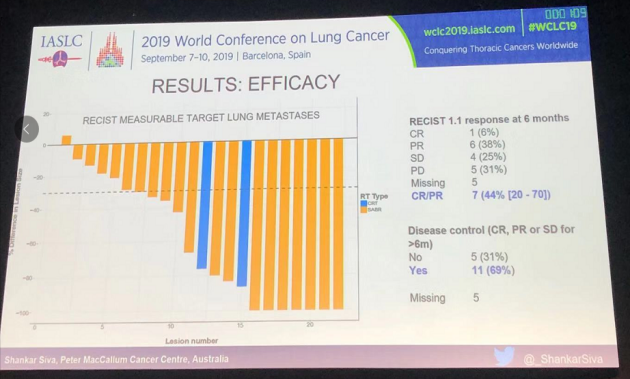 研究结果提示:在临床实践中,对于肺部寡转移病灶进行SABR联合帕博利珠单抗免疫治疗的毒副反应是可以耐受的。相比于既往所报道的帕博利珠单抗单药所引起的3级肺炎发生率,两者联合所致3级肺炎发生率是可以接受的。
研究结果提示:在临床实践中,对于肺部寡转移病灶进行SABR联合帕博利珠单抗免疫治疗的毒副反应是可以耐受的。相比于既往所报道的帕博利珠单抗单药所引起的3级肺炎发生率,两者联合所致3级肺炎发生率是可以接受的。
研究二
美国埃默里大学Winship肿瘤中心的Sibo Tian教授口头汇报了,针对肺部有限转移病灶,SBRT联合免疫治疗的安全性和毒性的研究结果。该项研究目的是评估肺部SBRT同步联合免疫治疗的安全性和耐受性。肺部SBRT和同步(30天内)免疫治疗的病人来自单一中心核证。仅进行SBRT治疗的病人作为对照组。SBRT相关急性毒性反应根据CTCAE标准评价定义,为30天内出现;亚急性是180天。
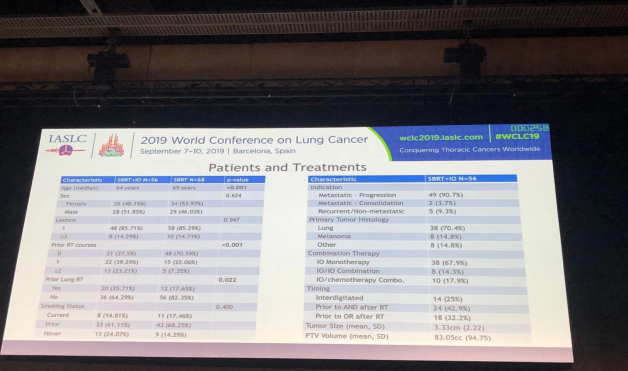
 该研究共纳入56个病人进行同步SBRT+ICI治疗, 68个病人进行SBRT未进行ICI治疗。SBRT+ICI组,中位年龄是64岁,中位随访时间为6.7个月。70.4%原发自肺部;14.8%为恶黑。90%进行了巩固治疗或者寡进展。62.5%的病人接受了既往放疗。35.7%的病人接受过肺部放疗。67.9%的病人接受过单药免疫治疗;17.9%接受过免疫联合化疗;14.3%接受过双免疫联合治疗。患者的基线特征如图所示。
该研究共纳入56个病人进行同步SBRT+ICI治疗, 68个病人进行SBRT未进行ICI治疗。SBRT+ICI组,中位年龄是64岁,中位随访时间为6.7个月。70.4%原发自肺部;14.8%为恶黑。90%进行了巩固治疗或者寡进展。62.5%的病人接受了既往放疗。35.7%的病人接受过肺部放疗。67.9%的病人接受过单药免疫治疗;17.9%接受过免疫联合化疗;14.3%接受过双免疫联合治疗。患者的基线特征如图所示。
 SBRT+ICI组的G3级和任何级别的肺炎发生率为10.7%(SBRT:0%,P=0.007)和33.9%(SBRT:27.9%,P=0.472)。两组的中位复发时间为距离SBRT放疗结束3.4个月。急性G3+ AEs发生率,SBRT+IO为1.8%,SBRT组为0%。亚急性GE3+ AEs在SBRT+IO组为26.8%,在SBRT组为2.9%。
SBRT+ICI组的G3级和任何级别的肺炎发生率为10.7%(SBRT:0%,P=0.007)和33.9%(SBRT:27.9%,P=0.472)。两组的中位复发时间为距离SBRT放疗结束3.4个月。急性G3+ AEs发生率,SBRT+IO为1.8%,SBRT组为0%。亚急性GE3+ AEs在SBRT+IO组为26.8%,在SBRT组为2.9%。
G3级肺炎及任何级别肺炎发生率与免疫药物、免疫介入时间、既往放疗、既往肺部放疗、病变中心性、靶病灶数目及吸烟状态均无关。SBRT+ICI组,免疫联合免疫治疗增加任何肺炎的发生可能(62.5% 对 29.17%, P=0.04);但未增加3级肺炎发生率。
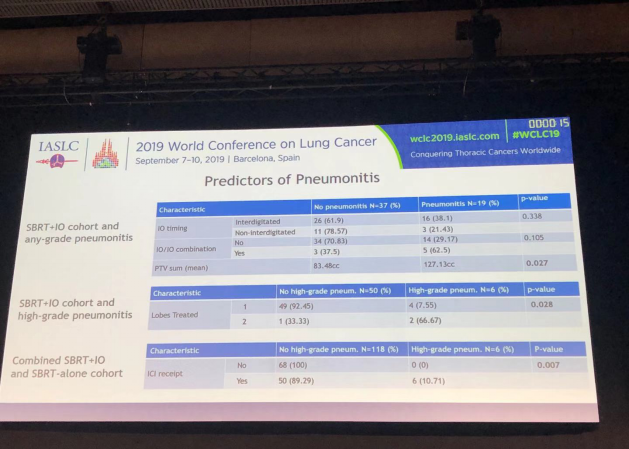
该研究结果提示:肺部SBRT同步ICI,特别是ICI/ICI联合能增加G3肺炎的发生率。然而,SBRT+ICI与SBRT相比,安全且可耐受。SBRT联合ICI的治疗模式需要进一步探索。
研究三
美国威斯康星大学卡本癌症中心T.Leal教授口头汇报了一项对非小细胞肺癌(NSCLC)寡转移患者的所有病灶行SBRT后联合德瓦鲁单抗+替西利姆单抗治疗的IB期研究的中期安全性结果分析。
既往研究证明立体定向放射治疗(SBRT)可改善免疫微环境;在临床前模型中,抗PD-1抗体联合放疗(RT)可改善抗肿瘤疗效。因此我们假设放疗(RT)诱导的肿瘤微环境效应将增强德瓦鲁单抗+替西利木单抗对非小细胞肺癌(NSCLC)寡转移患者的疗效。

主要研究终点:NSCLC寡转移患者所有病灶SBRT后德瓦鲁单抗+替西利姆单抗治疗的安全性和耐受性。首批队列包含3-6名患者,如果3位患者中2位出现≥3级毒性反应,停止替西利姆单抗治疗;如果3位患者中1位出现≥3级毒性反应则入组6名患者后再次评估,如果6名患者中多于2名出现≥3级毒性反应,停止使用替西利姆单抗治疗。次要研究终点:PFS,OS;探索性终点:肿瘤组织的PD-L1的表达和TMB;循环肿瘤细胞。

该IB期研究目前共入组21名患者NSCLC寡转移患者;对患者所有病灶行SBRT治疗(30~50 Gy/5 f)2周后行德瓦鲁单抗1500 mg和替西利姆单抗75 mg治疗,每4周一次,4个周期治疗后行每4周一次的德瓦鲁单抗维持治疗直至进展。入组患者有1~6个颅外转移灶,ECOG 0~1分,无驱动基因突变,未接受过免疫治疗;评估剂量限制性毒性(DLT)时间为第一次SBRT后直到首次免疫治疗结束后28天,期间为患者取血进行循环肿瘤细胞和流式细胞计数,并在SBRT后进行活检组织的PD-L1和TMB检测作为基线值。

2018年2月至2019年3月入组10名患者,中位随访时间:2.8个月(1.5~8.2个月),患者基线特征:中位年龄72岁(56~81岁),女性/男性3/7,鳞癌/非鳞癌2/8,治疗病灶中位数目2,主要毒性为1/2级毒性;2例患者在接受德瓦鲁单抗+替西利木单抗治疗前出现中枢神经系统进展并解除协议治疗;迄今为止,已有8例患者在SBRT后进行德瓦鲁单抗+替西利木单抗治疗;一个DLT为3级肝功能毒性(LFTs);另外一名患者在DLT期后解除协议治疗,包括3级LFTs、3级皮疹和4级血清磷酸肌酸激酶毒性。
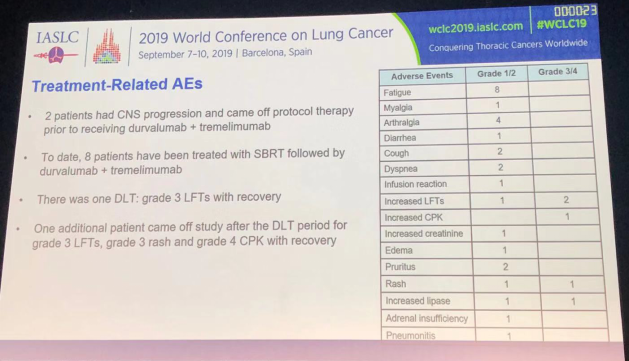
到目前为止,对于NSCLC寡转移患者,SBRT后德瓦鲁单抗+替西利木单抗治疗未出现新的可观测到的安全问题,方案可行;免疫介导的毒性副作用发生率似乎与既往研究一致;没有患者出现治疗部位病灶进展;最佳治疗顺序仍然是一个待解决问题;目前研究正在进行中,研究结果和生物标志物结果将在以后的会议中报告。
既往对于肺部寡转移病灶开展的Oli-GOMEZ、COMET、PEMBRO-RT、NRG-LU002以及LONESTAR等众多研究,充分证实了在全身抗肿瘤治疗的基础上,针对肺部病灶进行局部治疗的必要性。以上的临床数据也再次表明,对于肺部寡转移病灶的患者,SBRT联合免疫治疗毒副反应是可以耐受的,并且具有临床有效性。尽管如此,SBRT联合免疫治疗模式仍需要进一步探索,如两者联合顺序的排布,临床获益的预测生物标志物等。
撰稿 | 孟雪 发自西班牙巴塞罗那(山东省肿瘤医院)
查看更多