查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:郑州大学基础医学院 丁若琦
本文由郑州大学基础医学院的在读博士丁若琦与大家分享于2022年10月24日在线发表于Nature Communications的“Microglial debris is cleared by astrocytes via C4b-facilitated phagocytosis and degraded via RUBICON-dependent noncanonical autophagy in mice”一文。
研究背景
小胶质细胞在机体的全生命周期内持续性进行细胞更替。在此过程中,衰老的小胶质细胞死亡伴随着新生小胶质细胞的再生。如果死亡小胶质细胞所产生的碎片不能及时被清除,其将会在脑内大量积累引起中枢神经系统(CNS)功能紊乱,以及加速神经退行性病变的病理进程。此外,近年来研究发现通过抑制集落刺激因子1受体(CSF1R)等方式可在短时间内快速耗竭脑内超过99%的小胶质细胞。然而,在此过程中并未伴随大量的细胞碎片聚集,且检测不到炎症反应。由此可见,机体内存在高效的清除死亡小胶质细胞碎片的机制。因此,研究小胶质细胞碎片如何被清除对理解CNS的稳态维持和神经退行性病变机理至关重要。
研究目的
探索脑内吞噬小胶质细胞碎片的主要细胞,以及吞噬和降解小胶质细胞碎片的分子机制。
研究方法
构建小胶质细胞/巨噬细胞基因靶向小鼠模型(CX3CR1-CreER::Ai14 mice)。小胶质细胞基因靶向小鼠模型(P2Y12-CreER-GFP::Ai14 mice; P2Y12-CreER-GFP::DTA mice)。通过CSF1R抑制剂PLX5622耗竭脑内小胶质细胞,以在短时间内产生大量小胶质细胞碎片,同时通过免疫荧光染色排除少突胶质细胞及其前体细胞、周细胞、平滑肌细胞、神经元细胞、CNS巨噬细胞吞噬小胶质细胞碎片的可能,以及应用神经干细胞基因靶向小鼠模型(Nestin-GFP mice)排除神经干细胞对小胶质细胞吞噬可能。构建星形胶质细胞基因靶向病毒(AAV PHP.eB Gfap-mCherry);构建星形胶质细胞基因靶向小鼠模型(ALDH1L1-CreER::Ai14);以及星形胶质细胞标志物GFAP荧光染色确定星形胶质细胞(脑、视网膜和脊髓)和Müller胶质细胞(视网膜内特有的一类胶质细胞)具有小胶质细胞碎片吞噬能力。同时,通过低浓度他莫昔芬对P2Y12-CreER-GFP::Ai14和CX3CR1-CreER::Ai14进行稀疏标记,以此为方法发现小胶质细胞不能吞噬同源碎片。体外,提取小胶质原代细胞与星形胶质原代细胞。反复冻融获得小胶质细胞碎片,并应用PHrodo标记小胶质细胞碎片。观察体外星形胶质细胞吞噬小胶质细胞碎片能力。通过磁性细胞分选获得星形胶质细胞。荧光激活细胞分选出星形胶质细胞。运用单细胞转录组测序星形胶质细胞转录本,并应用定量PCR进行关键指标验证。用Bodipy染色法检测培养的星形胶质细胞内中性脂质的积聚。使用葡聚糖测定血脑屏障完整性。
研究结果
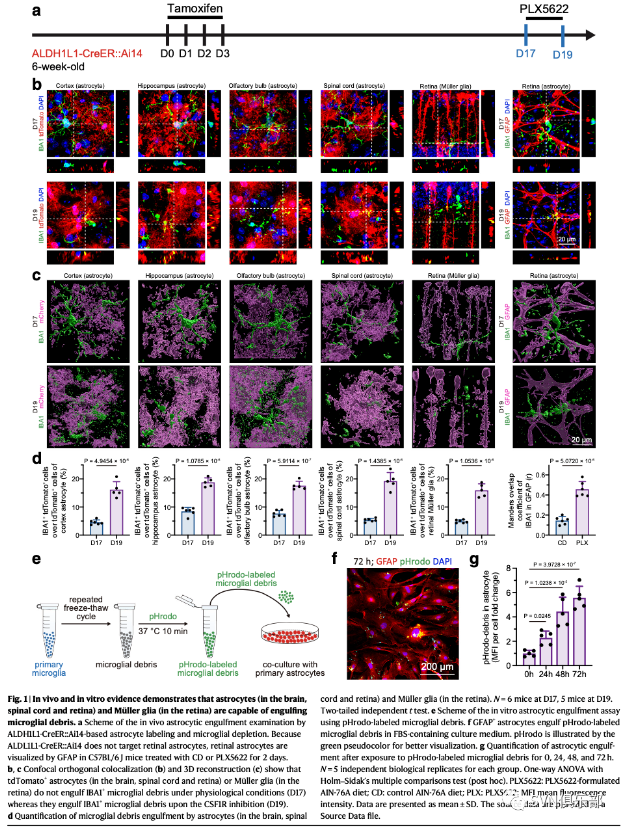
图1. 体内和体外证据表明,星形胶质细胞(大脑、脊髓和视网膜)和Müller胶质细胞(视网膜)能够吞噬小胶质碎片
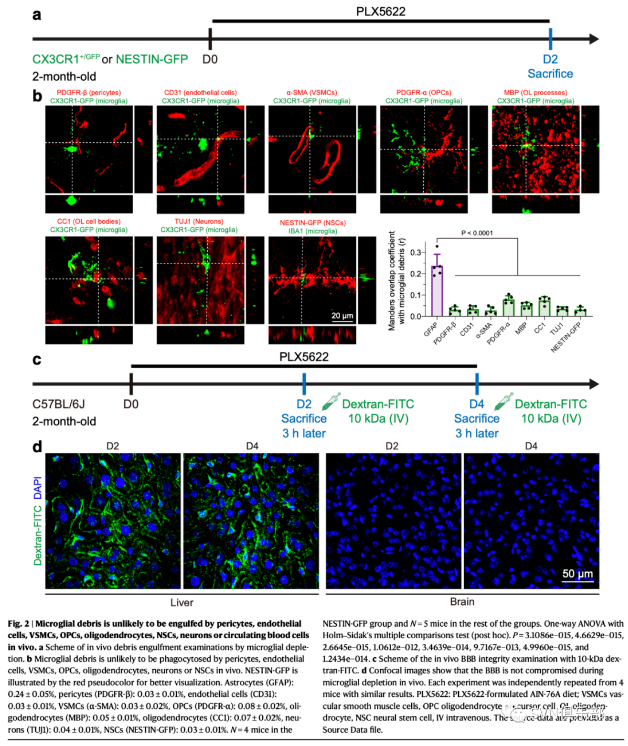
图2. 小胶质碎片在体内不可能被周细胞、内皮细胞、VSMCs、OPCs、少突胶质细胞、NSCs、神经元或循环血细胞吞没
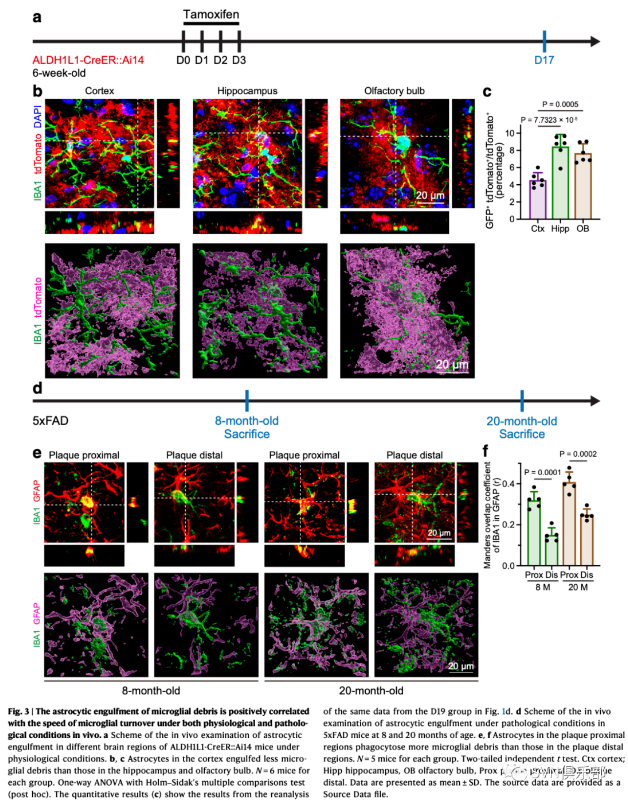
图3. 星形胶质细胞吞噬小胶质碎片与小胶质细胞周转速度呈正相关
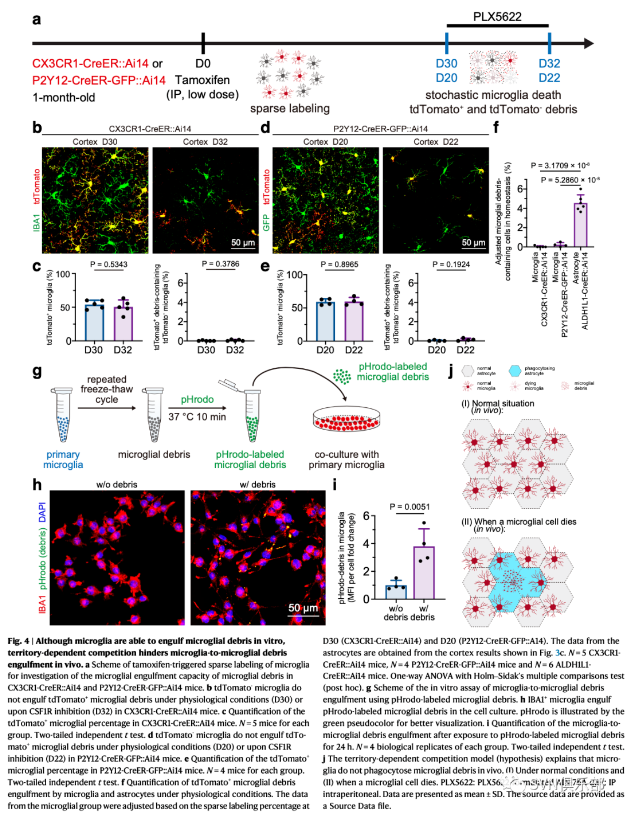
图4. 尽管小胶质细胞在体外能够吞噬小胶质碎片,但在体内,区域依赖性竞争阻碍了小胶质细胞对小胶质碎片的吞噬
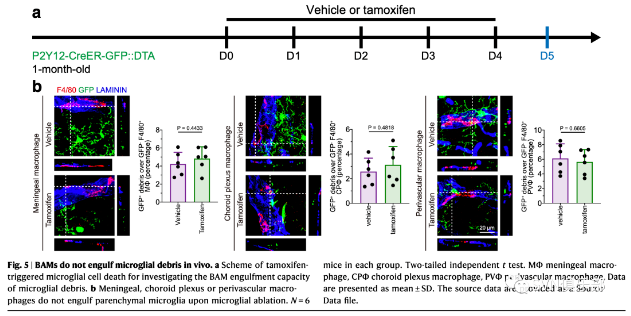
图5. BAMs不会吞噬体内的小胶质碎片
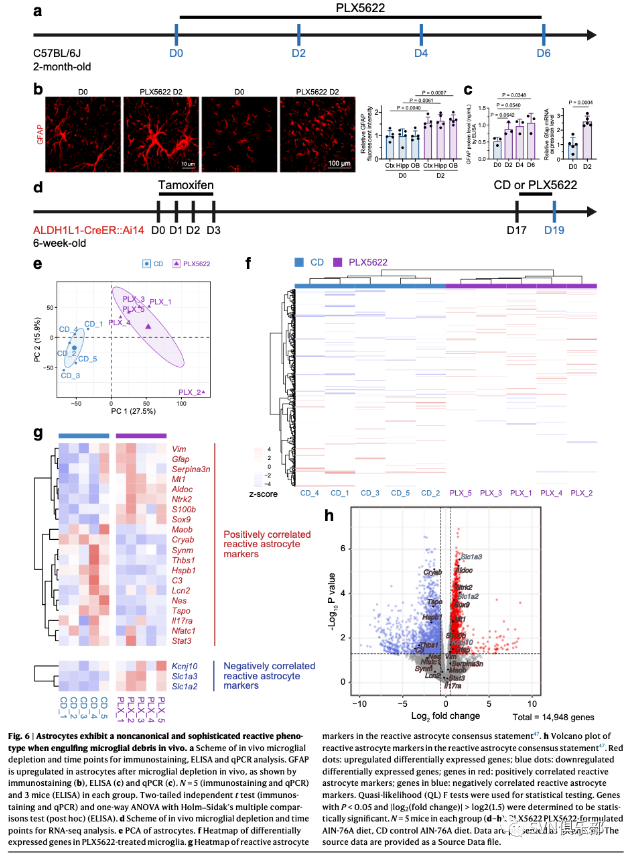
图6. 星形胶质细胞在吞噬体内小胶质碎片时表现出一种非典型性的复杂反应表型
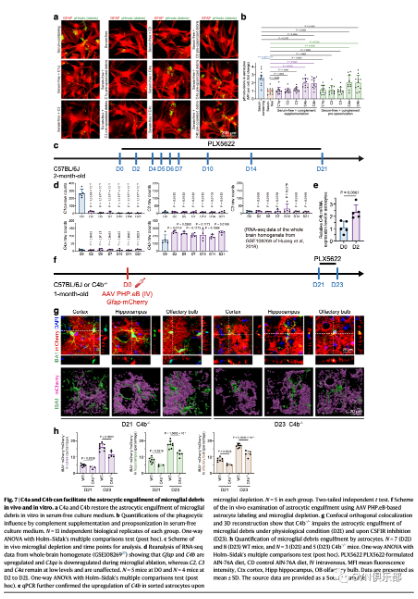
图7. C4a、C4b对星形胶质细胞吞噬小胶质细胞碎片的促进作用
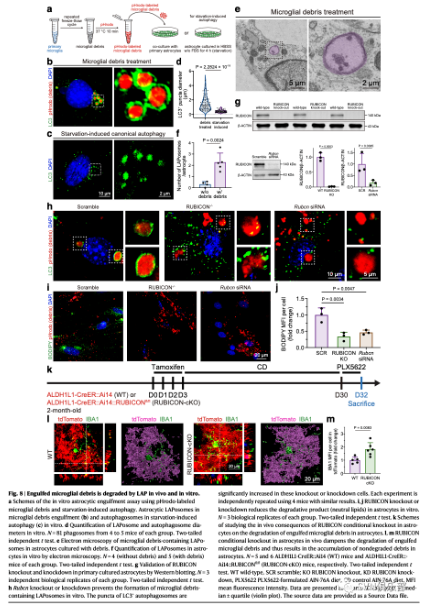
图8. 吞噬的小胶质碎片在体内外均被LAP降解
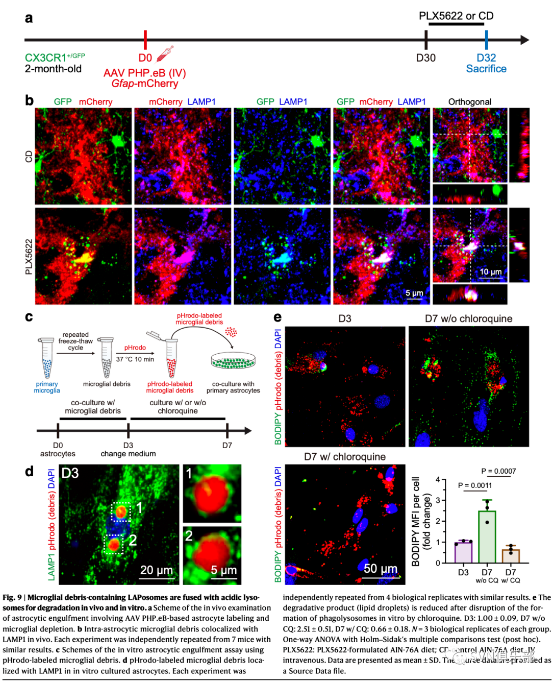
图9. 在体内和体外含小胶质碎片的LC3相关的吞噬小体与酸性溶酶体融合后降解
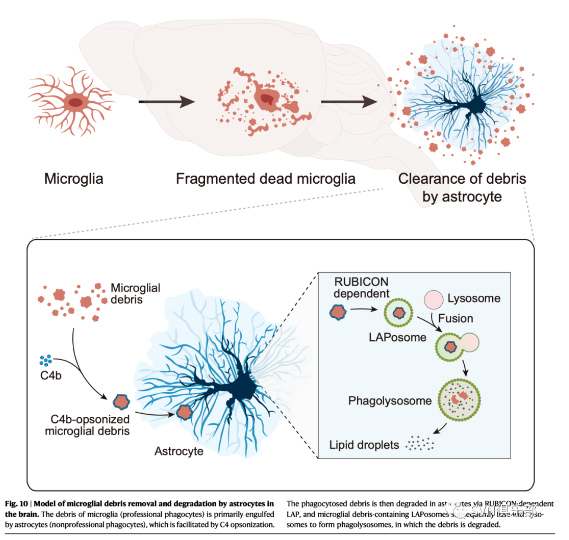 图10. 星形胶质细胞清除和降解脑内小胶质碎片的模式图
图10. 星形胶质细胞清除和降解脑内小胶质碎片的模式图

Q1:作者为何选择皮层、海马和嗅球来研究星形胶质细胞吞噬小胶质细胞碎片?
A1:赵恒教授认为大脑中有许多区域,不同区域的小胶质细胞、星形胶质细胞、神经元等具有不同的基因型和功能。另外,一篇文章难以解决所有问题,所以也有可能是作者团队选择这3个区域作为示例的缘由。David Wang教授认为这篇文章有可能是关注到这3个区域在生理状态下的小胶质细胞替换速度不同,比如小胶质细胞在皮层替换的速度是较慢的,在海马和嗅球中小胶质细胞替换速度较快,而星形胶质细胞吞噬碎片的速度与小胶质细胞替换速度相关。以及在5xFAD小鼠中,小胶质细胞替换速度加快,星形胶质细胞则表现出更快的吞噬碎片的速度。
Q2:为什么不共培养小胶质细胞与星形胶质细胞或小胶质细胞与其他细胞比较其吞噬功能?
汤耀辉教授指出文中用到简单的体外模型,即将小胶质细胞碎片加入到星形胶质细胞中。如果共培养小胶质细胞与星形胶质细胞,难点在于如何使小胶质细胞死亡,以及如何表明星形胶质细胞吞噬了小胶质细胞碎片。赵恒教授提出CSF1R抑制剂是否也能杀死体外的小胶质细胞?在体外实验中,如果能使小胶质细胞死亡,而非补充小胶质细胞碎片,能够更好地表示实验结论。王建教授补充,可以应用星形胶质细胞、少突胶质细胞、神经元等混合细胞共培养模型,观察小胶质细胞碎片是否主要被星形胶质细胞吞噬。
Q3:有什么方法可以在中枢神经系统中研究吞噬?
王建教授认为电镜是研究神经系统吞噬的金标准。
Q4:文中如何排除小胶质细胞对小胶质细胞碎片的吞噬作用?
王建教授认为,使用PLX5622后会杀死小胶质细胞,所以无法完全排除小胶质细胞吞噬小胶质细胞碎片的作用。另外,星形胶质细胞的吞噬功能是有限的。汤耀辉教授指出,文中应用了低剂量他莫昔芬稀疏标记法用以标记部分小胶质细胞,小胶质细胞耗竭前约有54%的小胶质细胞被tdTomato标记,小胶质细胞耗竭后约51%小胶质细胞tdTomato阳性,在PLX5622处理下,tdTomato+和tdTomato-小胶质细胞被相同的耗竭。如若存活的小胶质细胞能够吞噬小胶质细胞碎片(如tdTomato-小胶质细胞吞噬tdTomato+碎片),则应在tdTomato-小胶质细胞中观察到tdTomato+碎片。实验结果表明tdTomato-小胶质细胞中未检测到tdTomato+碎片,提示存活的小胶质细胞不吞噬小胶质碎片。王建教授补充,tdTomato-的小胶质细胞不一定是存活的小胶质细胞,可能正在死亡,不具有正常吞噬功能。文章缺乏小胶质细胞碎片的明确定义。
Q5:目前研究表明有“A1”和“A2”两种类型的星形胶质细胞,这篇文章中发挥吞噬小胶质细胞碎片功能的是哪种星形胶质细胞类型?
汤耀辉教授认为从文章中的RNA测序可以看出,在“A1”类型的星形胶质细胞中应该上调的基因呈现相反的趋势,表明文中观察到的发挥吞噬小胶质细胞碎片功能的星形胶质细胞表现出一种非经典的活化状态。王建教授补充,目前划分“A1”型和“A2”型星形胶质细胞的标记基因尚不明确,需要进一步研究探索。
Q6:文章结果涉及LAP和RUBICON,但讲者并未在背景中介绍相关内容
汤耀辉教授表示,讲者在结果部分提及了相关背景知识,但不够细致,建议青年科学家汇报时将重要的背景知识在研究背景部分进行阐述。
赵恒教授最后总结道,本次会议有许多同学提出了有意思的问题,是非常精彩的讨论,并鼓励更多的青年科学家参与讨论。王建教授认为,当阅读文献时遇到模糊的问题时,可直接向作者团队请教,因为他们对于实验设计和实验结果会有更为清楚的解释。

来源:SVN俱乐部
转载已获授权,其他账号转载请联系原账号
倾倒综合征(dumping syndrome)是什么疾病?怎么诊断和治疗?
扣带回癫痫(cingulate epilepsy,CE)是什么疾病?
王拥军教授 | 2022年神经病学10大研究进展,深入解读不容错过!
Neurology:取栓后CT发现造影剂渗出者更应该强化降压治疗?
查看更多