查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





一般资料:患者男性,75岁,于2020年10月12日就诊。
主诉:体检发现肺部阴影2月余。
既往史:血吸虫病史50余年,控制尚可。
个人史:吸烟史30年,已戒。
体格检查:无明显阳性体征。
实验室检查:血常规、血生化、肿瘤标志物无明显异常。
胸部CT(平扫+增强)检查(2020年10月13日): 左上叶尖段支气管新生物,如图1-1所示。
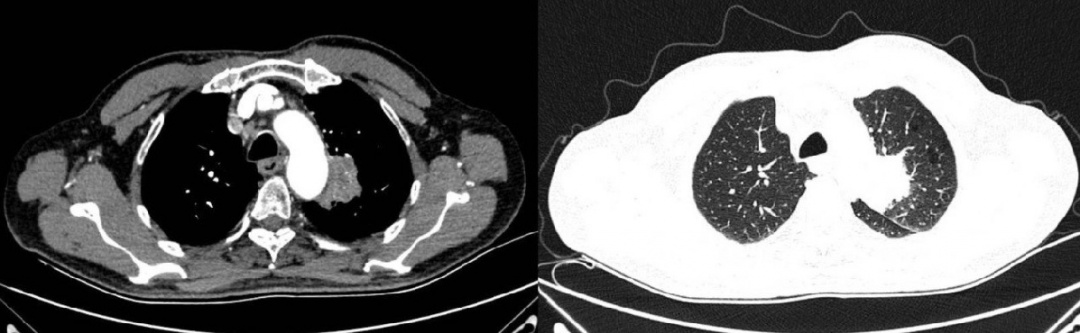
图1-1 治疗基线胸部CT
CT引导下经皮肺穿刺术病理(2020年10月19日):(左肺组织)鳞状细胞癌。
诊断:肺鳞状细胞癌(T3N3M0,Ⅲc期)。
一线治疗:免疫联合化疗
治疗方案:患者无手术指征,自2020年10月21日开始应用替雷利珠单抗+白蛋白紫杉醇+奈达铂方案治疗4周期(C1-C4),2021年2月5日调整为替雷利珠单抗单药免疫维持治疗,至今共完成9周期治疗(C5-C13)。
影像学及疗效评价:患者治疗期间定期复查胸部CT,见左肺上叶病灶持续缩小(如图1-2所示),疗效评估为持续PR。
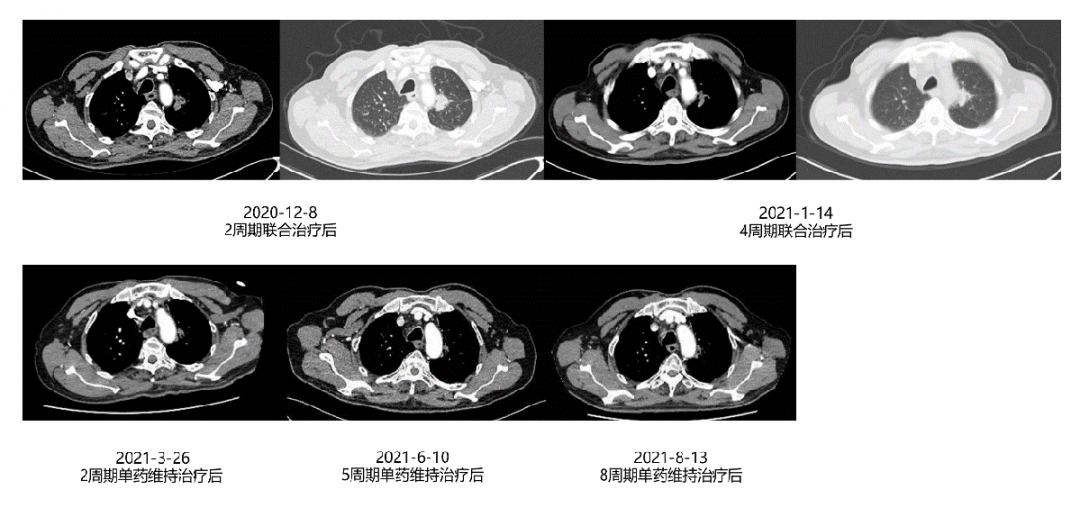
图1-2 治疗期间原发灶动态变化
安全性评价:无明显不良反应。
本例患者为老年男性,经临床诊断为Ⅲc期的肺鳞癌患者,无手术指征。患者无化疗禁忌和免疫相关疾病,经分析,建议选择免疫抑制剂联合化疗,2程治疗后临床症状明显缓解,病灶明显缩小,达到疗效PR,截至目前,已完成13周期治疗,仍保持PR疗效。治疗期间未见明显治疗相关不良反应,现仍在治疗及随访中。
一般资料:患者男性,64岁,于2020年7月26日就诊。
主诉:反复右侧背部疼痛1年,加重半月。
现病史:患者1年前无明显诱因出现右侧背部不适,呈阵发性针刺束带样疼痛,无明显放射痛,深吸气时明显加重,休息后稍缓解。2天前查胸部CT见前纵隔类圆形软组织密度影。
既往史、个人史及家族史:高血压病史1年,血压控制可;胆囊结石病史;脑梗死病史,无明显后遗症;余无特殊。
体格检查:右下肺呼吸音稍低;余无明显阳性体征。
实验室检查:血常规、血生化无异常,肿瘤标志物细胞角蛋白22.40ng/ml。
胸部CT(平扫+增强)检查(2020年7月27日):1.右前纵隔占位,考虑恶性病变,纵隔性肺癌或纵隔原发癌可能;并右肺叶间裂、右侧胸膜多发转移,纵隔内及右锁骨上窝多发淋巴结转移。2.右侧胸腔积液。3.左下肺条索影,考虑轻度慢性感染。4.所示肝多发囊肿。如图2-1所示。
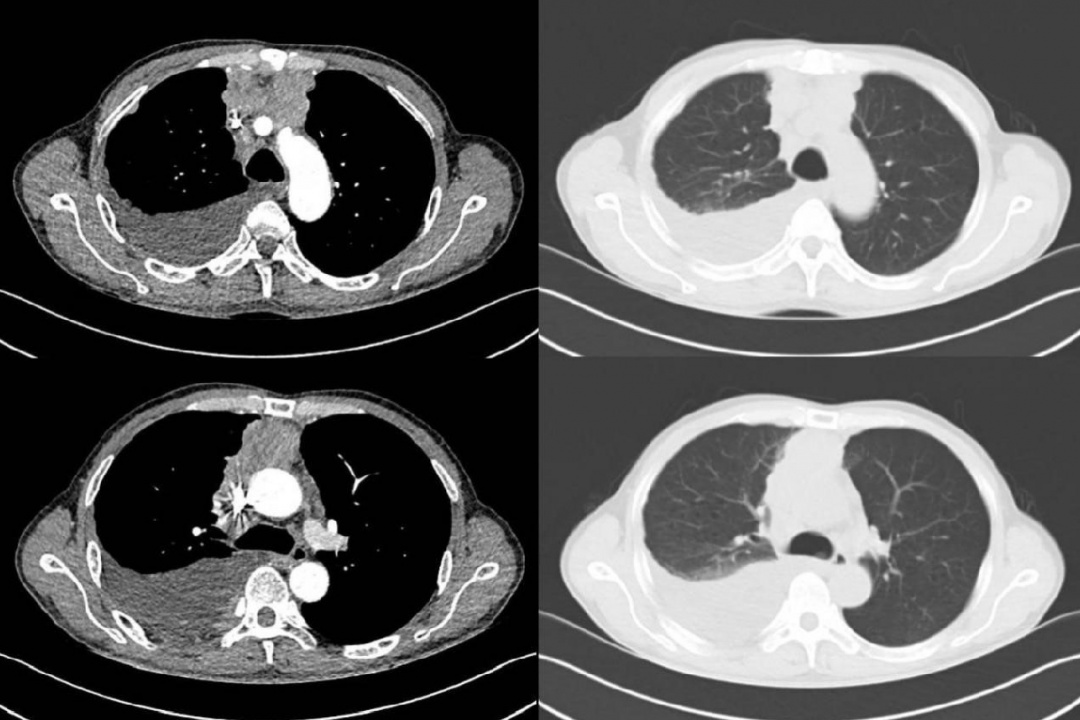
图2-1 治疗基线胸部CT
左锁骨上淋巴结穿刺细胞学及病理(2020年7月27日):考虑转移性癌(倾向低分化鳞癌),细胞蜡块有利于进一步诊断。
左锁骨上淋巴结穿刺细胞蜡块病理:检见鳞状细胞癌细胞。免疫组化示:P63(3+);P40(3+);CK5/6(3+);CR(-);CK7(-);NapsinA(-);TTF-1(-);Ki-67(癌细胞+);CD56(-)。
胸水细胞蜡块病理:检见癌细胞,结合免疫组化,考虑鳞状细胞癌。免疫组化示:CK(+);P63(+);P40(+);WT-1(-);TTF-1(-);Ki-67(5%+);Vimentin(-);D2-40(-)。
SPECT/CT检查(2020年8月4日):1.T12及L3代谢增高,骨转移不能排外;2.右侧第8-9前肋骨代谢增高,考虑骨折改变征象。
颅脑MR平扫检查(2020年8月3日):1.右侧侧脑室旁及左侧基底节区陈旧性病灶。2.缺血脱髓鞘脑改变。
诊断:肺鳞状细胞癌(T4N3M1c,ⅣB期)。
一线治疗:免疫+抗血管生成+化疗
手术方案:患者无手术指征,自2020年8月4日开始应用替雷利珠单抗+重组人血管内皮抑制素+白蛋白紫杉醇+奈达铂治疗,共4周期;其中第2周期因“反复发热1月余”停用替雷利珠单抗;4周期后因重度化疗后骨髓抑制,第5周期应用替雷利珠单抗+白蛋白紫杉醇治疗。自第6周期(2020年12月9日)开始规律应用替雷利珠单抗单药免疫治疗至今,共完成16周期治疗(C6-C16)。
影像学及疗效评价:患者治疗期间定期复查胸部CT(如图2-2所示),见原发肿块持续缩小,右侧胸腔积液逐渐吸收,疗效评估为持续PR。
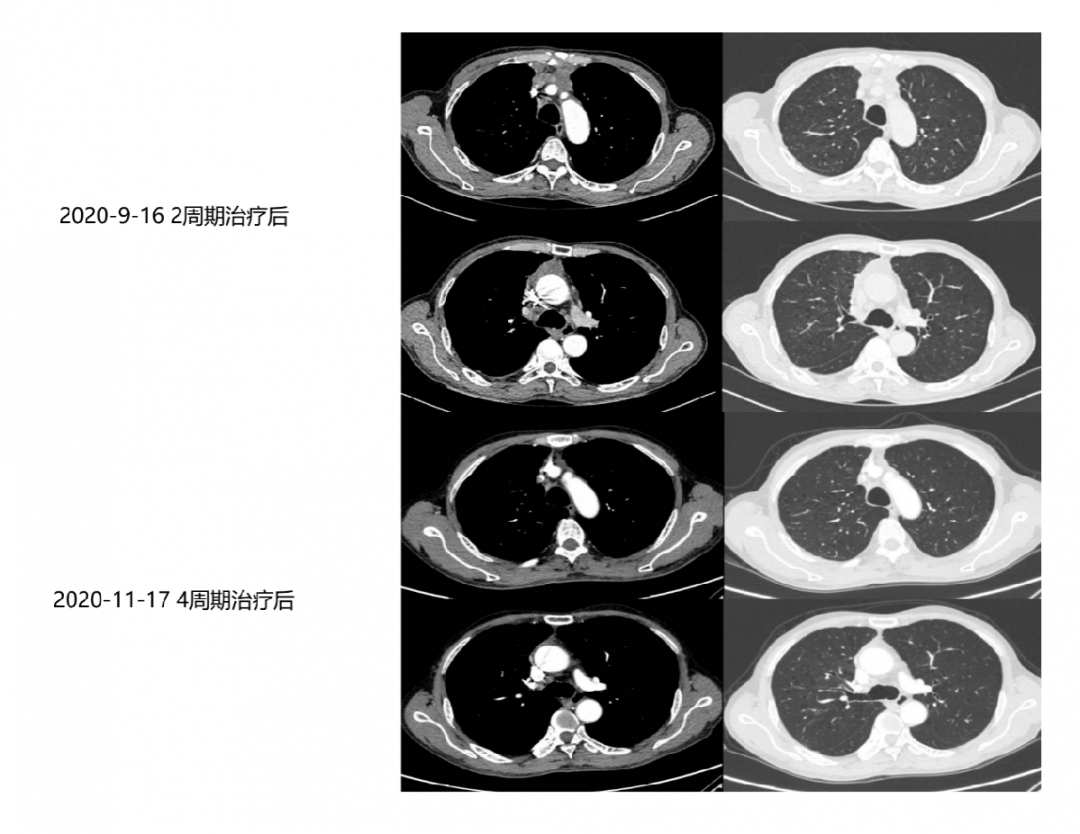
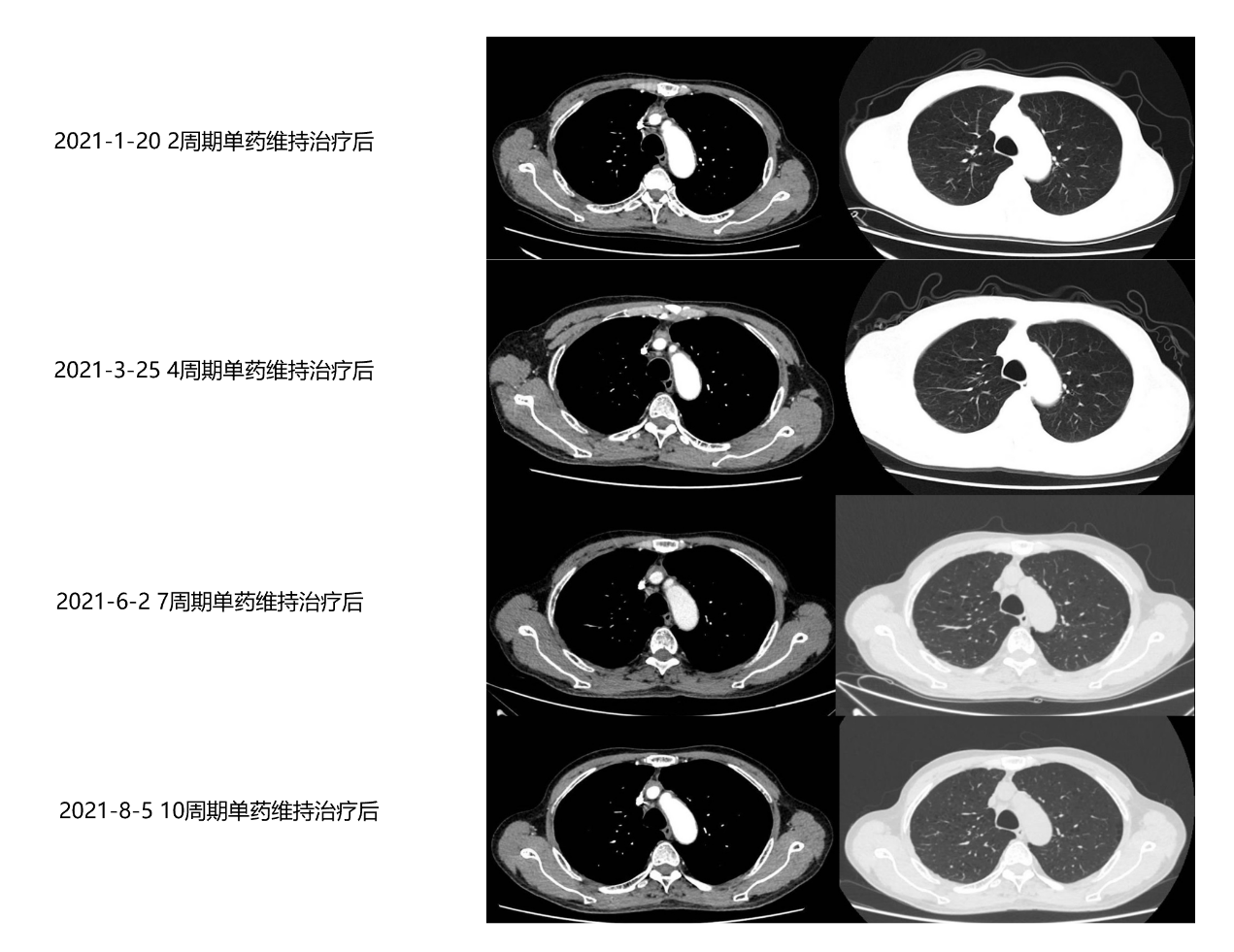
图2-2 治疗期间原发灶动态变化
安全性评价:患者化疗期间曾出现重度骨髓抑制,余无明显不良反应。
本例患者为老年男性,因“反复右侧背部疼痛1年,加重半月”就诊,病理检查后明确诊断为ⅣB期的肺鳞癌,无手术指征。患者无化疗禁忌,入院后查免疫相关指标多个指标阳性,但是因患者无免疫相关疾病病史,经仔细分析,建议化疗及抗血管生成治疗,同时可加用免疫抑制剂,1周期后因患者出现反复发热1月后停用免疫治疗,第2周期单用化疗联合抗血管生成治疗,经2程治疗后部分缓解,病灶明显缩小,临床症状明显缓解,治疗期间未见明显治疗相关不良反应。继续原方案治疗2程,复查原发肿块继续缩小,治疗效果良好。4周期后患者出现重度骨髓抑制,不能耐受化疗,故再次加用免疫治疗。治疗后患者无药物不良反应,复查胸部CT仍持续缓解,患者现接受免疫单药维持治疗,仍在持续获益。
肺癌的发病率和死亡率在我国恶性肿瘤疾病中高居首位[1]。NSCLC是主要的病理类型,约占原发性肺癌的80-90%[2]。由于起病隐匿,我国多数NSCLC患者确诊时已为晚期,无法行手术切除治疗,而传统化疗的治疗效果并不理想,患者的5年生存率不到5%[3]。近年来,随着肺癌治疗步入精准医疗时代,以免疫治疗、靶向治疗为主的系统治疗方式发展迅速,尤其是化疗联合免疫检查点抑制剂,逐渐成为晚期NSCLC一线及后线的标准治疗方案,为患者带来了希望,同时也改写了NSCLC的整体治疗格局。
在中国NSCLC患者中开展的RATIONALE 307研究结果显示,相较于单纯化疗,替雷利珠单抗联合紫杉醇/白蛋白紫杉醇+铂类化疗方案可显著提高患者的无进展生存期(PFS,7.6个月/7.6个月 vs 5.5个月)、客观缓解率(ORR,73%/75% vs 50%),且不需考虑PD-L1表达水平及疾病分期;在安全性方面,治疗的总体安全性和耐受性均良好。2021年4月该研究数据发表在国际著名临床肿瘤期刊JAMA Oncology[4],获得了国际学术界的高度认可。基于RATIONALE 307研究在肺鳞癌一线治疗上的成功探索,替雷利珠单抗现已被《中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南(2021版)》推荐为晚期肺鳞癌的一线治疗。2021年1月12日,替雷利珠单抗联合化疗也已正式获得国家药品监督管理局(NMPA)批准用于晚期肺鳞癌的一线治疗。
替雷利珠单抗的抗肿瘤优势源于其独特的分子结构。通过对Fc段的改造,替雷利珠单抗最大限度消除了抗体依赖的细胞吞噬作用(ADCP)。在解除T细胞的免疫抑制的同时,最大程度保留效应性T细胞数量及功能,增强抗肿瘤活性[5]。此外,替雷利珠单抗具有更高的PD-1亲和力、更加缓慢的解离速率以及更长的半衰期,可以使替雷利珠单抗能够更彻底、更持久地阻断PD-1与PD-L1的结合[6],更好地满足了临床中对药物“高效低毒”的需求。
病例一为一例IIIc期肺鳞癌患者,无手术指征,无化疗禁忌和免疫相关疾病。参考RATIONALE 307研究结果,一线治疗给予替雷利珠单抗联合化疗方案。2周期治疗后,病灶即明显缩小,疗效达到PR。后续应用替雷利珠单抗单药维持治疗,仍持续PR,且治疗期间未见明显不良反应。患者获益显著,目前还在持续治疗和随访中。
病例二为一例ⅣB期肺鳞癌的患者,无手术指征,无化疗禁忌。虽然患者入院后查出多个免疫相关指标阳性,但无免疫相关疾病病史。经仔细分析,一线治疗采用了替雷利珠单抗+化疗+抗血管生成治疗,期间虽曾因反复发热及化疗后骨髓抑制短暂停用免疫治疗及化疗,但未对整体疗效造成影响,治疗期间病灶持续处于退缩状态,胸腔积液消失,临床症状明显缓解,疗效评估达到PR。后续应用替雷利珠单抗单药维持治疗仍持续PR疗效,目前患者还在持续治疗和获益中。
从这两例临床实践可以看出,无论前期化疗联合治疗方案,还是后续单药免疫维持治疗,替雷利珠单抗在晚期肺鳞癌治疗上都起着不可或缺的作用,其突出的疗效及可靠的安全性使得晚期肺鳞癌患者显著而持久的获益。随着替雷利珠单抗纳入最新版的国家医保药品目录,药品价格明显降低,药物可及性大大提高。 期待未来替雷利珠单抗能够在肺癌研究领域获得更多循证医学证据,惠及更多晚期肺癌患者!
参考文献:
[1] Latest global cancer data:Cancer burden rises to 19.3 million new cases and 10.0 million cancer deaths in 2020[J]. IARC.2020.
[2]Galluzzi L, Vacchelli E, Bravo-San Pedro JM, et al. Classification of current anticancer immunotherapies[J]. Oncotarget, 2014 5(24): 12472-12508.
[3] Noone AM, et al. SEER Cancer Statistics Review, 1975–2015, National Cancer Institute.
[4] Jie Wang , Shun Lu,et al. JAMA Oncol,2021,7(5):709-717.
[5] Zhang T,et al. Cancer Immunol Immunother,2018,67(7):1079-1090.
[6] Yuan Hong,et al. FEBS Open Bio,2021,11(3):782-792.查看更多