查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





本文作者 | 陈功(中山大学肿瘤防治中心) 本文欢迎转发,未经书面申请,请勿在其他平台转载。
2020年美国临床肿瘤学会(ASCO)是局部进展期直肠癌(LARC,locally advanced rectal cancer)研究丰收的一年,一共有3篇摘要入选口头报告和1篇研究入选壁报讨论。其中口头报告的这3个研究均关注了目前LARC术前治疗最重要的两个话题:如何提高疗效,如何注重器官功能保全,在治疗策略里均涉及到目前该领域最重要的理念-TNT(total neoadjuvant therapy,全程新辅助治疗),这些研究结果将给我们的临床实践带来怎样的影响呢?我们解读如下。

研究基本信息
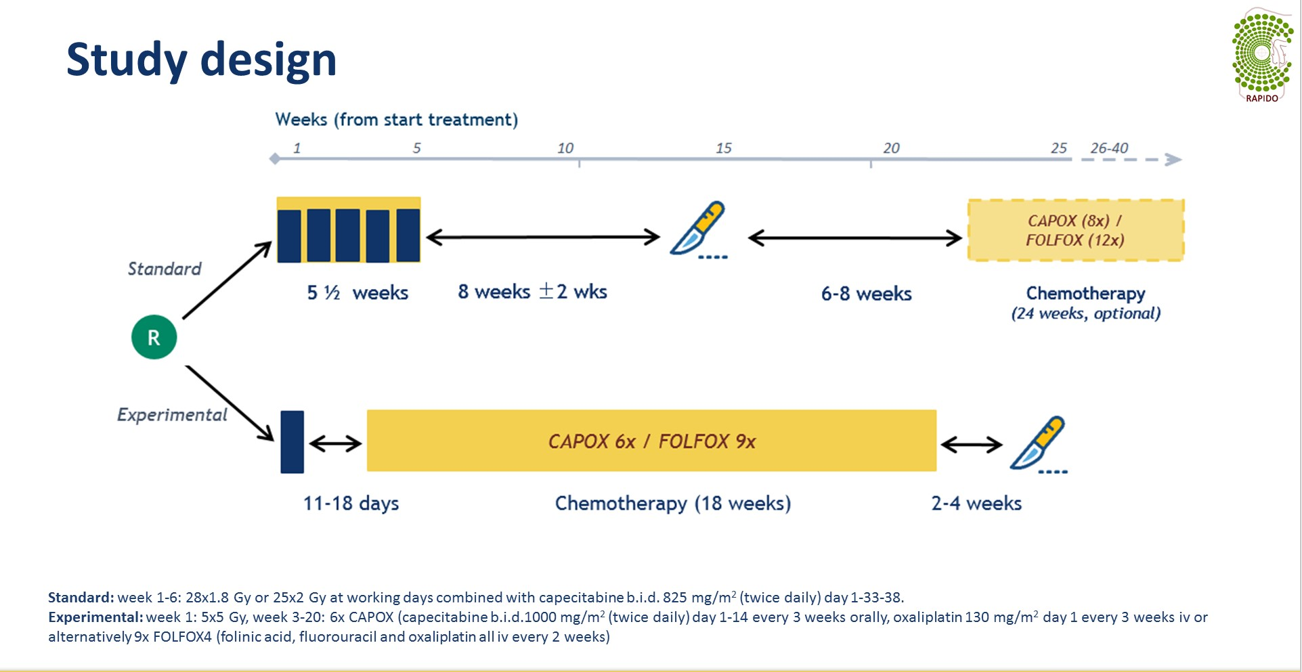

RAPIDO这是一项主要在欧洲荷兰、瑞典和西班牙等国家(也是目前5X5短程放疗开展最广泛的地区)开展的一项国际多中心Ⅲ期临床试验,旨在研究短程放疗(SCRT)后延迟手术,期间联合全身巩固化疗的TNT模式,对比“三明治式“标准治疗(氟化嘧啶增敏的CRT-TME手术-术后辅助化疗),能否在不影响局部控制的情况下降低全身复发的风险。
研究入组高分辨率MRI评价为高危转移复发的LARC。入组标准为至少满足一下一条:T4a/b、EMVI(壁外血管浸润)+、N2、MRF阳性(<1 mm)、侧方淋巴结+。
治疗分配
研究组TNT模式:先给予SCRT(5x5Gy),然后给予6周期CAPOX或9周期FOLFOX4,2-4周后TME手术,术后不再化疗;对照组传统的“三明治“标准CRT治疗:卡培他滨为基础的放化疗(25~28x 2.0 Gy~1.8Gy),6-10周后TME,术后辅助化疗(8周期的CAPOX或12个周期的FOLFOX4)。

研究的主要终点是“疾病相关治疗失败率“(Disease-related Treatment Failure,DrTF),具体定义为局部复发、远处转移、新发原发型结直肠癌、治疗相关死亡。次要终点包括总生存(OS)、R0切除率、pCR等。
统计学假设是3年的DrTF从30%降低到22.5%,样本量842例。
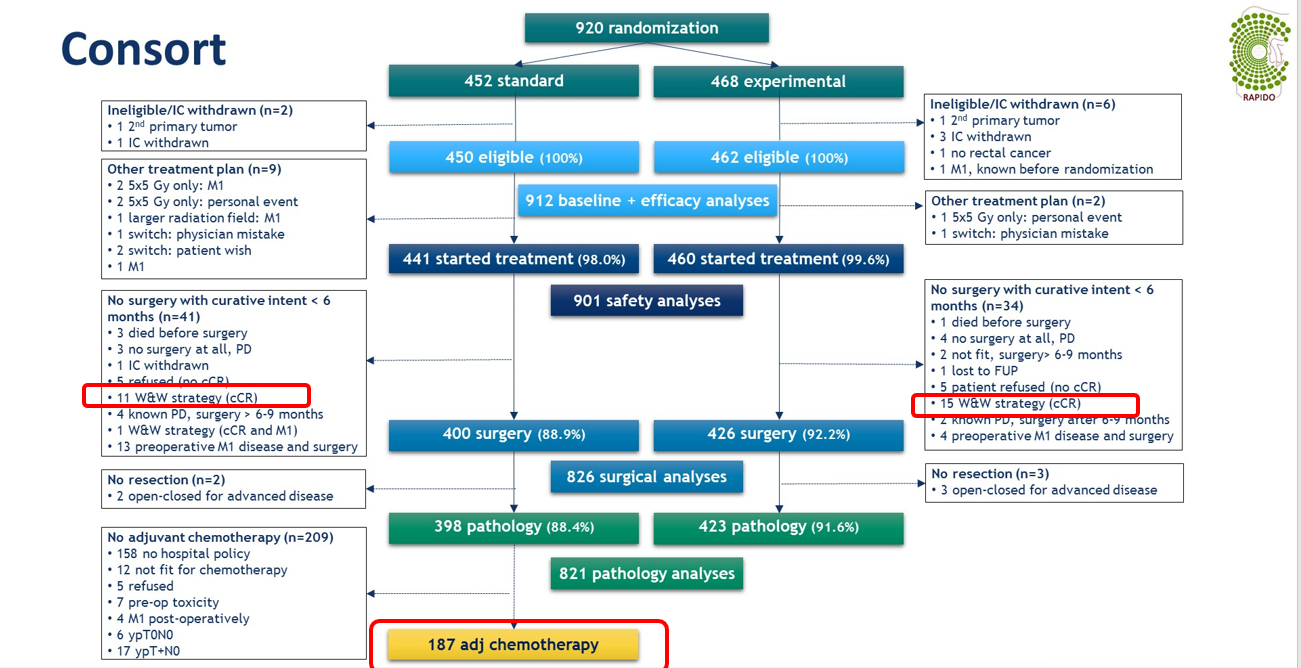
最终入组912例病例可行有效性分析,826例患者接受了手术治疗,因为肿瘤完全缓解(cCR)而未手术的分别是TNT组15例和CRT组11例;CRT组400例接受手术,但术后共有209例患者(52.3%)未接受术后辅助化疗,其中159(76.1%)例是因为所在医院没有LARC新辅助CRT+TME手术后的术后辅助化疗共识。
主要结果
手术相关结果
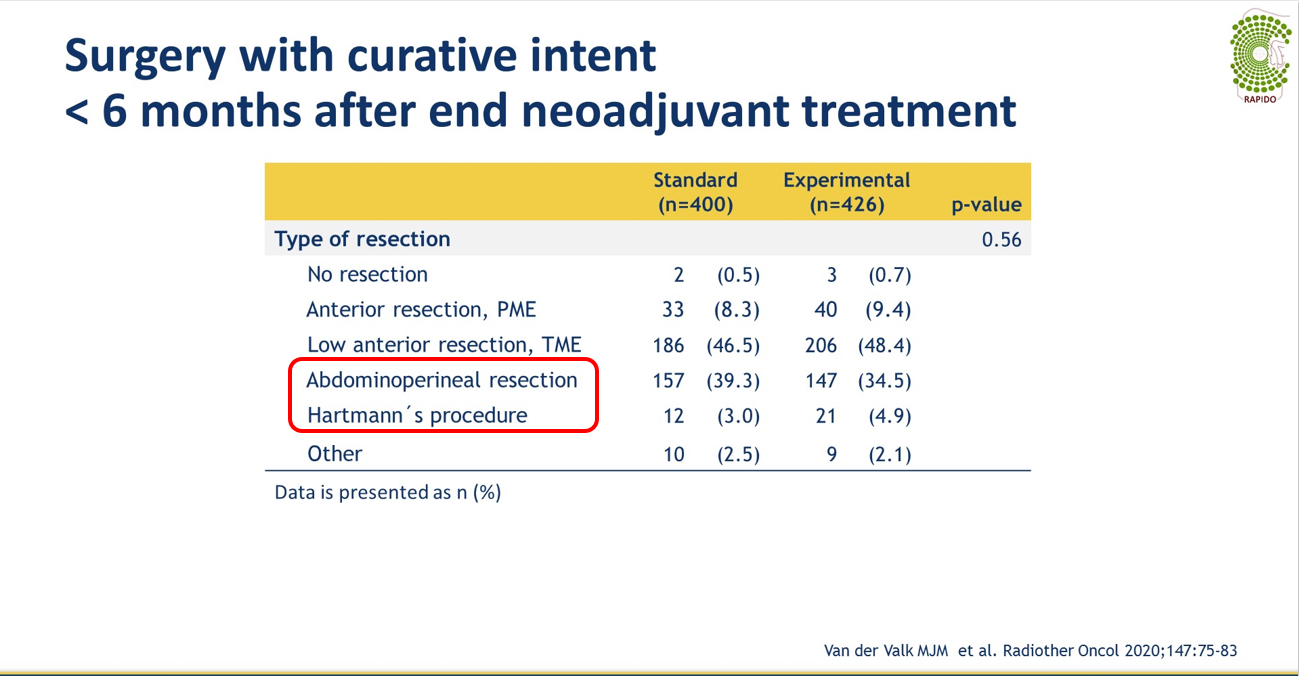
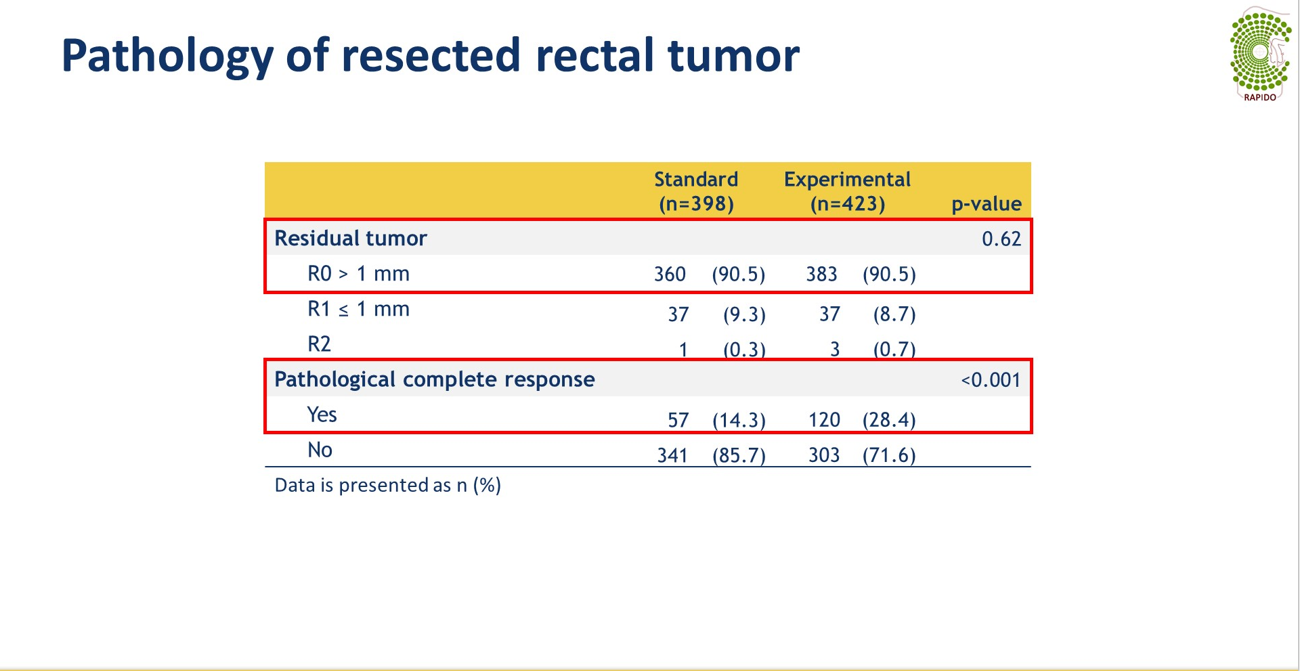
TNT组和CRT组两组间外科手术方式基本相似,在造口率(APR+HARTMANN手术)分别是39.4%和42.3%,R0切除率也相似,均为90.5%。TNT组病理完全缓解率(pCR)28.4%,显著高于CRT组的14.3%,P<0.001。
主要疗效终点
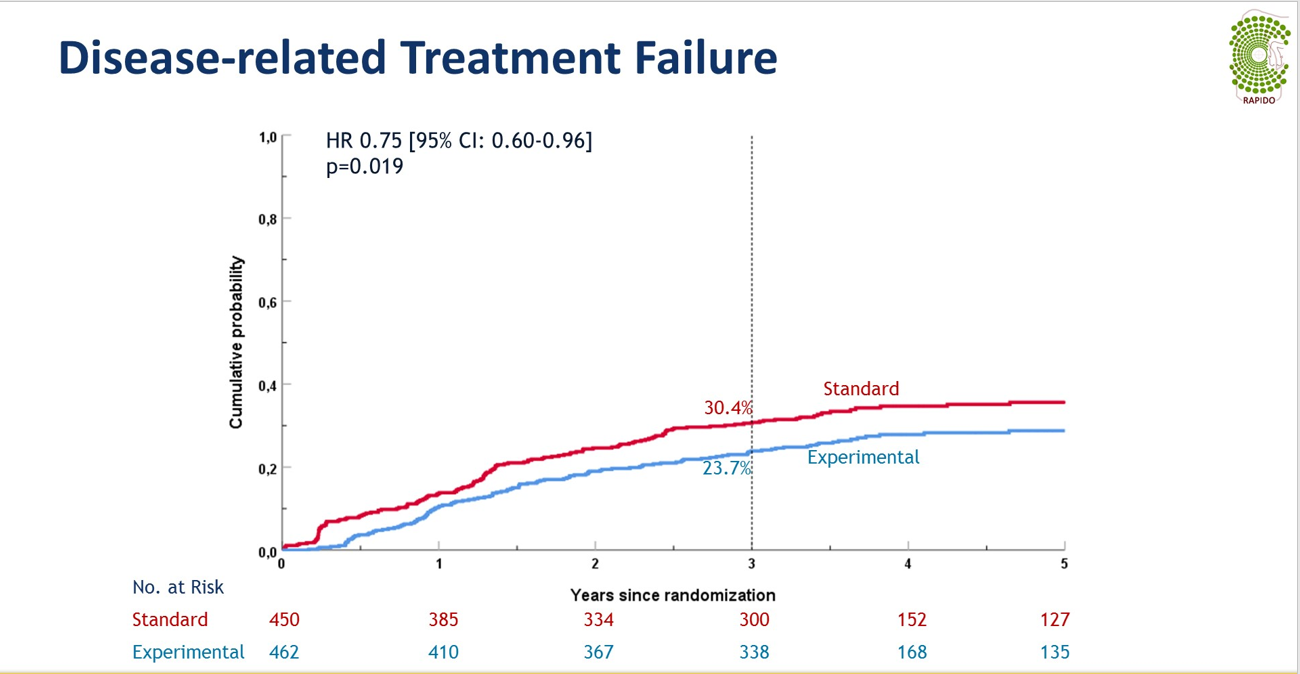
主要终点3年DrTF从30.4%降低为23.7%,差异又显著性,HR=0.75(95%CI 0.60-0.96),P=0.019。其中主要降低的是远处转移率,26.8%降低至20.0%,HR=0.69(95%CI 0.54-0.90),P=0.005.局部复发率TNT组稍高,但未见显著性差异(8.7%对6.0%,P=0.09)。
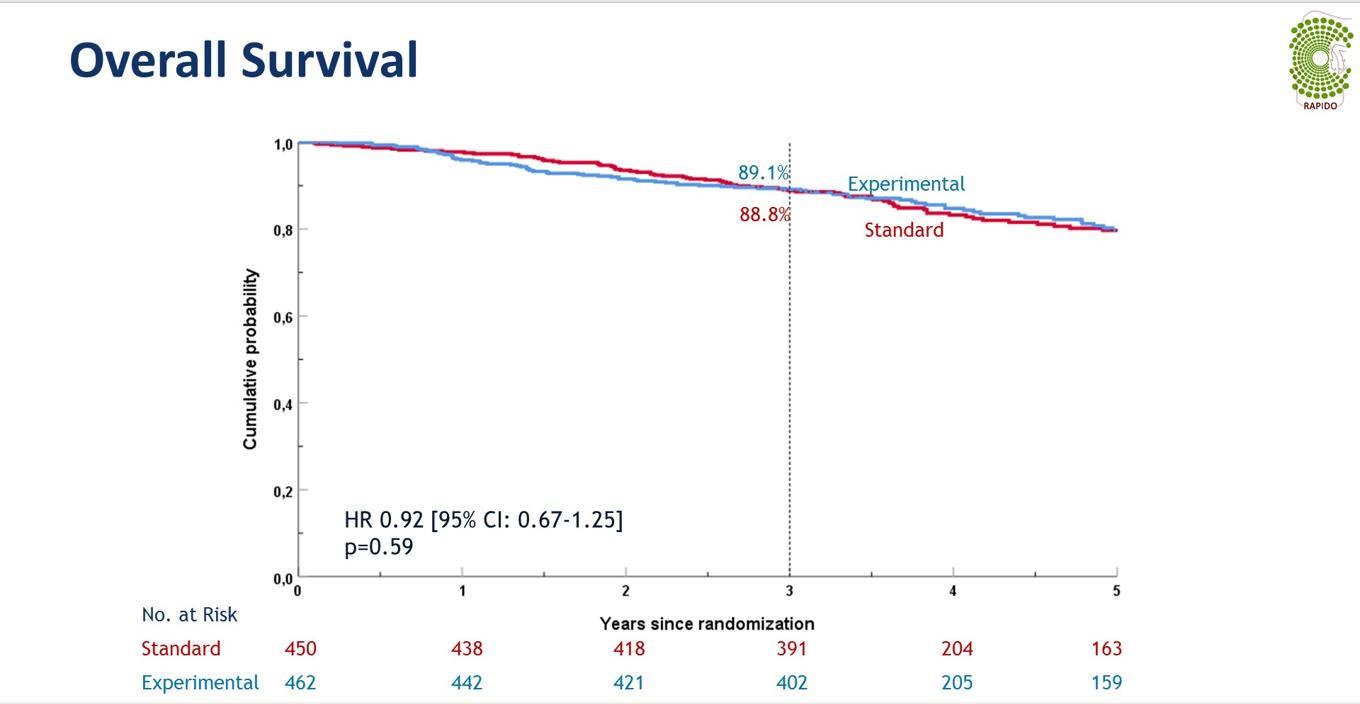
3年OS在两组间分别为89.1%和88.8%,差异无显著性,HR=0.92(95%CI 0.67-1.25),P=0.59.
研究结论

RAPIDO研究采用短程放疗后给予巩固化疗最后接受TME手术的TNT治疗模式,与传统的“三明治式“标准CRT模式比较,疾病相关治疗失败率和远处转移率均显著降低了7%,病理完全缓解率则从14%提高了一倍到28%,但3年OS未见差异,未见明显的不可预期毒性,外科并发症和生活质量也未见差异。研究提出将“短程放疗+巩固化疗+TME手术”的TNT模式作为LARC的新型标准治疗。

研究基本信息

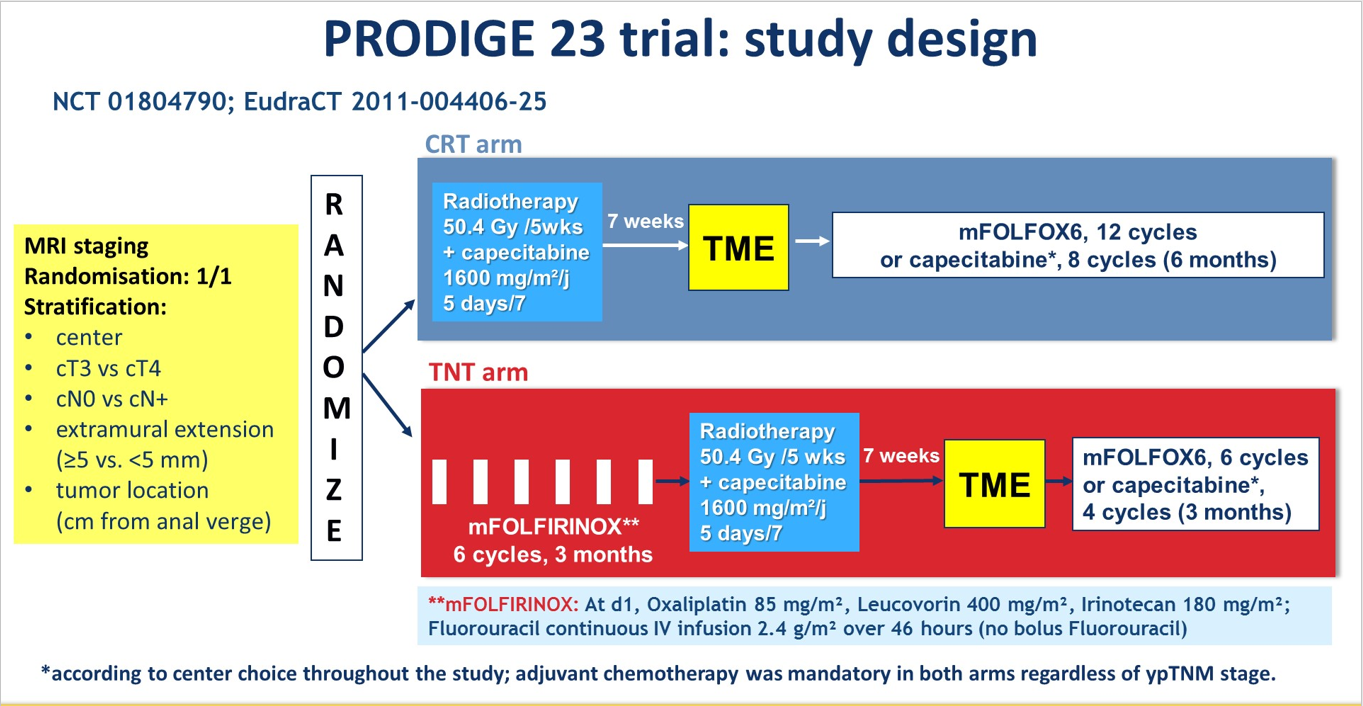
法国的PRODIGE 23研究纳入临床II/III期直肠癌(>cT3或N+),传统的“三明治”标准CRT对比类TNT模式治疗(在CRT前给予6个周期的mFOLFIRNOX诱导化疗)。

主要研究终点是DFS,研究假设是3年DFS提高10%(从75%提高到85%)。
基本特征
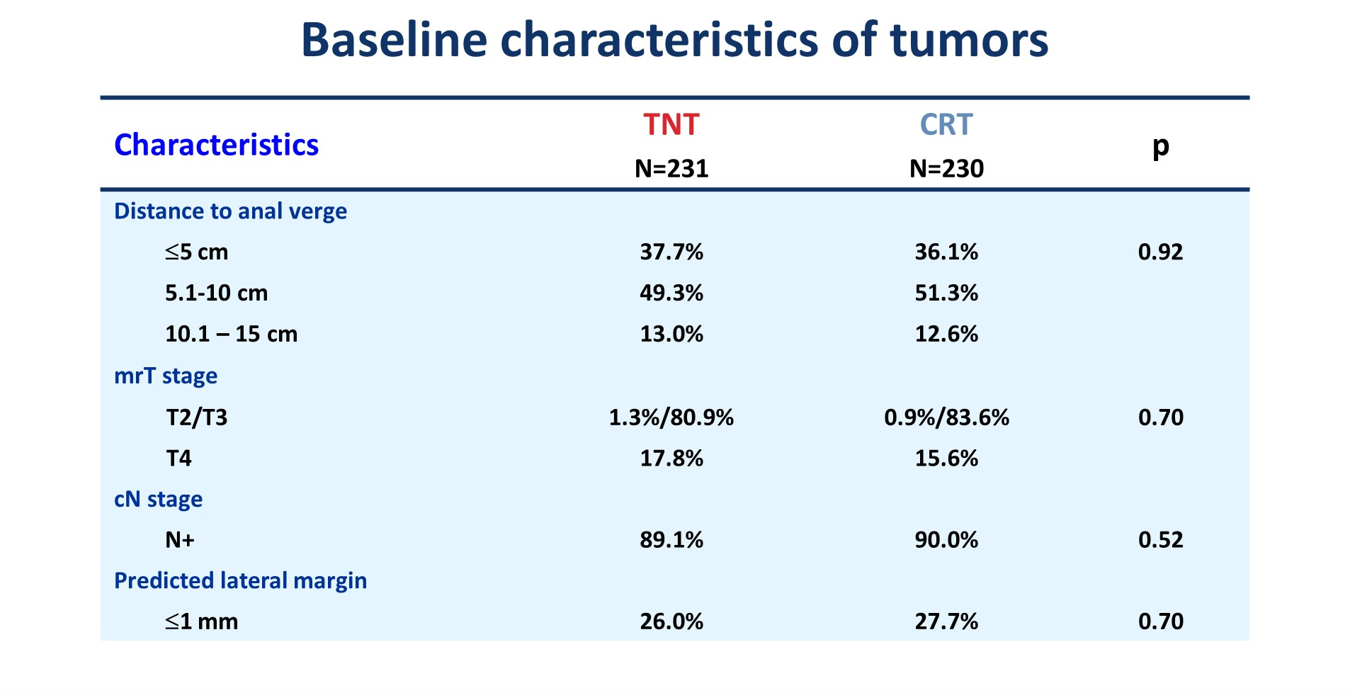
主要入组了肿瘤距离肛缘10cm以下的中低位直肠癌(>85%),III期比列接近90%,MRF阳性约26%。
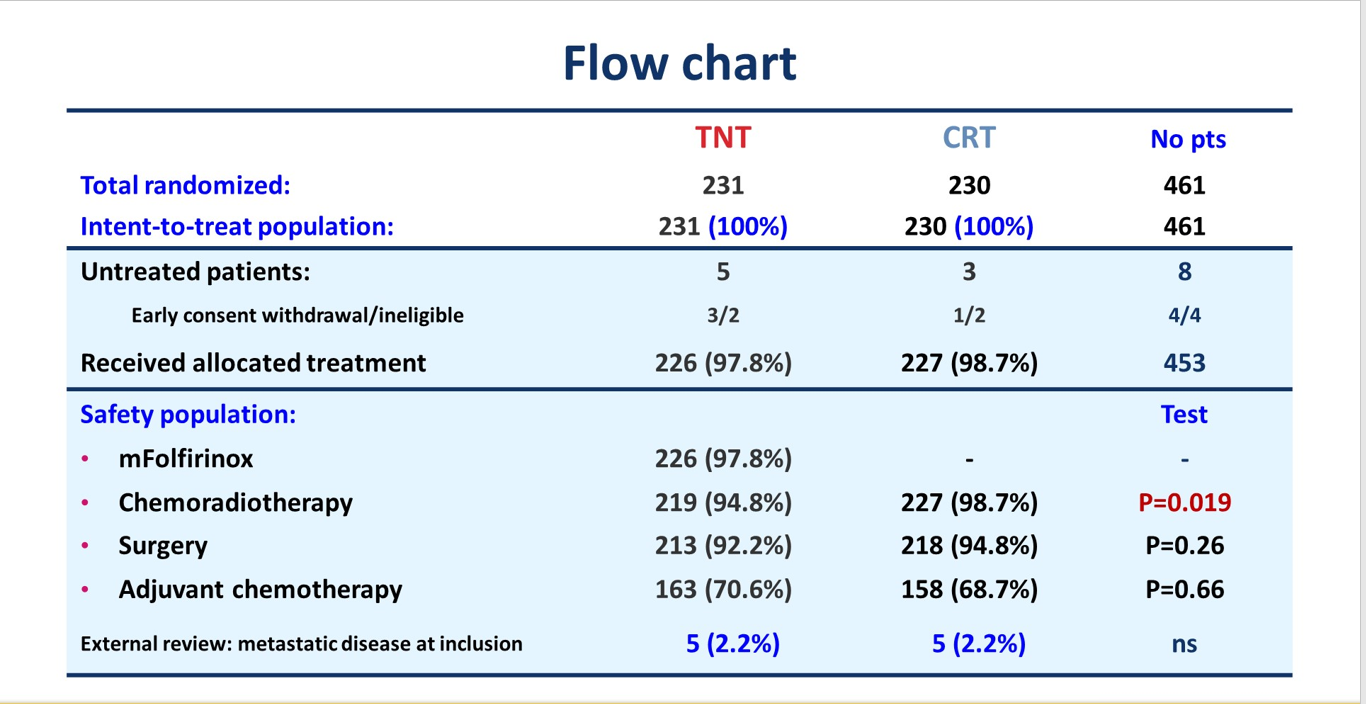
两组患者的治疗完成度都相当好,不管是三药诱导化疗,还是同步CRT,完成度均在95%以上。术后辅助化疗的完成度也在70%左右,这在同类研究中算很高了。
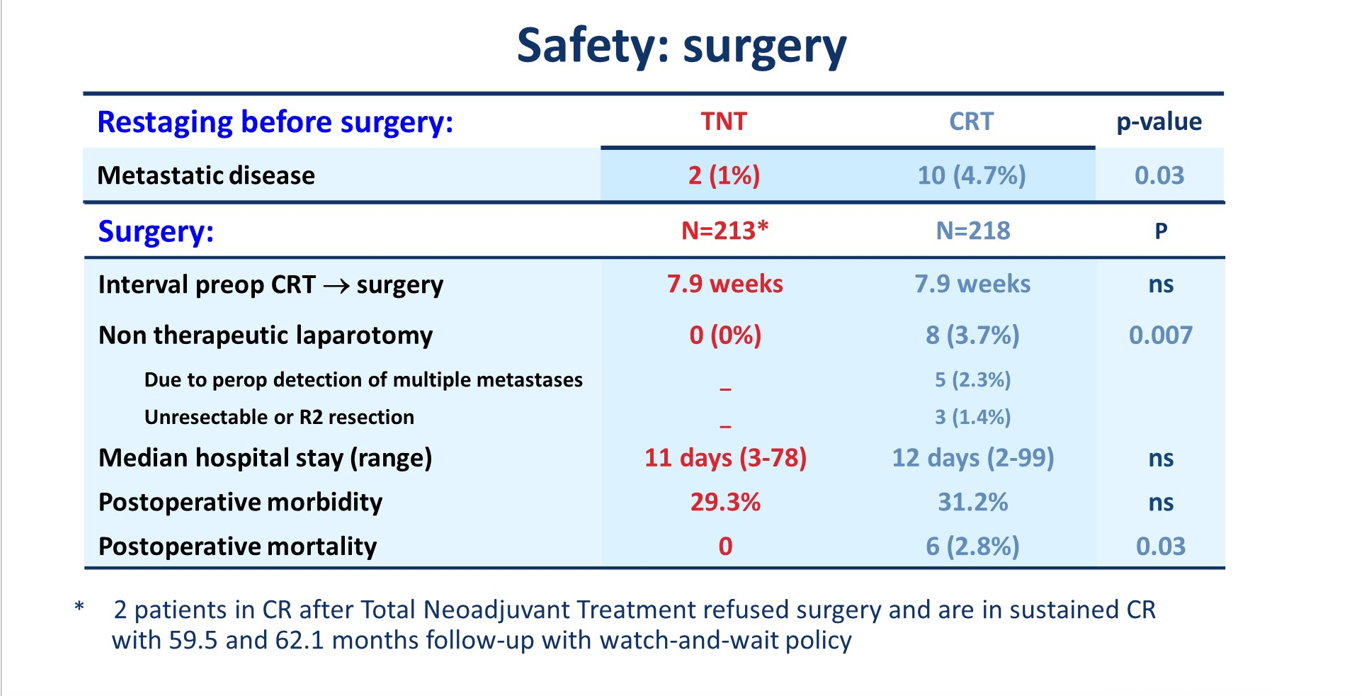
CRT结束到手术的平均时间是8周,术前再分期时出现远处转移的比例TNT组为1%,明显低于常规CRT组的4.7%,P=0.03。
病理学结果
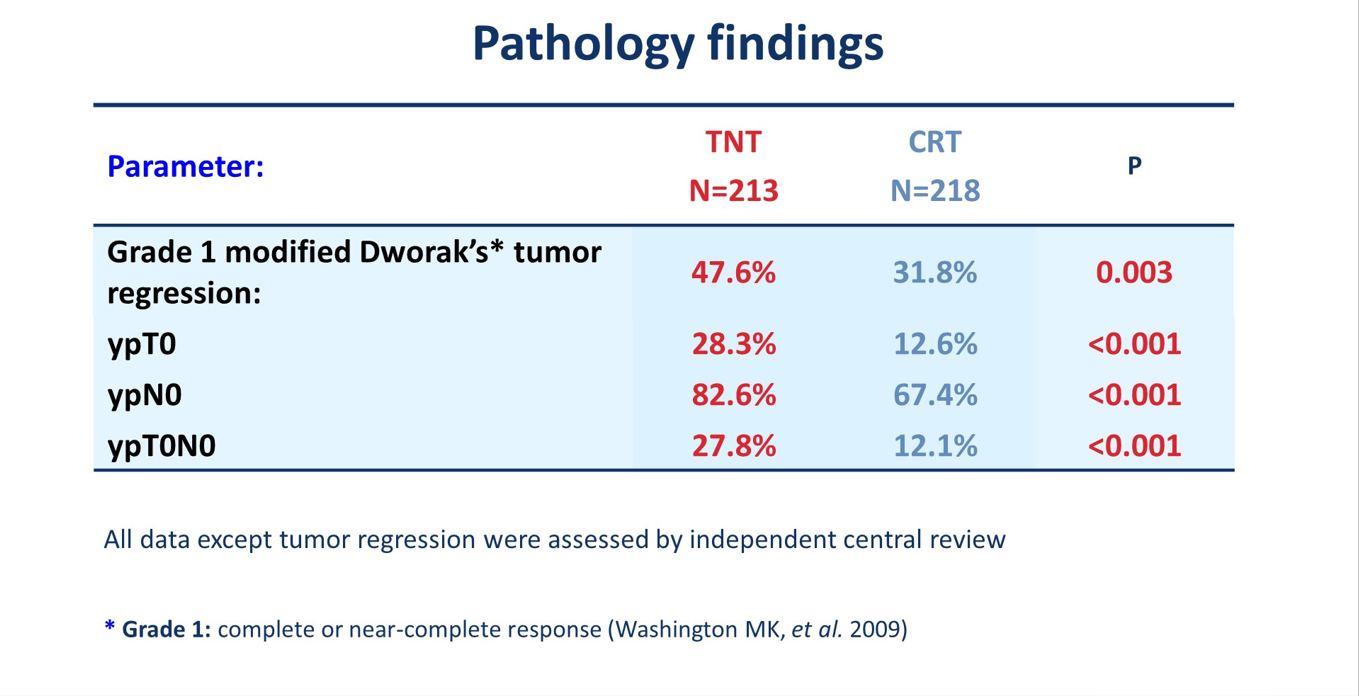
TNT组在TRG1(pCR或接近pCR)、ypT0、ypN0和pCR等病理学指标上均获得显著性提高,最终pCR率从12.1%提高到了27.8%。
主要疗效指标
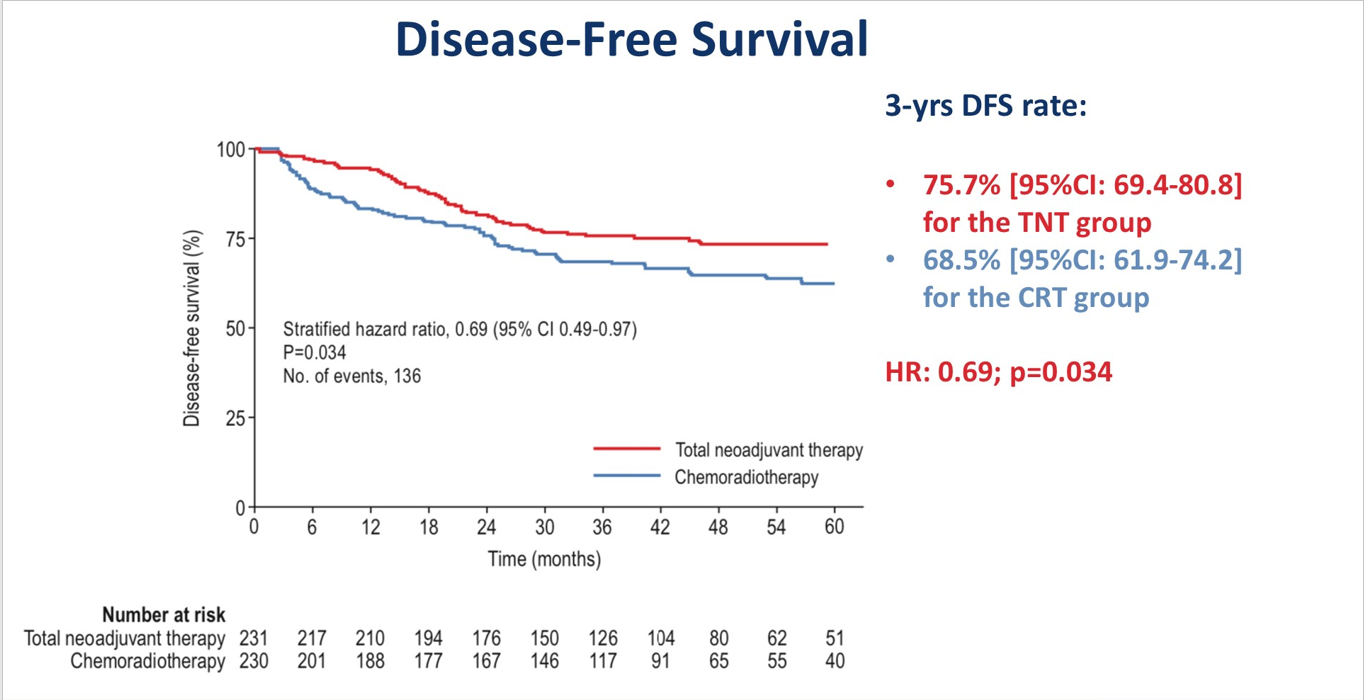
主要终点3年DFS 从68.5%提高到75.7%,HR=0.69 (95%CI 0.49~0.97),p=0.034,主要终点达成,是阳性研究。
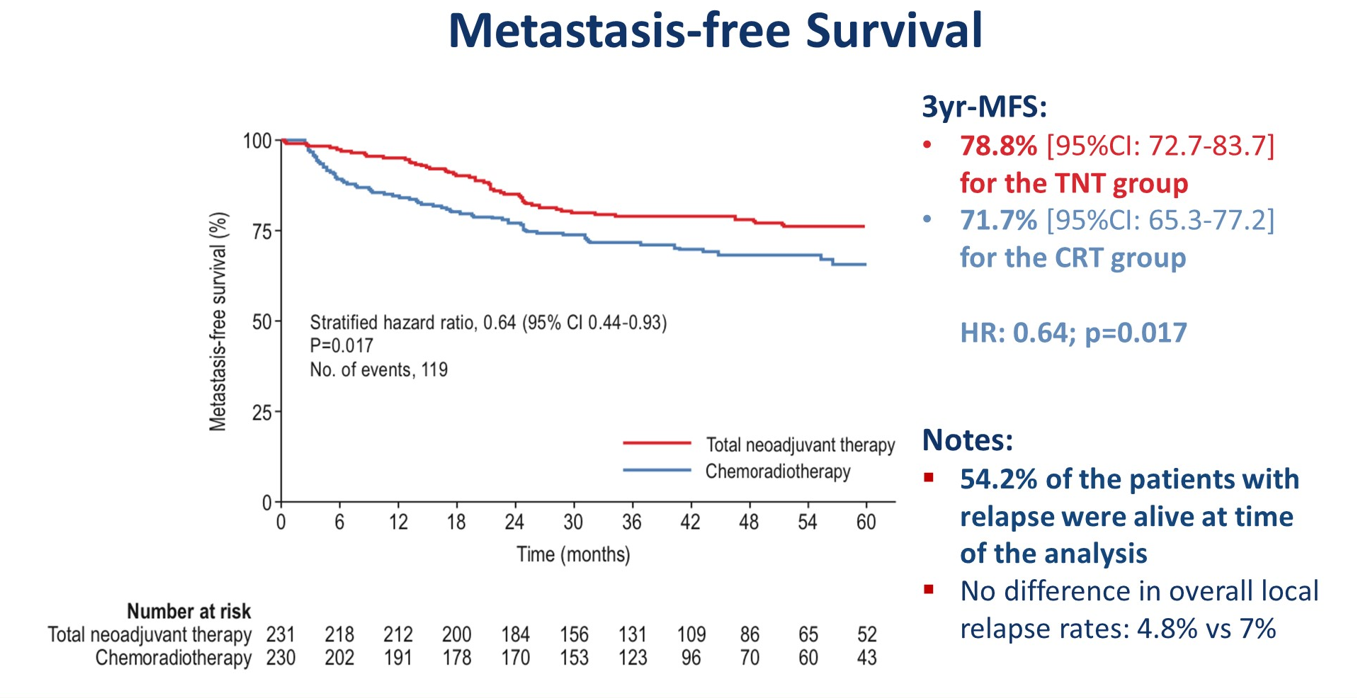
其中,无远处转移生存率改善尤为显著,从71.7%提高到78.8%,HR=0.64(95%CI 0.44-0.93),p=0.017;TNT组数值上也降低了局部复发率(4.8%对7%),但差异没有显著性。
研究结论

II/III期LARC患者在标准CRT前给予mFOLFORINOX强烈诱导化疗是安全可行的,能显著提高病理缓解率、提高根治意向的手术切除率、改善无病生存率和无转移生存率,同时生活质量没有受损。研究建议CRT前给予mFOLFIRINOX诱导化疗的TNT模式应该成为II/III期LARC患者的一直新治疗标准。

研究基本信息

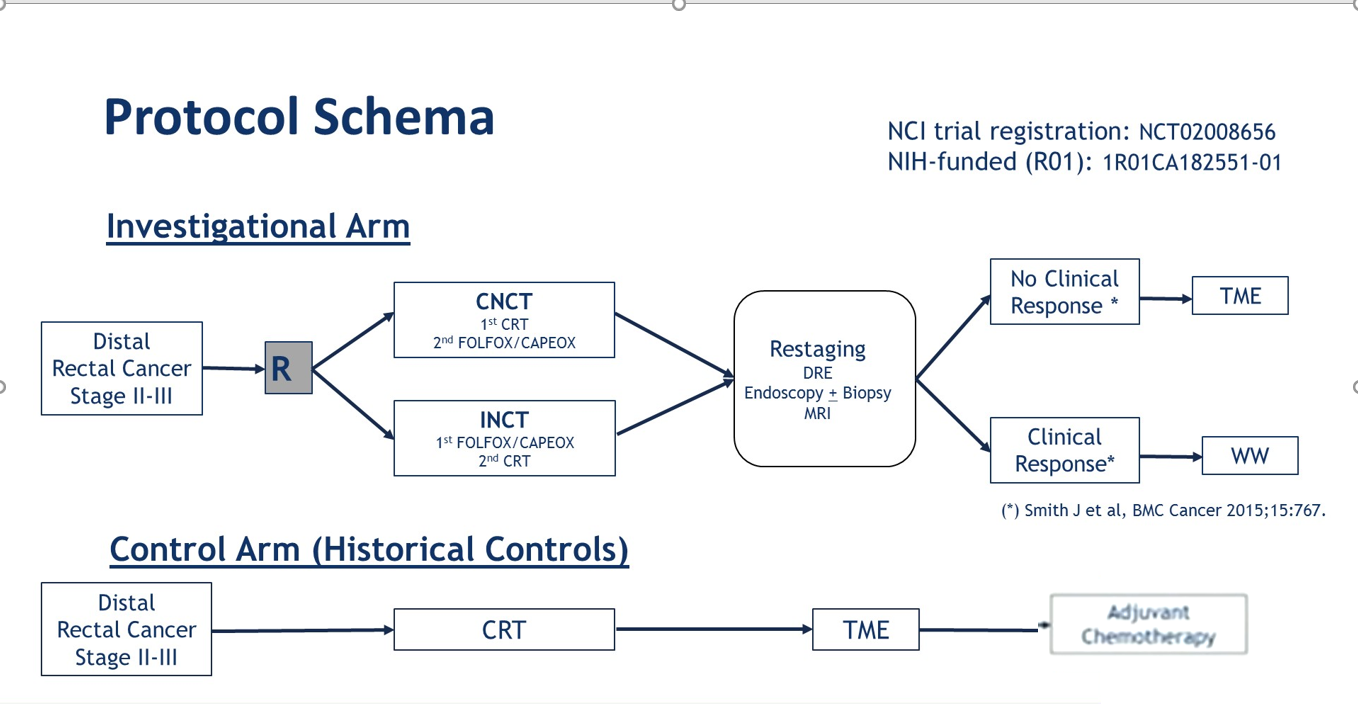

美国的OPRA研究专门针对II/III期低位直肠癌,即基线时外科判断须行APR(腹会阴联合切除术,俗称人工肛门手术)或须行结肠-肛管吻合术,给予两种模式的TNT治疗,分别是CNCT(CRT-巩固化疗)和INCT(诱导化疗-CRT),然后再分期,如果肿瘤完全缓解(cCR),则给予“观察等待”(W&W),如果肿瘤未完全缓解,再施行TME手术。对照组采用传统的“三明治”标准治疗作为历史对照。


研究主要终点是TNT模式的3年DFS,假设从历史对照组的75%提高到85%。次要终点是两种TNT模式的器官保全概率,历史对照INCT模式的3年NOM(“观察等待”的非手术治疗)率20%,CNCT模式则为35%;次要终点还包括TME手术组和NOM组的患者自我报告的功能结局、生活质量。
临床完全缓解(cCR)进入W&W策略患者的随访计划

进入W&W策略NOM的患者,需要行密切随访,包括,乙状结肠镜+直肠指检+CEA,每4个月1次共2年,然后每6个月1次共3年;直肠MRI每6个月1次共2年,然后每年1次共3年;胸腹盆增强CT每年1次共5年;全结肠镜检查在确诊后1年时复查1次,然后根据指南规定进行。
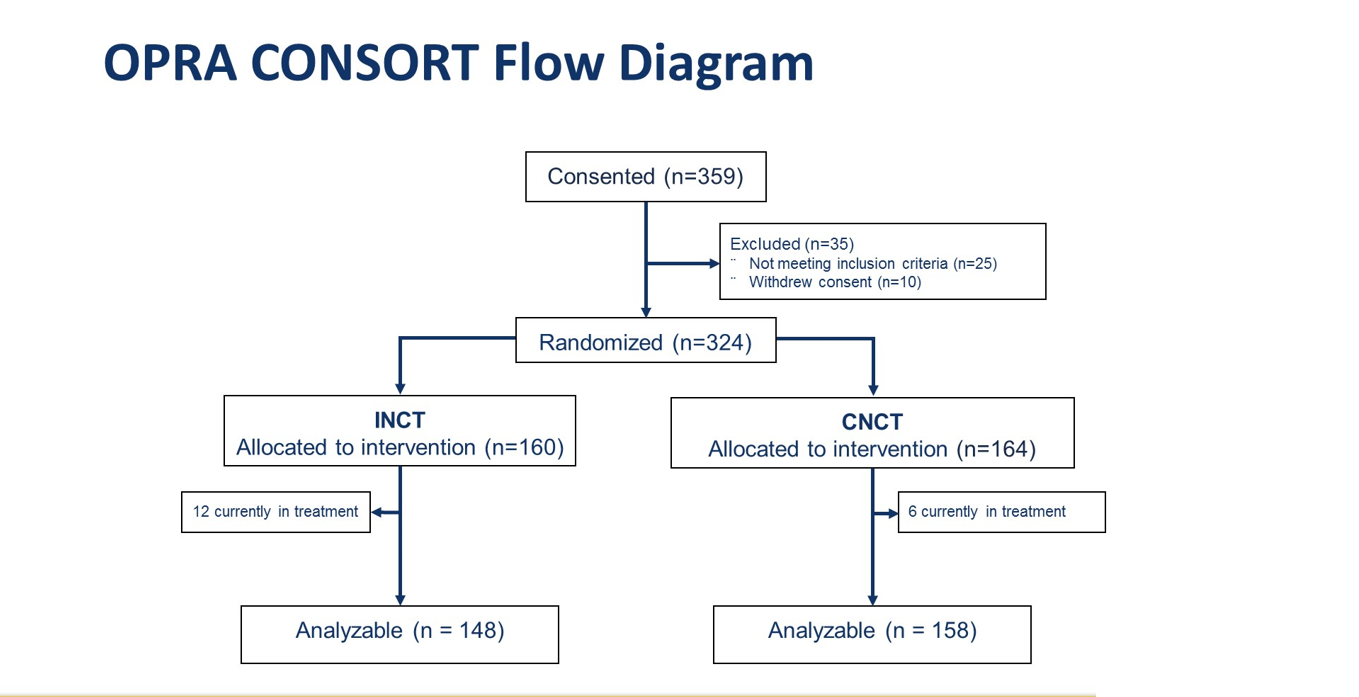
研究最终纳入324例患者,其中INCT组160人,CNCT组164人。
主要疗效结果
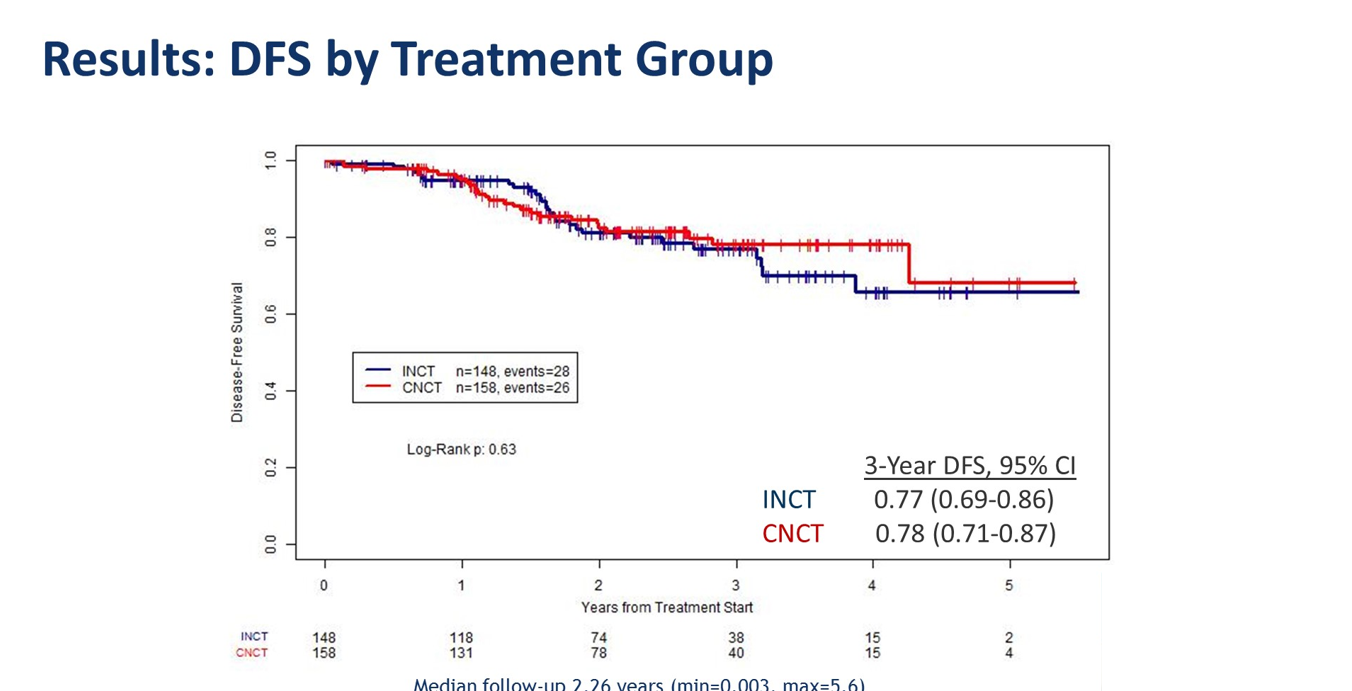
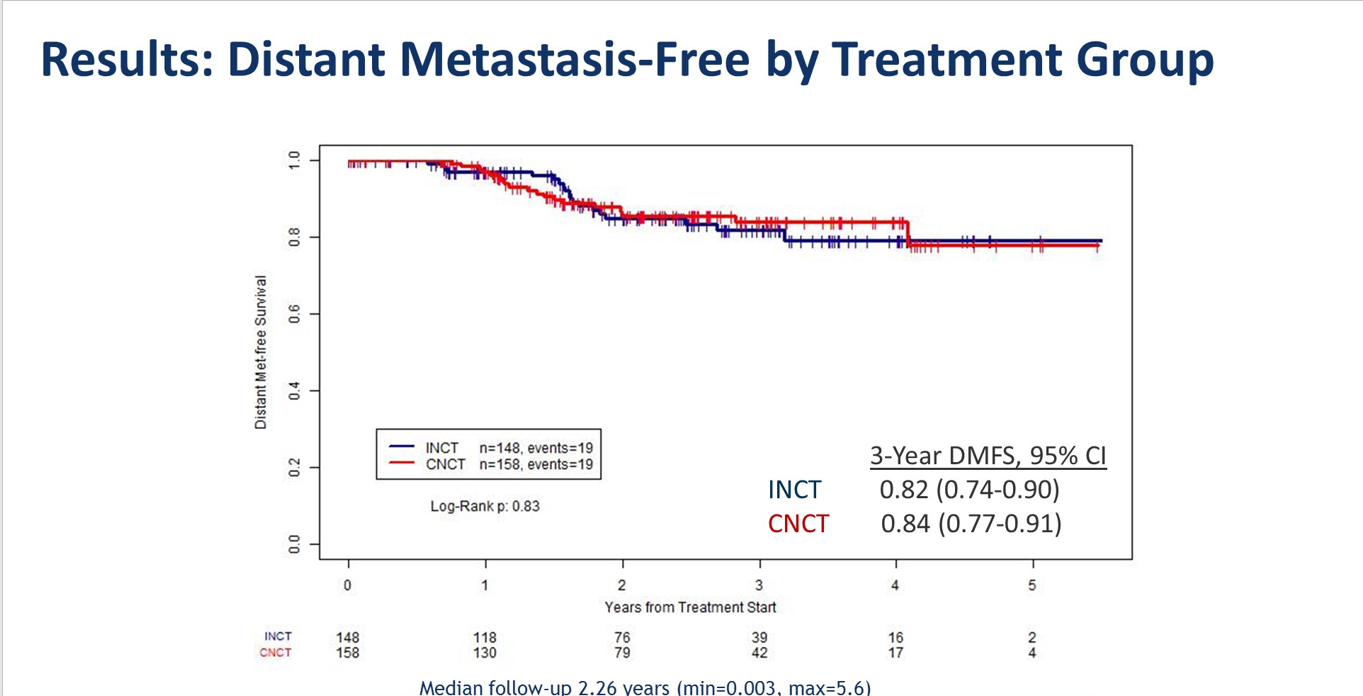
两组的3年DFS、无远处转移生存率均没有差异。
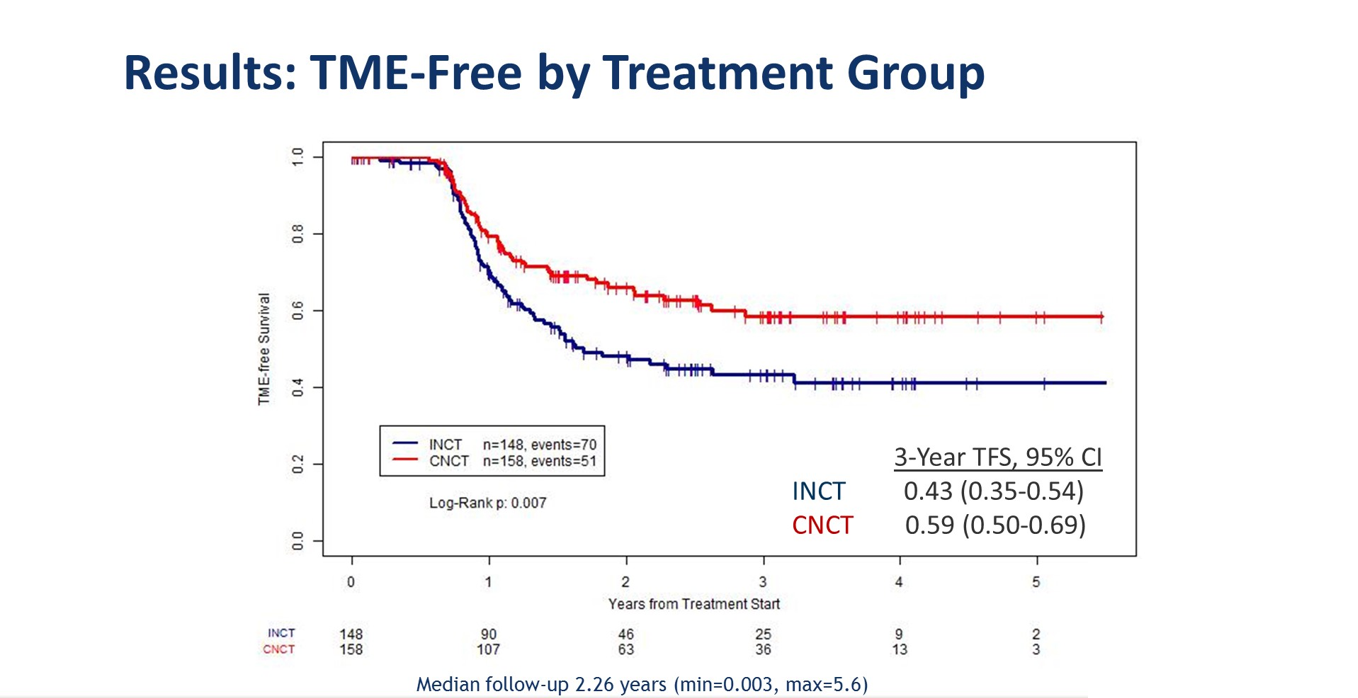
中位随访2.26年后,两组间3年NOM生存率则存在显著差异,CNCT组59%(148例中有70例),明显高于INCT组的43%(158例中有51例),p=0.007,意示着CNCT组能带来更多的cCR,从而让患者免于TME手术治疗。但两者TNT模式的NOM率均高于历史对照CRT模式的20%.
研究结论

OPRA研究预先制定了包含TNT后完全缓解者采取W&W策略的治疗计划,这使得近一半的LARC患者保全了直肠器官功能。和历史数据对比,TNT模式后不管采用TME还是W&W,无病生存率均无差异。OPRA并未发现CRT和全身化疗应用顺序对长期生存或远处转移带来影响,但基于该研究结果,CNCT(先行CRT再给予巩固性全身化疗)模式相较于INCT模式(全身化疗先行)更容易获得直肠保留的机会。

“三明治”治疗(CRT-TME-术后化疗)模式的利弊凸显
局部进展期直肠癌(LARC)的治疗,进入肿瘤学效果和功能并重的时代,传统“三明治”治疗(CRT-TME-术后化疗)模式的利弊凸显,该模式可以显著降低局部复发率,但却没能改善远期生存,其中一个重要原因就是在CRT和TME之后,术后辅助化疗完成度很低,可能影响了远期生存。
另外一方面,尽管CRT较单纯的术前RT提高了肿瘤缓解率,进而提高了保肛率,毕竟传统的CRT模式带来了肿瘤完全缓解率一般不超过20%,这对于绝大多数极低位直肠癌的肛门功能保全显然是不够的。
因此,目前全球业界的应对策略是强化术前治疗,一方面提高全身治疗的剂量强度,把术后完不成的全身化疗提前到术前来进行,以期减少远处转移,提高生存率。另一方面,强烈的术前治疗带来更多的肿瘤退缩,从而改变手术方式:将直肠癌的手术治疗模式“从大变小,从小变无”:显著的肿瘤退缩,使得原本需要行TME APR手术的患者可以施行括约肌保留的TME根治术式(LAR或ISR),乃至经肛门的局部切除,而完全消退者,也即达到”临床完全缓解“(cCR,complete clinical regression),可以考虑施行 “观察等待”策略(Watch & Wait, W&W策略)。
“三明治”模式在近10年的演变过程中,变化最大的就是逐渐延长的手术等待间歇期(从CRT结束到TME手术的间期),美国国家癌症综合网络(NCCN)指南的推荐从最初的4-6周延长到5-8周,再到现在的5-12周;而在逐渐延长的间歇期内,可给予更多的全身化疗,由于间隔时间延长和间歇期化疗的双重作用,肿瘤进一步退缩,pCR率逐渐增加,理论上获得更大的保肛机会。
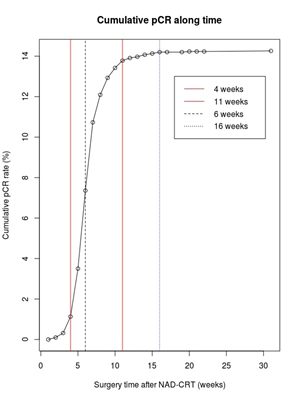
图:术前放化疗至手术间隔时间与pCR率的关系
在这个临床实践的演化过程中,TNT模式浮出水面,水到渠成,应该说,TNT治疗满足率上述的几乎所有元素,因此成为LARC术前治疗最优化的策略而大热。根据全身化疗与放化疗/放疗的顺序,TNT模式又可以分为两种:模式1,NeoCT-CRT/SCPRT-TME,或模式2,CRT/SCPRT-NeoCT-TME(见下图)。但不管哪一种模式,TNT策略期望达到的潜在优势都是一致的:提高全身化疗依从性和完成率,增加肿瘤缓解程度,提高保肛率或非手术治疗率,最终延长生存。
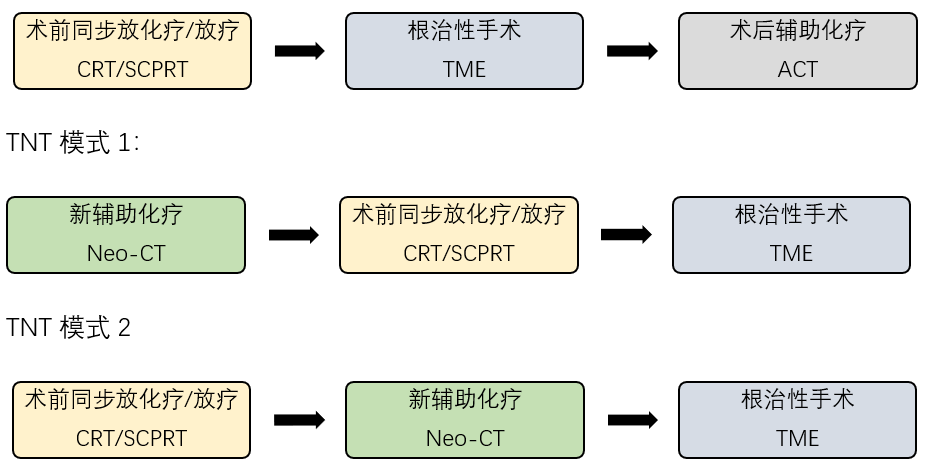
图:局部进展期新辅助治疗的模式图
本次ASCO大会的三个LARC领域TNT研究,都达到了什么目的呢?
术前放疗的两大模式,5X5短程放疗(SCRT)和长程同步放化疗(CRT),从治疗时间安排上来说,SCRT是最适合做模式二TNT策略的,既往的POLISH II研究已经证明了这一点。而CRT模式如果要做TNT策略,手术前的治疗时间就会明显延长。
RAPIDO研究是SCRT模式下最大规模的完全TNT模式2研究,是近几年该领域业界最期待的研究,它的结果也基本解释、解决了“三明治“模式的弊端:极大程度提高了全身化疗完成度,最终转化为远期生存的提高。
法国PRODIGE23研究则是践行了TNT模式1,但不是完全TNT,可以称为类TNT(TNT like),因为并没有把所有全身化疗置于术前进行,尚有一半的化疗还是在术后以辅助化疗的方式给予,主要原因在于该研究的诱导化疗使用了目前结直肠癌领域最强烈的三药方案,该方案一般仅用于肿瘤负荷较重的晚期疾病。最终,该研究也成功的改善了DFS。
因此,从结果来看,RAPIDO和PRODIGE23两个TNT模式都取得了阳性的结果,改善了LARC的无病生存率,但这种改善可能是建立在对照组全身治疗完成度太低、开始太晚有关。RAPIDO研究中对照组的术后辅助化疗完成度仅48%,而且,对照组开始接受全身化疗的时间与TNT组比较,迟了差不多20周(5个月);PRODIGE23研究里TNT组术前化疗采用的是三药FOLFIRINOX方案,而对照组的全身化疗则仅有mFOLFOX,那么,生存的改善是来源于TNT模式呢还是来源于术前化疗中增加的另外一个药物伊立替康,这是无法分清楚的。
另外,从器官功能改善角度来看,RAPIDO和PRODIGE23两个研究却没有显示出优势,尽管两个研究的肿瘤缓解指标均大幅改善、pCR率都翻了一翻,这是为什么呢?这两个研究没有预先设定器官功能保全的计划,也就是W&W策略问题,几乎所有的患者还是接受了TME手术,因此,TNT带来的肿瘤缓解率提高没有最终转化为器官保全。
反之,美国OPRA研究则显示不管哪一种模式的TNT,和传统CRT模式对比均不能改善生存,研究者认为术前CRT和诱导化疗的试验顺序不会影响生存,主要终点3年DFS并未达到。当然,该研究的对照组是采用CRT模式的历史数据,而不是统一研究中的一个真实对照组,该结论是否可靠,值得商榷。
欣喜的是,由于OPRA研究预先设定了器官保全计划,而且入组的基本都是基线时保肛无望或很困难的低位直肠癌,因此可以说OPRA是第一个以器官功能保全为目标的TNT研究,尽管该目标不是主要终点,而且,和传统CRT模式的历史数据比较,两种TNT模式均显著提高了NOM率,CRT模式20%, INCT模式 43%,CNCT模式59%。
可以说,OPRA研究是“有心栽花花不开,无心插柳柳成荫”,主要终点未达成,却收获了阳性的次要终点。但这并不是偶然。历史上第一次最大宗TNT模式回顾性病例报告正是来自OPRA主要研究者所在的MSKCC(纽约纪念斯隆凯瑟琳癌症中心),该中心在2017年ASCO会议上报道了628例回顾性大宗病例对比分析(ASCO 2017 #3519,JAMA ONCOLOGY 2019),308例INCT 模式TNT组患者先行8程FOLFOX方案或5程CAPOX方案化疗,再行放化疗,320例接受常规的CRT治疗模式。TNT组全身化疗依从性显著提高,出现了更多肿瘤退缩,这使得21.8%的患者因此而没有接受手术治疗(W&W),但对照组常规CRT模式里,该比例仅为5.9%。尽管MSKCC早期的这个回顾性研究采用TNT模式治疗的初衷是改善远处生存,但结果显示最终并未带来生存获益,但意外的发现就是该模式能让更多患者由于肿瘤完全缓解而接受WW策略,从而保全器官功能。因此,基于这个回顾性分析,今天的OPRA研究结果就不难理解了,用一个前瞻性RCT来验证了既往的发现。
OPRA研究的结果还比较了INCT和CNCT两种TNT模式,发现CNCT模式能带来更多肿瘤退缩,更加有利于极低位置的LARC,这个结果和早前报道的类TNT研究AIO-12结果一致。
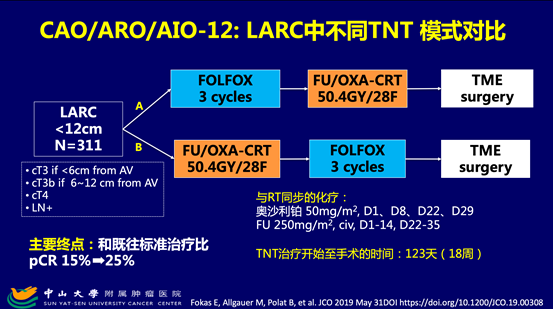
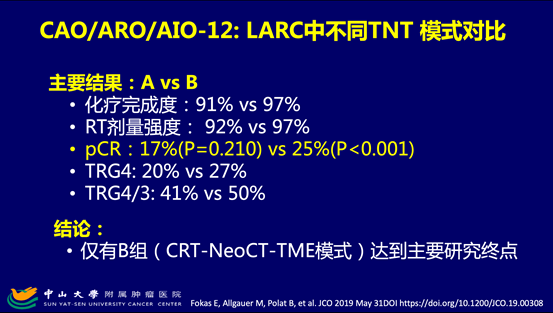
TNT治疗带来显著肿瘤退缩后,临床常用的器官功能保全策略包括三个:器官毁损性TME手术变为括约肌保留性TME手术,这主要适用于肿瘤基线位于距肛3-5cm左右的肿瘤,未达cCR,不可经肛局部切除;TME手术变为经肛门局部切除术,这主要适用于肿瘤获得明显缓解但未达cCR;需要手术变为非手术治疗(即W&W策略),适用于cCR者。
OPRA研究的另外一个启示还在于常规CRT模式也是可以践行TNT策略的,因此,对于RAPIDO和PRODIGE 23研究来说就是一直有益的补充。如果把这两种模式结合起来,不但能增加器官功能保全的机会,也能改善远期生存。
可见,以强化术前全身化疗、延长手术等候间隔为标志的TNT模式,是目前LARC术前治疗策略中能带来最大程度肿瘤退缩的治疗模式,为器官功能保全提供了肿瘤学基础。
下图是我在临床实践中对于传统CRT、TNT模式的具体临床选择标准。那些如果按照计划进行手术就会面临肛门括约肌功能丧失或极大损伤的低位直肠癌,且在前期的CRT治疗后肿瘤退缩明显,有cCR的趋势者,我会积极践行CRT先行的TNT模式治疗,以期达到cCR,然后W&W来最大程度保全功能。对于保肛没有难度、但远处转移风险较高的LARC,如距肛>5cm中上段肿瘤但伴有EMVI+、N2、侧方淋巴结+等不良预后因素,我会积极践行诱导化疗先行的TNT模式治疗,改善长期生存;而其他情形下则不会刻意去做TNT,除非是临床研究。
回头看这样的临床实践选择,也很好地得到了今年ASCO年会的RAPIDO、PRODIGE23和OPRA研究结果的支持。
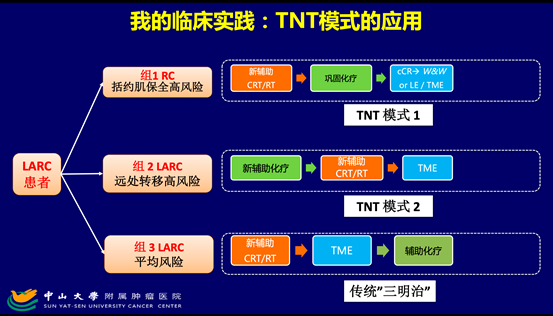
总之,局部进展期直肠癌治疗过程中面临的问题很多,改善生存和器官功能保全是主要的两方面,从治疗前的诊断评估开始就应该给予高度关注,TNT策略可能是目前的最优化模式。
查看更多