查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





间变性淋巴瘤激酶(ALK)融合基因是非小细胞肺癌(NSCLC)常见的驱动基因之一[1]。流行病学数据显示,在中国晚期NSCLC患者中,ALK融合基因的阳性率为9.06%[2]。ALK酪氨酸激酶抑制剂(TKIs)能结合到ALK融合蛋白的激酶结构域,抑制其磷酸化,阻断下游信号通路,产生抗肿瘤活性[3],已经成为ALK融合基因阳性晚期NSCLC患者的标准治疗选择。然而,随着各种ALK抑制剂不断涌现,如何在众多的治疗选择中优化治疗策略,成为临床热点问题之一。
为进一步探索ALK阳性NSCLC患者的治疗选择,中国医学论坛报社开展“实例呈现——最佳临床病例分享项目”。第八期特邀山东第一医科大学附属肿瘤医院(山东省肿瘤医院)杨广建医师分享《一例ALK G1202R阳性NSCLC患者二线接受伊鲁阿克治疗后PFS超13个月》,并邀请山东第一医科大学附属肿瘤医院(山东省肿瘤医院)唐晓勇教授进行点评。现将病例及点评内容整理如下,供大家分享、交流。
该患者为cT3N3M1c IVB期肺腺癌,合并左肺门、纵隔、腹膜后淋巴结转移,胸膜转移,骨转移,EML4-ALK基因融合阳性;
一线阿来替尼治疗20个月后,出现疾病进展,再次组织活检并行NGS检测,发现TTC7A-ALK、EML4-ALK双融合;
二线接受伊鲁阿克治疗13个月,总体疗效评价为疾病稳定(SD)。治疗期间耐受性良好。
一般资料:患者男性,39岁,ECOG:1分。
诊断过程:
胸部CT(2022.3.24):左肺门、纵隔淋巴结肿大,左侧胸腔积液。
超声气管镜(2022.3.29):气管镜淋巴结穿刺涂片及胸水细胞学提示“腺癌”。
病理会诊(2022.4.6):(胸水细胞块)免疫组化结果,TTF-1+,NapsinA+,CEA+,CR-,WT-1-,P40-,Ki-67+约30%,符合肺腺癌。
基因NGS检测(2022.4.18):(组织+胸水)EML4-ALK基因融合(EML4 exon6-ALK exon20), NFE2L2 2号外显子错义突变,p.E79K。
诊断:左肺腺癌cT3N3M1c,IVB期。左肺门、纵隔、腹膜后淋巴结转移,胸膜转移,骨转移。
第一阶段:阿来替尼治疗
治疗方案:2022年4月28日起,给予阿来替尼600mg每天2次靶向治疗。
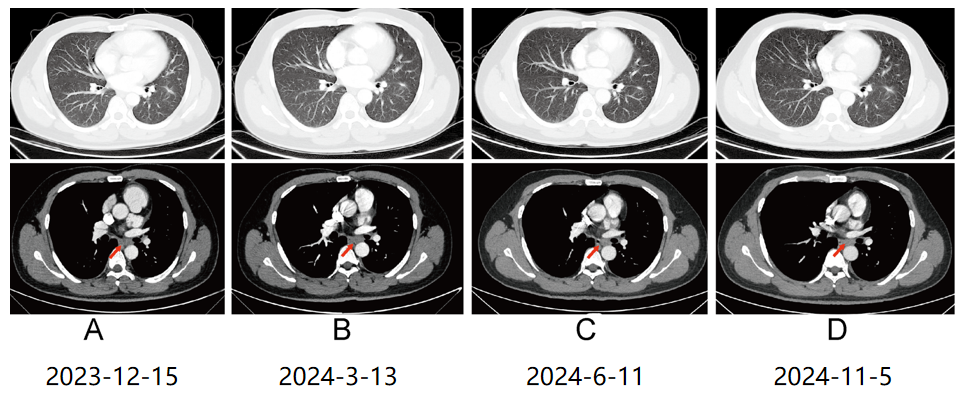
辅助检查及疗效评价:治疗期间,持续进行效果评估,治疗最佳总体疗效为部分缓解(PR)。左肺原发灶缩小,纵隔、左肺门转移淋巴结缩小,获益明显(图1),但治疗20个月后,胸腹增强CT复查发现纵隔8L区淋巴结转移较前增大,其余转移部位无显著变化。行超声支气管镜检查(2023.12.18),病理结果提示,纵隔8L区增大淋巴结活检查到癌细胞,考虑腺癌(图2),并进行肺组织活检(2023.12.27),样本经Dako22C3 IHC检测,结果为PD-L1阴性肿瘤细胞TPS<1%(图3)。纵隔淋巴结活检组织NGS基因检测(2024.1.8)结果提示,ALK基因重排,ALK-TTC7A(A19:T16)、EML4-ALK(E6:A20),ALK 23号外显子错义突变,p.G1202R(图4、图5)。
图1 阿来替尼靶向治疗期间左肺原发灶及纵隔、左肺门转移淋巴结变化情况
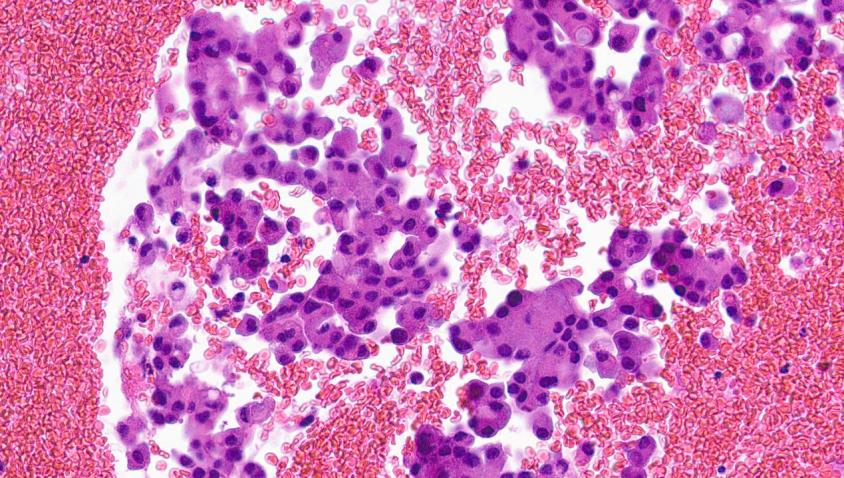
图3 阿来替尼治疗进展后再次PD-L1检测(22C3)(200×)
图4 阿来替尼治疗进展后再次NGS检测结果
图5 利用IGV软件分析NGS测序数据(TTC7A-ALK、EML4-ALK双融合)
安全性:治疗相关副反应类似阿来替尼,主要为1级高甘油三酯血症及1级高胆固醇血症,未出现其他药物治疗相关不良反应。
唐晓勇教授点评
锚定耐药关键,国产ALK-TKI“迭代升级”,破解临床耐药困局
研究发现,在NSCLC患者中,约2/3存在基因突变[4],其中,ALK融合基因属于NSCLC的少见驱动基因。目前靶向治疗均为首选治疗方式,但靶向治疗最终也会出现耐药,进而导致疾病复发或进展,即产生ALK-TKI的获得性耐药。从机制上看,获得性耐药大致可分为ALK依赖性和ALK非依赖性耐药两类。其中,ALK依赖性耐药是指ALK基因本身发生继发突变或扩增,导致ALK靶向药物的结合能力或活性降低,如G1202R、L1196M、G1269A等突变;而非ALK依赖性耐药则指肿瘤细胞通过激活其他信号通路或转化为其他表型,包括MET扩增、EGFR突变、BRAF突变等[5-6]。
目前,在临床应用的ALK-TKI 药物中,我国自主研发、高选择性的新型ALK/ROS1抑制剂伊鲁阿克对ALK融合蛋白及G1202R和L1196M等常见ALK-TKI耐药突变具有较强的抑制活性,提示伊鲁阿克除了可以作为一线治疗选择外,还可作为其他ALK-TKI耐药后的治疗选择之一[1]。伊鲁阿克之所以能够帮助一线ALK-TKI耐药的患者再次获益,主要得益于其关键结构的优化:以双苯胺嘧啶为主要骨架,通过对4个关键基团的改造优化,增强了与ALK激酶结构域的结合能力,包括对耐药突变的结合能力,展现出更强的抑制活性和更高的选择性 [7]。
本病例中,患者一线使用阿来替尼治疗20个月后产生耐药,出现疾病进展,随后治疗方案调整为伊鲁阿克。治疗两个月后复查CT,结果显示纵隔淋巴结病灶较基线缩小,最佳疗效评估为SD,截至目前无进展生存期超13个月。这一治疗反应有力证明了伊鲁阿克在ALK-TKI耐药后的临床价值。
稳扎稳打,临床研究层层验证,伊鲁阿克为ALK阳性NSCLC患者筑牢获益 “堡垒”
此前,剂量递增及剂量扩展阶段的Ia/Ib期研究探寻了伊鲁阿克的最佳用药剂量及安全性[8],并确定了导入期给药方式:前7天60mg每天1次,若可耐受,则从第8天起提高到180mg每天1次。基于这些良好数据,研究者进一步开展了单臂、多中心II期INTELLECT研究,共入组146例接受克唑替尼治疗至少12周之后出现了疾病进展、经组织病理学或细胞学确诊的晚期ALK阳性NSCLC患者,结果显示,独立评审委员会评估的客观缓解率达69.9%,中位无进展生存期(mPFS)达19.8个月[9],延长随访后,中位总生存期(mOS)达到41.8个月[10],同时安全性依然良好。
在此基础上,伊鲁阿克向ALK阳性NSCLC一线治疗发起挑战。INSPIRE III期临床研究结果显示,随着随访时间的延长,伊鲁阿克组的疗效愈发显著,特别是对于经中心实验室复检ALK阳性人群,伊鲁阿克治疗组的mPFS达45.9个月[12]。这一结果不仅彰显了伊鲁阿克在一线治疗中的卓越疗效,也为ALK阳性非小细胞肺癌的治疗策略带来了新的思考和方向。伊鲁阿克在一线治疗ALK阳性NSCLC中展现出优异PFS数据,为治疗策略提供了新的选择和参考。
安全性突出,医保范围扩大,伊鲁阿克不断拓展适应证,为肺癌治疗注入新活力
唐晓勇 教授
山东第一医科大学附属肿瘤医院
医学博士、教育学博士后
呼吸内科二病区主任,主任医师
山东省肿瘤质控中心肺癌学组秘书
山东省肿瘤医院肺癌MDT专家成员
山东省研究型医院协会肺癌转化医学分会主任委员
山东省研究型医院协会肿瘤协作分会副主任委员
山东中西医结合学会肿瘤专业委员会副主任委员
山东省抗癌协会肺癌专业委员会常委
山东省抗癌协会小细胞肺癌分会常委
中国抗癌协会化疗专业委员会青年委员
山东省医学会流行病学与循证医学分会青年学组委员
山东第一医科大学附属肿瘤医院
山东第一医科大学附属肿瘤医院呼吸内科二病区科主任助理
硕博连读毕业于北京协和医学院/中国医学科学院肿瘤医院
山东第一医科大学骨干人才
第一届山东省研究型医院协会肺癌转化医学分会学术秘书
第一届北京整合医学学会胸部肿瘤精准诊疗分会委员
第二届山东省医学会类器官分会青年委员
从事肺癌内科临床与基础转化研究,擅长非小细胞肺癌少见基因突变诊治
以第一作者于BMC Medicine、Lung Cancer、Therapeutic Advances in Medical Oncology等知名杂志发表SCI等论文26篇,相关临床研究成果多次于ASCO/WCLC/ELCC等国际学术会议展示
参考文献
本文由唐晓勇教授、杨广建主治医师审校
查看更多