查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





淀粉样变性是一组以淀粉样蛋白在全身组织器官沉积的疾病,常见的受累器官有肾脏、心脏、神经系统、胃肠道和肝脏。许多不同的蛋白质可以形成淀粉样原纤维,迄今为止,已经发现将近40种不同的蛋白质可以在体内形成淀粉样原纤维,其中系统性轻链型(AL型)淀粉样变性是最常见的系统性淀粉样变性类型。AL型淀粉样变性是一种浆细胞疾病,其前体蛋白来源于异常浆细胞克隆产生的游离轻链,后者形成的淀粉样物质沉积于组织器官造成病变。从发病率来看,AL型淀粉样变性发病率在9~14例/100万人口/年,在我国属于罕见病目录中的病种。AL型淀粉样变性的起病隐匿,临床表现多样,临床易误诊及漏诊,预后也具有很强的异质性,与患者诊断时的器官受累程度密切相关,心脏受累严重的患者预后不佳。故提高广大医务工作者对AL淀粉样变性的认识,规范AL型淀粉样变性的诊治对提高患者的预后至关重要。
早在2016年,东部战区总医院国家肾脏疾病临床医学研究中心刘志红院士组织肾脏科和血液科的专家制定了我国首部《系统性轻链型淀粉样变性诊断和治疗指南》,对规范AL型淀粉样变性的诊治起到了推动作用。近年来,随着相关检测技术的提高和新药的不断问世,AL型淀粉样变性的诊治也有了很多进展,基于此,东部战区总医院国家肾脏疾病临床医学研究中心联合北京大学人民医院国家血液系统疾病临床医学研究中心及相关领域专家对AL型淀粉样变性诊断和治疗指南作了更新。
指南的主要内容包括九个部分,主要有疾病的定义与概况、临床表现、诊断标准分期及危险分层、鉴别诊断、诊断AL型淀粉样变性所需要的检查、疗效评估标准、治疗原则、治疗方案及随访监测。每个部分的重点内容总结如下。
AL型淀粉样变性是由单克隆免疫球蛋白轻链错误折叠形成淀粉样蛋白,并沉积于组织器官,造成组织结构破坏、器官功能障碍并进行性进展的疾病,主要与克隆性浆细胞异常增殖有关,少部分与淋巴细胞增殖性疾病有关。淀粉样蛋白具有如下特点:光镜下HE染色呈嗜伊红均质状,PAS染色呈弱阳性或阴性,Masson染色呈嗜亮绿;刚果红染色呈砖红色,偏振光显微镜下呈苹果绿色双折光;电镜下表现为直径8 - 14 nm、无分支、排列紊乱的纤维丝状结构;X线衍射显微镜下可见β片层结构。
AL型淀粉样变性的临床表现多样,可累及多个器官。肾脏及心脏是最常见的受累器官,其他受累器官包括肝脏、自主或外周神经、消化道、皮肤软组织等。具体临床及实验室检查特点见表1。对临床表现的认识可增加AL型淀粉样变性患的早期诊断率。
表1 AL型淀粉样变性器官受累的临床表现
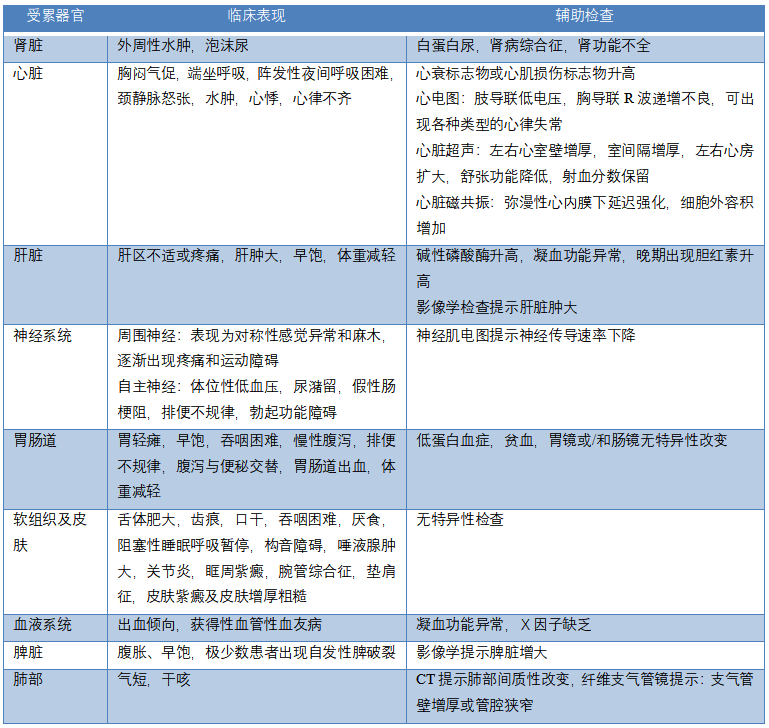
诊断AL型淀粉样变性需符合以下条件:(1)临床表现、体格检查、实验室或影像学检查证实有组织器官受累。(2)组织活检病理证实有淀粉样蛋白沉积,且淀粉样蛋白的前体蛋白为免疫球蛋白轻链或重轻链,具体病理表现为:①刚果红染色阳性,在偏振光下呈苹果绿色双折光;②免疫组化、免疫荧光或免疫电镜检查结果为轻链限制性表达,或质谱分析明确前体蛋白为免疫球蛋白轻链;③电镜下可见细纤维状结构,无分支,僵硬,排列紊乱,直径8~14nm。(3)血液或尿液中存在单克隆免疫球蛋白或游离轻链的证据,或骨髓检查发现有单克隆浆细胞/B细胞。确诊的患者可以使用表2的标准判断器官受累的范围。
表2 系统性轻链型淀粉样变性器官受累判断标准
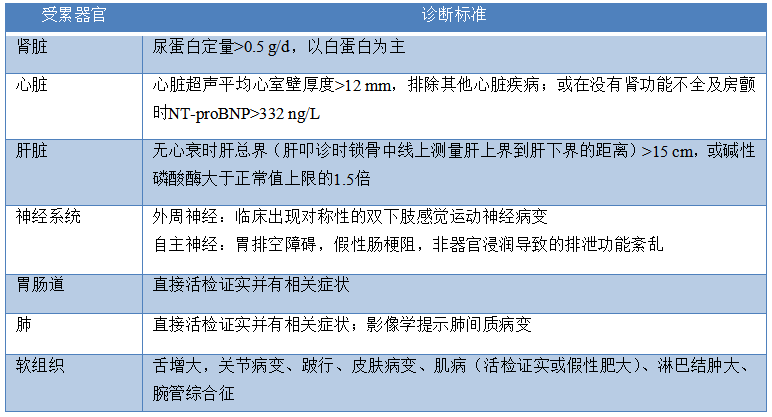 注:NT-proBNP为N端前脑钠肽
注:NT-proBNP为N端前脑钠肽
建议根据单克隆轻链类型和是否合并血液肿瘤对AL型淀粉样变性进行分型。根据组织病理结果中单克隆轻链沉积的类型,可将AL型淀粉样变性分为λ轻链型和κ轻链型。临床上以λ轻链型为主,约占85%。少数患者在轻链之外尚合并出现单一的重链或者片段,临床为重轻链型(AHL)淀粉样变性,此类患者在IgG分型中仅表达IgG1、IgG2、IgG3、IgG4中单一类型,或者IgA分型中仅表达IgA1、IgA2中单一类型。
临床常规使用梅奥2012分期系统判断预后,以心脏受累为主的患者建议使用梅奥2004分期系统,判断肾脏淀粉样变性进展建议使用肾脏预后分期系统,合并肾脏和心脏受累的患者建议使用南京预后分期系统。AL型淀粉样变性的预后分期系统的具体分级方法见表3。
表3 系统性轻链型淀粉样变性的常用预后分期系统汇总
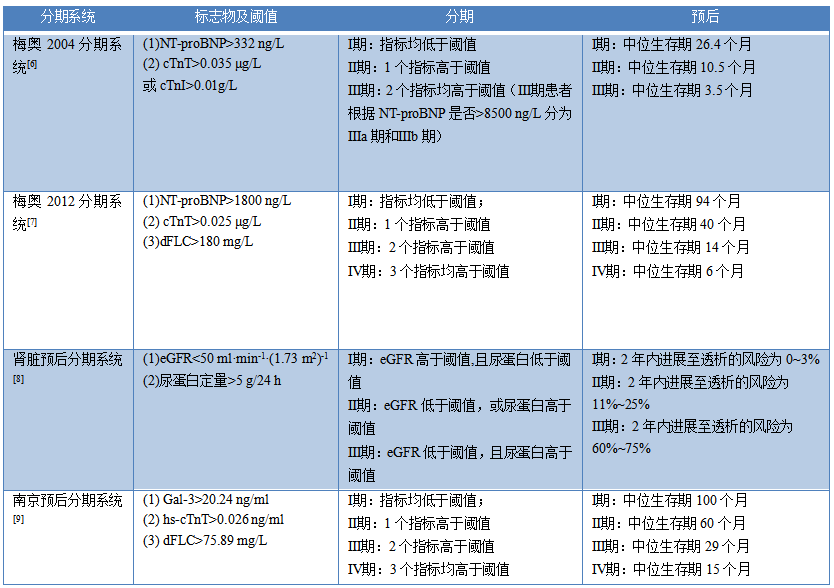 注:NT-proBNP为N端前脑钠肽;cTnT为血清肌钙蛋白T;cTnI为血清肌钙蛋白I;dFLC为血清游离轻链差值;eGFR为估算的肾小球滤过率;Gal-3为半乳糖凝集素-3;hs-cTnT为超敏肌钙蛋白T
注:NT-proBNP为N端前脑钠肽;cTnT为血清肌钙蛋白T;cTnI为血清肌钙蛋白I;dFLC为血清游离轻链差值;eGFR为估算的肾小球滤过率;Gal-3为半乳糖凝集素-3;hs-cTnT为超敏肌钙蛋白T
AL型淀粉样变性患者一般分为低危组、中危组和高危组。符合以下所有条件为低危组:美国东部肿瘤协作组(ECOG)体力状态评分0~2分;纽约心脏病学会(NYHA)分级Ⅰ~Ⅱ级;心脏超声射血分数>45%;NT-proBNP<5 000 ng/L;cTnT<0.06 μg/L;不吸氧血氧饱和度>95%;总胆红素< 34 μmol/L(2 mg/dl);基线收缩压>90 mmHg(1 mmHg=0.133 kPa)。中危组指不符合低危组条件且梅奥2004分期在Ⅰ~Ⅲa期患者。高危组指梅奥2004分期Ⅲb期或NYHA分级Ⅳ期的患者。
AL型淀粉样变性主要与下列两类疾病作鉴别诊断:一类是其他类型的淀粉样变性,另一类是M蛋白相关的其他疾病。其他类型淀粉样变性包括AA型淀粉样变性、遗传性淀粉样变性和局限性AL型淀粉样变性。M蛋白相关疾病的鉴别中,需明确AL型淀粉样变性是否继发于血液肿瘤,如多发性骨髓瘤、华氏巨球蛋白血症或B细胞淋巴瘤等;还需要与其他累及肾脏的单克隆免疫球蛋白病(MGRS)相鉴别。遗传性淀粉样变性种类较多,需要借助基因分析来进一步确诊,常见基因突变有TTR(编码甲状腺素转运蛋白)、APOA1,APOA2,APOC2和APOC3(分别编码载脂蛋白AI,载脂蛋白AII,载脂蛋白CII和载脂蛋白CIII)、FGA(编码纤维蛋白原α链),GSN(编码凝溶胶蛋白)、CSN3(编码胱抑素C)和LYZ(编码溶菌酶)等。对常规治疗鉴别困难的患者,质谱分析鉴定淀粉样变性的类型至关重要。此外,AL型淀粉样变性中约有5%的患者表现为局限性淀粉样变性,常见部位为膀胱、喉、胃、结肠、皮肤、眼睑、肺和泌尿道,这些患者不需要系统性治疗。
诊断AL型淀粉样变性所需的检查分为两部分进行,一是确诊AL型淀粉样变性所需的检查;二是明确受累组织器官范围及严重程度的相关检查。确诊淀粉样变性的检查主要通过组织活检来实现,一般选择淀粉样变性可能累及(临床症状或者实验室检查证实)的器官或组织进行活检,并结合临床易操作性和安全性。可选取的活检部位包括肾脏、心脏、皮肤脂肪、舌、骨髓、胃肠道等。淀粉样变性物质的分型检测包括免疫病理染色、免疫电镜和质谱分析,怀疑遗传性淀粉样变性者行相关基因检测。对受累器官/组织进行κ、λ轻链的免疫组化或免疫荧光染色,如呈现单一轻链阳性,即可明确诊断为AL型淀粉样变性。对所有患者应该行血清/尿蛋白电泳、血清/尿免疫固定电泳、血清游离轻链、骨髓单克隆浆细胞增殖(骨髓流式检查:CD38/CD138/CD45/CD56/CD19/CD20/cκ/cλ、骨髓活检κ/λ轻链免疫组化)等检查来获取AL型淀粉样变性的间接证据。
AL型淀粉样变性在诊断后还需要评估器官/组织受累及情况,一般来说一旦经过一个部位的病理活检证实为淀粉样变性后,其他器官/组织是否受累不需要再行病理活检,而是通过影像学、实验室检查以及相关的临床表现来证实。具体判断标准见表2。
疗效评估是AL淀粉样变性患者治疗过程中的重要组成部分,所有接受抗浆细胞治疗的患者应定期进行血液学和器官疗效评估。血液学评估需根据患者基线血清游离轻链差值(dFLC)水平选择合适的标准,dFLC>50 mg/L的患者所有血液学反应均可评估,dFLC水平在20~50 mg/L的患者可评估完全缓解(CR)和部分缓解(PR),dFLC<20 mg/L的患者目前仍无法评估血液学疗效。器官反应中可评估的疾病标准为:心脏:NT-proBNP>650 ng/L或BNP>150 ng/L;肾脏:尿蛋白定量>0.5g/24h;肝脏:碱性磷酸酶>1.5倍正常值上限。表4和表5分别是血液学疗效评估标准和器官疗效评估标准。本次疗效评估较之前的指南有较大的更新,主要是扩大了可评估患者的范围,使更多的患者可以评估疗效,另外对评估的标准进行了细化,强调了更高质量的血液学缓解和器官缓解对患者预后改善的重要作用。
表4 系统性轻链型淀粉样变性的血液学缓解和进展标准
 注:iFLC为血清受累游离轻链;dFLC为血清游离轻链差值
注:iFLC为血清受累游离轻链;dFLC为血清游离轻链差值
表5 系统性轻链型淀粉样变性的器官缓解和进展标准
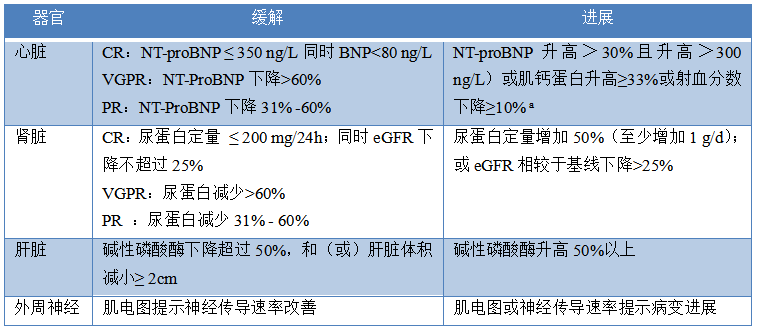 注:本标准综合了NCCN
2021版系统性轻链型淀粉样变性指南和2020年第17届国际淀粉样变性研讨会对器官反应标准的更新内容;a肾功能进行性恶化的患者无法评估NT-proBNP进展;CR为完全缓解;VGPR为非常好的部分缓解;PR为部分缓解;NT-proBNP为N端前脑钠肽;eGFR为估算的肾小球滤过率
注:本标准综合了NCCN
2021版系统性轻链型淀粉样变性指南和2020年第17届国际淀粉样变性研讨会对器官反应标准的更新内容;a肾功能进行性恶化的患者无法评估NT-proBNP进展;CR为完全缓解;VGPR为非常好的部分缓解;PR为部分缓解;NT-proBNP为N端前脑钠肽;eGFR为估算的肾小球滤过率
AL型淀粉样变性的患者一经确诊,应当按照预后分期、受累脏器功能、体能状况及可获得的药物尽早开始治疗。治疗目标是降低体内单克隆免疫球蛋白轻链的水平,阻止淀粉样蛋白在重要脏器的进一步沉积,减轻或逆转淀粉样蛋白沉积导致的器官功能障碍。实现上述治疗目标的主要方法是清除产生异常轻链的浆细胞或B细胞克隆。建议治疗过程中遵循以下原则:(1)符合自体造血干细胞移植条件的患者应首选移植,特别是浆细胞比例大于10%的患者应积极选用自体造血干细胞移植治疗,并在未获得微小残留病灶(MRD)阴性的患者中加用维持治疗,拒绝移植的患者也可选择激素、烷化剂、免疫调节剂、蛋白酶体抑制剂以及抗CD38单抗等药物的联合方案治疗;(2)不符合移植条件的患者,推荐含硼替佐米的联合治疗方案,每2疗程后再次评估是否符合移植条件;(3)三药的联合方案疗效优于两药,但需综合考虑患者耐受性和药物不良反应等因素选择联合治疗方案;(4)血液学不能达到非常好的部分缓解(VGPR)及以上疗效的患者应考虑进行巩固治疗;达到VGPR及以上疗效的患者,可考虑停药观察;(5)对于复发难治的AL型淀粉样变性的患者,若条件符合,推荐优先参加临床试验。
目前AL型淀粉样变性的主要治疗方案都是针对克隆性浆细胞的治疗,初治患者推荐的治疗方案见表6。两个疗程后血液学疗效评估为PR及以下疗效的患者需及时更换为二线方案以争取更好的血液学缓解和最大程度的重要器官缓解。
表6 初治AL型淀粉样变性患者的可选方案
 a:符合移植条件的患者,如患者拒绝接受移植,也可选择含美法仑的方案。DARA为达雷妥尤单抗
a:符合移植条件的患者,如患者拒绝接受移植,也可选择含美法仑的方案。DARA为达雷妥尤单抗
符合移植条件的初治AL型淀粉样变性患者中首选ASCT治疗;也推荐在经过抗浆细胞治疗后状态改善,转为符合移植条件的患者中进行ASCT治疗。初诊不适合移植的患者应在治疗2疗程后再次评估是否符合移植条件。移植适应证:(1)年龄<70岁;(2)ECOG评分0-2分;(3)NYHA分级Ⅰ-Ⅱ级;(4)心脏超声射血分数>45%,NT-proBNP<5000 ng/L,TnT<0.06 ng/ml;(5)不吸氧血氧饱和度>95%;(6)总胆红素<2 mg/dl;(7)基线收缩压>90 mmHg;(8)eGFR>30 ml·min-1·(1.73 m2)-1;(9)无大量浆膜腔积液;(10)无活动性感染。
AL型淀粉样变性疾病复发进展的标准根据血液学及器官分别定义,满足任何一条均定义为复发进展,详见表4和表5。难治定义为初治患者对一线治疗方案无效,需要更改一线治疗方案并开始二线治疗。其治疗原则如下:①有合适临床试验者,参加临床试验;②既往治疗有效且缓解持续时间>12月,可以采用既往治疗方案再治疗;③换用以前未曾治疗的新的方案:未使用蛋白酶体抑制剂,可以使用硼替佐米或伊沙佐米;对蛋白酶体抑制剂耐药,改用IMiDs(如来那度胺、泊马度胺),或者DARA;如果没有使用过烷化剂,可以使用美法仑-地塞米松或苯达莫司汀;适合移植患者,可以考虑自体干细胞移植。
支持治疗是AL型淀粉样变性治疗的重要组成部分。有肾脏和心脏受累的患者应给予低盐饮食,每日钠盐摄入量<6g;保持容量稳定,避免容量负荷的快速增加或减少;每日监测体重、尿量、血压、心率等基础生命体征。肾脏受累的支持治疗:(1)以肾病综合征为主要表现的患者主要是利尿治疗,常用药物有呋塞米、螺内酯、氢氯噻嗪和复方阿米洛利,有腹腔积液的患者可选择托伐普坦,用药过程中,应监测容量状态、血压、电解质等指标;(2)建议白蛋白<20g/L且无出血倾向的患者常规抗凝治疗;(3)在合并心脏或自主神经系统受累的患者中,尤其在存在低血压的情况下,应避免使用血管紧张素转化酶抑制剂(ACEI)和血管紧张素受体拮抗剂(ARB);(4)终末期肾功能衰竭的患者应适时开始透析治疗,综合考虑患者年龄、肾外器官受累的严重程度以及抗浆细胞疗法的可及性等因素选择血液透析或腹膜透析;(5)受累游离轻链>500mg/L同时合并急性肾损伤的患者,可联合高截留量透析治疗,有高粘滞血症症状的患者建议行血浆置换治疗;(6)符合肾移植受者标准的患者可接受肾移植治疗,患者肾移植前应获得血液学完全缓解。心脏受累的支持治疗:(1)心功能不全患者以控制容量为主,避免使用洋地黄类药物或β受体阻滞剂;(2)胺碘酮是控制心室率的首选药物,β受体阻滞剂仅限于其他治疗方案无效的房颤合并快速心室率患者;(3)非二氢吡啶类钙离子通道阻滞剂(如维拉帕米和地尔硫卓)可与淀粉样蛋白原纤维紧密结合,有加重心衰、严重低血压和晕厥的风险,在心脏淀粉样变性患者中禁用;(4)心脏起搏器适用于有心脏传导阻滞或症状性心动过缓的患者,有晕厥病史的患者,应将放置起搏器的适应证放宽;(5)存在与血流动力学不稳定相关的室性心律失常且预期寿命>1年的患者可考虑植入埋藏式心律转复除颤器(ICD);(6)AL型淀粉样变性导致的心力衰竭患者,因心血管疾病不能耐受原发病的治疗,可以在经验丰富的中心进行心脏移植治疗。其他的支持治疗包括外周神经受累和胃肠道受累的支持以及体位性低血压的处理。
一般治疗期间每个疗程后评估血液学疗效,对于完成治疗后的患者则建议规律随访,每3-6个月评估血液学疗效。所有患者首先评估血清游离轻链定量。对于诊断时骨髓浆细胞>10%的患者随访时需要进行骨髓检查,包括骨髓穿刺和活检,按照多发性骨髓瘤的随访每3-6个月进行检查。建议有条件的患者进行微小残留病灶(MRD)检测。治疗期间每3个月评估器官功能缓解情况,治疗结束后每3-6个月评估一次。随访内容包括:24小时尿蛋白定量、血清肌酐和eGFR、碱性磷酸酶等肝功能指标、心肌标志物(cTNT、cTNI和NT-proBNP));必要时复查心电图、心脏超声、MRI等。最低随访要求:心脏淀粉样变性每3-6个月必须要随访NT-proBNP水平变化;肾脏淀粉样变性每3-6个月定期随访24小时蛋白尿变化;肝脏淀粉样变性则需要每3-6个月随访碱性磷酸酶变化。
AL型淀粉样变性是一种典型的多学科诊疗模式病种,诊断和治疗均有其特殊之处。诊断上应重视早期症状的甄别和M蛋白的筛查,及早发现疑似病例,并通过组织活检明确诊断。治疗应建立在器官功能全面评估和危险分层的基础上,结合药物的可及性和毒副作用选择合理的治疗方案,同时治疗过程中应注意重要器官的支持治疗和并发症的预防。
来源:东部战区总医院供稿,摘自《肾脏病与透析肾移植杂志》
查看更多