查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





CAR-T细胞疗法是目前处于国际顶尖水平的生物免疫治疗,利用患者自身的免疫细胞,经体外改造成可以识别肿瘤特异靶点的T细胞,能够精准识别恶性血液肿瘤细胞并将其清除。
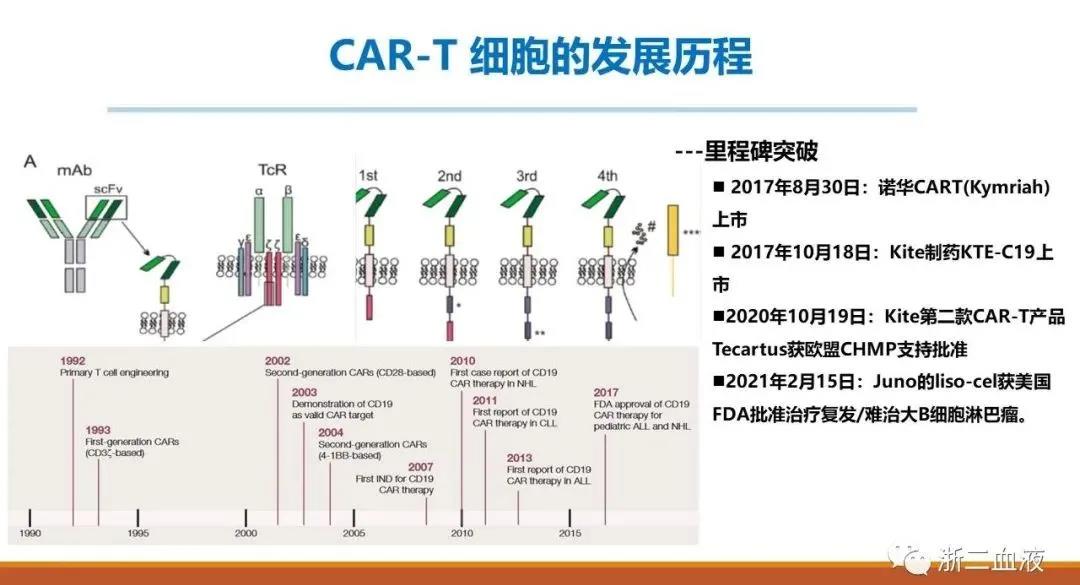
CAR-T细胞治疗B细胞淋巴瘤的有效率可达60%,大大提高了复发/难治性B细胞淋巴瘤患者生存期,改善生活质量。目前,CD19-CAR T治疗淋巴瘤的临床研究汇总如下:
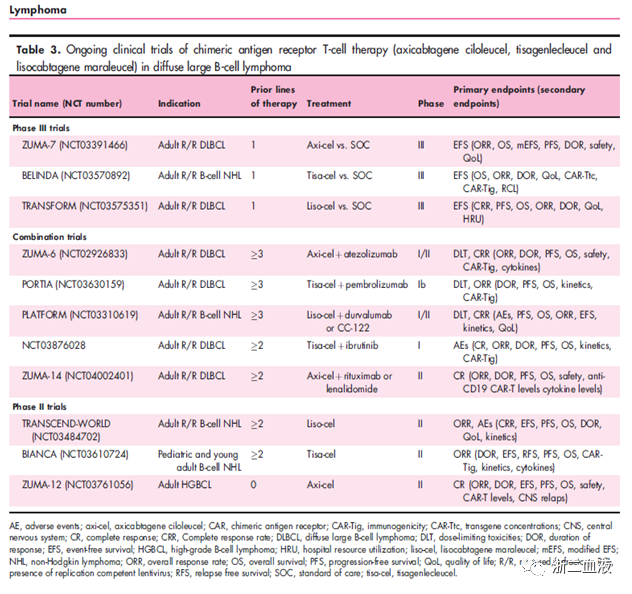
表格来源:Curr Opin Oncol. 2020
CAR T治疗也受到各种条件的制约,包括:CAR T制备失败,治疗过程中出现脱靶效应,CAR T毒性反应以及特定类型受限。
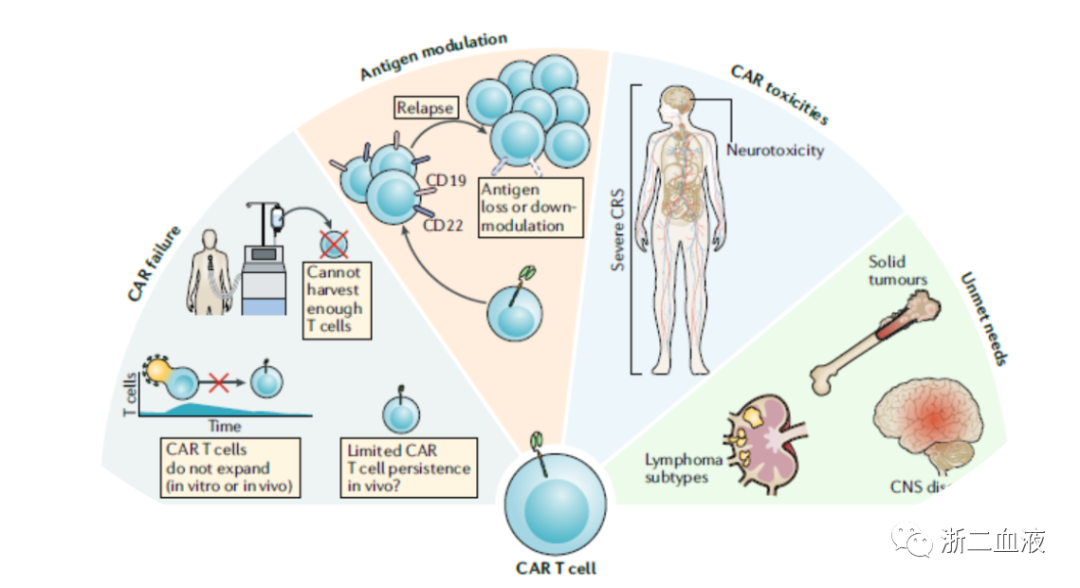
图片来源:Clinical Oncology, 2019
浙江大学医学院附属第二医院已成功开展以CD19为靶点的CAR-T细胞疗法治疗复发/难治性B细胞淋巴瘤,有强大的科研临床团队和丰富的CAR-T制备及治疗经验。目前采用
新型第四代CAR-T疗法提高治疗NHL的疗效,其作用机制涉及:
(1)阻断PD-1/PD-L1抑制信号;
(2)将PD-1/PD-L1的抑制信号转变为PD-1/CD28的激活信号,激活CD28-B7-1共刺激信号;
(3)联合41BB共刺激信号,发挥双重的共刺激作用。
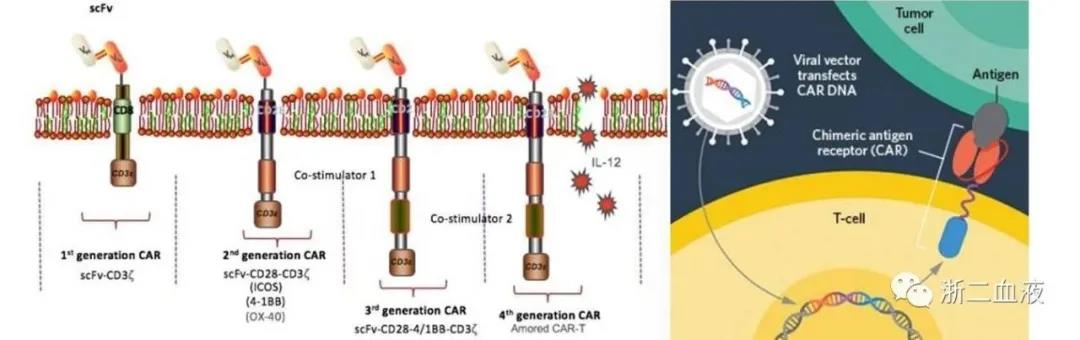
在前期研究中发现,低剂量Decitabine可以通过表观遗传学修饰增强CAR-T细胞持久抗肿瘤作用。
现正式公开招募复发/难治性B细胞淋巴瘤患者,本项目研究已经获得浙江大学医学院附属第二医院临床研究伦理委员会批准。
项目名称
携带PD-1/CD28转换受体的新型CAR-T细胞序贯低剂量地西他滨治疗复发/难治性B细胞淋巴瘤的临床研究。
患者入选标准
受试者必须符合下列所有标准才能入选
(1)年龄≥18岁,上限75岁,男女不限;
(2)ECOG评分0-3;
(3)组织学确诊弥漫大B细胞淋巴瘤(DLBCL)、转化滤泡淋巴瘤(TFL)、原发性纵隔B细胞淋巴瘤(PMBCL)、套细胞淋巴瘤(MCL)、其他惰性B细胞NHL转化型和难治或复发惰性B细胞NHL
(4)肿瘤组织CD19阳性(免疫组化或流式细胞仪)。
(5)患者先前治疗必须包括美罗华(CD20单抗)和蒽环类;
(6)至少有一个可测量的病灶,要求淋巴结病灶任一长径大于1.5cm 或结外病灶任一长径大于1.0 cm,PET-CT扫描病灶有摄取(SUV大于肝血池);
(7)外周血中性粒细胞绝对值≥ 1000/μl、血小板≥4.5万/μl;
(8)心、肝肾功能:肌酐<1.5mg/dL;ALT(谷丙转氨酶)/ AST(谷草转氨酶)正常上限的2.5倍以下;总胆红素<1.5mg/dL;心脏射血分数(EF)≥50%;
(9)有足够的理解能力和自愿签署知情同意书;
(10)有生育能力者必须愿意使用避孕方法;
(11)经研究者判断,预计生存期至少超过4 个月;
(12)愿意遵守访视时间安排、给药计划、实验室检查以及其他试验步骤。
排除标准
受试者符合下列任意一条标准均不能进入本研究:
(1)有其他肿瘤病史;
(2)6周内进行过自体造血干细胞移植;
(3)本次CAR-T治疗前3个月内曾行任何靶点CAR-T治疗;
(4)采细胞前2周内接受过细胞毒药物和其他靶向药物;
(6)活动性自身免疫性疾病;
(7)不能控制的活动性细菌、真菌感染;
(8)HIV感染、梅毒感染;活动性乙肝或丙肝:乙肝:HBV-DNA阳性;丙肝:HCV RNA阳性且肝功能异常。
(9)已知的中枢神经系统淋巴瘤。
如果您符合以上条件,并自愿参加本项研究,本院研究医生将对您进行相关检查。筛查结果经研究医生评估后,您若符合本研究的所有入组标准,同时充分了解该研究,并签署《知情同意书》后,方能正式进入本项研究。对于正式进入研究的患者,研究医生会根据研究方案和流程,制定诊疗及随访计划。
浙二血液 平台发布
查看更多