查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:北京协和医院 尹翮翔
一、多发性硬化(MS)残疾进展评估研究
MS的诊疗已进入着重关注残疾进展的时代。在本次AAN年会中,来自不同国家和地区的学者分别进行了多发性硬化预后生物学标志物的研究报告,包括神经丝轻链蛋白(Neurofilament light,NfL)、胶质纤维酸性蛋白(glial fibrillary acidic protein,GFAP)、端粒长度、外周血RNA谱、铁代谢遗传变异等。

Nfl是神经轴索细胞骨架中间蛋白,GFAP是星形细胞中间蛋白,两者均存在于血浆和脑脊液中,前者与MS复发相关,后者与MS非复发性进展相关,因此将两者结合起来可能作为MS的预后生物学标志物。来自加拿大渥太华医院的研究团队报道了一项Nfl和GFAP在MS长期临床结局方面的单中心回顾性队列研究。
研究纳入标准:有MS发病后5年内血清和脑脊液标本;随访15年以上;在生物样本库中标本可获得。
研究方法:超敏单分子免疫阵列(single molecule array,SiMOA)法进行Nfl和GFAP检测,对血清Nfl进行年龄校正。结局变量:确认的残疾进展(CDW),定义为2次相隔6个以上的访视EDSS增高(a.基线EDSS为0,增高≥1.5;b.基线EDSS 1-5,增高≥1;基线EDSS >5,增高≥0.5) 。
研究结果:研究共纳入60例患者,女性42例(70%),平均年龄39(±9)岁;首次诊断疾病类型CIS 17(28%)例,RRMS 31例(52%),PPMS 12例(20%);基线中位EDSS 2(1);平均随访期17.6(±2.9)年,末次随访中位EDSS 3(4.3)。
1. 血清脑脊液参数相关性
血清Nfl和脑脊液Nfl显著相关,r=0.86(0.78-0.92),p=0.0001;而血清GFAP和脑脊液GFAP相关性较弱,r=0.5(0.29-0.67),p=0.0001
2. s/cNfl和GFAP与CDW相关性
ROC显示年龄校正血清NFL(AAsNfl)>脑脊液NFl,而脑脊液GFAP(cGFAP)>>血清GFAP,但将AAsNfl和cGFAP联合时ROC并未比AAsNfl单一指标增加。COX等比例风险回归模型显示在调整了基线EDSS、分型、治疗等因素后AAsNFL和cGFAP水平均与长期的CDW独立相关。进一步将60例患者的年龄校正血清Nfl和脑脊液GFAP按照百分位和数值进行五分位排序,并分成5组,显示血清Nfl和脑脊液GFAP最高组(Group 5)相较于最低组(Group 1)出现CDW的风险绝对增高,出现CDW的中位时间分别为6.6(3.4-9.8)年和15.4(14.1-16.8)年(p=0.0053)。

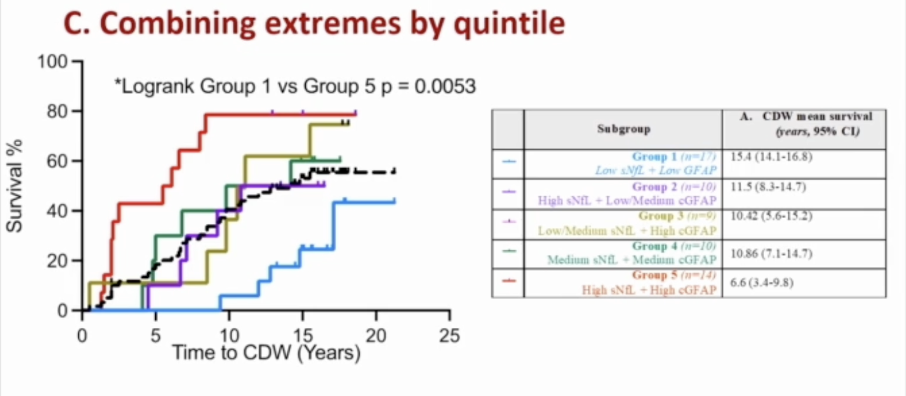
研究结论:MS患者CDW预后相关因素为脑脊液GFAP而非血清GFAP,血清Nfl和脑脊液GFAP均与之独立相关,两者结合的极值最有预后诊断价值。
而与之类似地,来自美国西奈山伊坎医学院的学者报道了一项Nfl与复发缓解型MS患者残疾进展相关性前瞻性纵向队列研究,分析对诊断5年内的复发型MS患者随访3年时的Nfl水平与EDSS评分增加的相关性。

研究纳入112例患者,女性74例(66.1),平均年龄37.2(±7.9)岁,基线中位EDSS 1.0(0,1.5),末次随访中位EDSS 1.0(0,2.0)。研究结果显示EDSS恶化患者组(n=31)血清Nfl水平显著增高(8.91(7.31,11.35)vs. 6.67(4.35,9.83),p<0.001),Nfl在90百分位以上的患者比例显著增加(55% vs. 22%, p<0.001)。此外,Nfl水平与EDSS变化值显著相关(r=0.344,p<0.001);Nfl水平在90百分位以上者的EDSS数值变化更显著(1(0,1.5)vs0(-1,1),p<0.001)。进一步分析发现,Nfl水平越高,脑萎缩越显著(r=-0.33,p<0.001)。多因素Logistic回归分析发现Nfl在90百分位以上与EDSS恶化显著独立相关(OR=5.24,95%CI 1.55-17.79,p=0.008)。
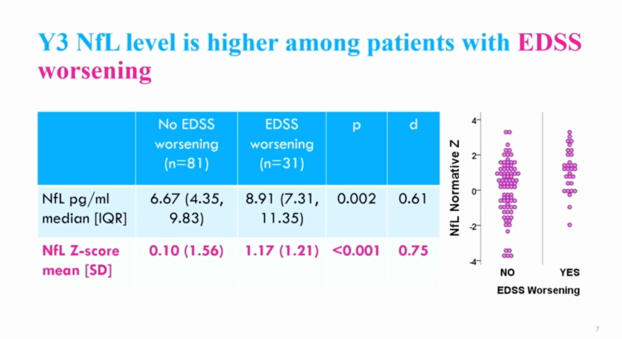
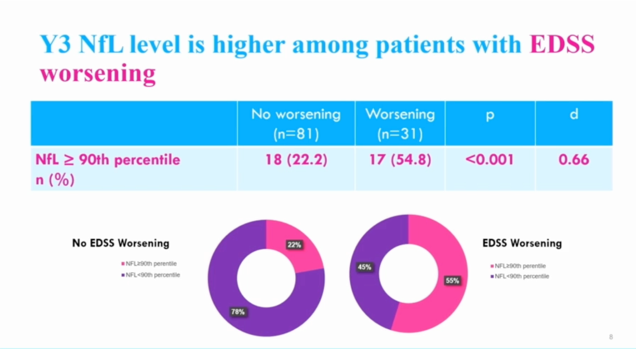
研究结论:即使在疾病早期进行Nfl采集,即使在使用高效治疗的早期RRMS患者中,校正的Nfl水平仍与独立于复发和脑萎缩的EDSS评分恶化显著相关。升高的NfL水平可能会为早期识别RRMS患者治疗同时伴随的潜在残疾进展提供辅助作用。
二、MS治疗研究
MS的治疗逐渐步入B细胞治疗时代,在本次AAN年会中,不同学者报道了B细胞靶向治疗在MS患者中的应用研究。来自瑞士的学者报告了奥瑞珠单抗IIIb期临床研究12个月中期分析,结果显示在经过1年治疗后所有B细胞亚型水平均耗竭,但CD4+或CD8 +T细胞无显著变化,奥瑞珠单抗对外周血免疫细胞亚型的长期影响还需要更长的时间观察。

来自美国的研究者报告了长程奥法妥木单抗治疗对MS患者残疾进展和脑萎缩的影响,研究发现在经过长达5年及以上的奥法妥木单抗治疗后,80%以上的患者可以维持6个月无确认的残疾进展;相比于初始随机至特立氟胺治疗组的患者,持续接受奥法妥木单抗治疗的患者更少出现残疾相关事件(包括独立于复发活动的进展PIRA和复发相关恶化RAW),同时这部分患者会出现很少的脑萎缩改变(小于1.5%),并且相较于后期换用者,早期起始奥法妥木单抗治疗者脑萎缩显著降低。研究结论支持在复发型MS患者中早期使用奥法妥木单抗。

除了单抗类药物,布鲁顿氏酪氨酸激酶抑制剂(BTKi)类药物在MS患者中的治疗研究也十分亮眼。其中Evobrutinib在复发型MS患者II期临床试验3.5年的开放标签研究(OLE)结果显示75mg BID是最优效给药剂量,在所有的治疗组,相比于每日1次用药(ARR 0.13-0.30),每日两次用药(ARR 0.07-0.12)可以使年复发率(ARR)更低。另外,在所有的治疗组,T1钆增强病灶平均数目持续维持在较低水平,从0-192周的平均EDSS评分保持在低水平,FSS评分保持稳定。安全性方面,并未观察到比双盲阶段更多的安全事件问题。研究表明在复发型MS患者治疗4.5年时间里,Evobutinib的有效性和安全性持续得到证实。

另有研究者报道了BTKiEvobrutinib相比于CD20单抗在治疗中枢神经系统局限性炎症方面的优效性研究,结果表明与CD20单抗不同,Evobrutinib并不会耗竭中枢神经系统中的B细胞,同时可以降低中枢神经系统髓样细胞、小胶质细胞、T、B细胞的活性,缓解动物EAE模型的症状。

Tolebrutinib治疗复发型多发性硬化(RMS)的2b期长期扩展研究(LTS)试验2.5年的结果显示截止到2022年7月参与LTS试验的129例患者中107例(85.6%)仍在接受治疗;接受tolebrutnib60mg/日8周及以上的患者,ARR维持在低水平[0.20(0.15-0.28)],而且约73%的患者到120周仍维持无复发状态。LST研究没有发现更多的安全性问题。结果表明为期120周的长期扩展研究,tolebrutinib60mg/日治疗展现出持续良好的耐受性,并且与低水平的ARR和稳定的残疾情况相关。

除了DMT治疗,来自澳大利亚的研究者MichaelBarmett报道了MS辅助药物CNM-Au8(一种具有催化活性、表面清洁、浓缩的金元素多面纳米晶体的水悬浮液)的治疗研究VISIONARY-MS.

研究设计:VISIONARY-MS是一项为期48周,多中心、随机、双盲、安慰剂对照II期临床试验,共纳入73例患者,旨在评估CNM-Au8(15mg/30mg)作为辅助疗法治疗有慢性视力障碍病史的稳定RRMS患者的疗效和安全性。主要终点是患者的最佳矫正低对比度字母敏锐度(BC-LCLA)评分的变化,次要终点是患者经调整的功能综合评分(mMSFC)的变化。
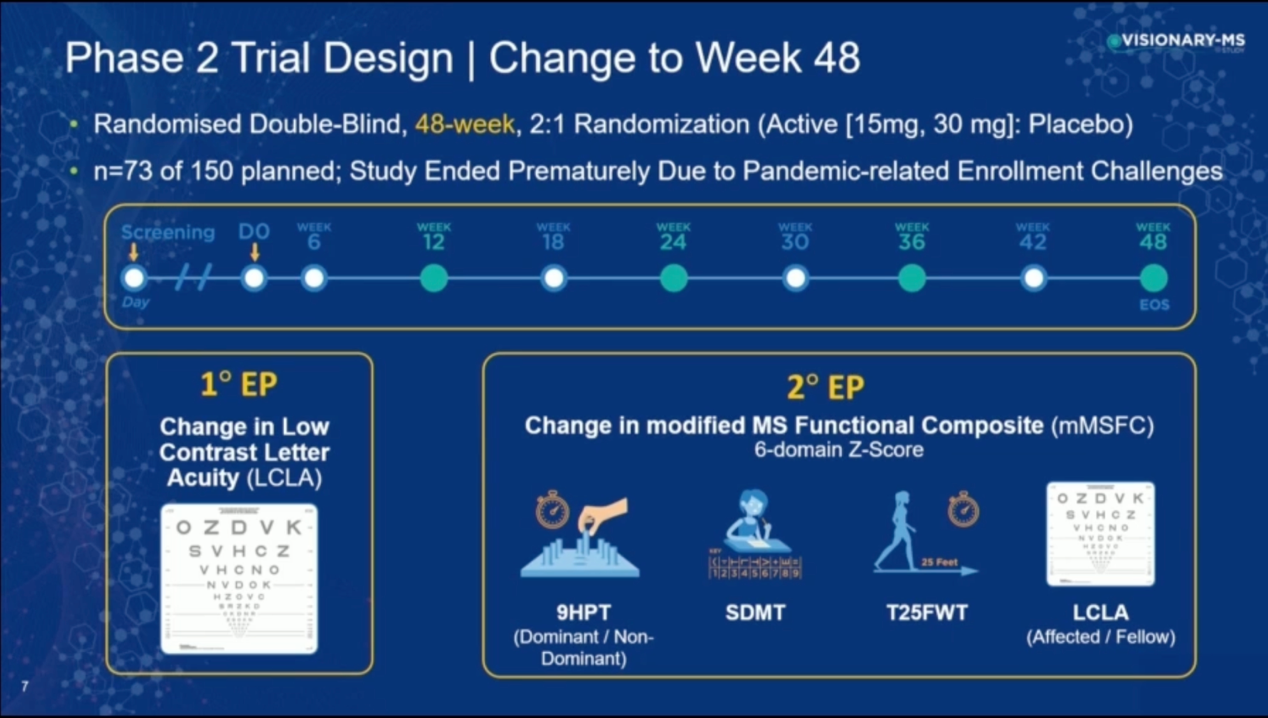
研究结果:在调整后的意向治疗人群(mITT)中,CNM-Au8组LCLA评分变化的最小二乘法(LS)平均差为3.13(95%CI: -0.08-6.33, p=0.056),mMSFC平均标准化差值的LS平均差为0.28(95%CI: 0.05-0.51, p=0.0197)。此外,在其他的临床指标如多灶性VEP及MRI弥散张量成像(DTI)方面也提示CNM-Au8可以增强神经轴索的完整性。不良反应方面CNM-Au8具有良好的耐受性,没有报告严重的安全事件。
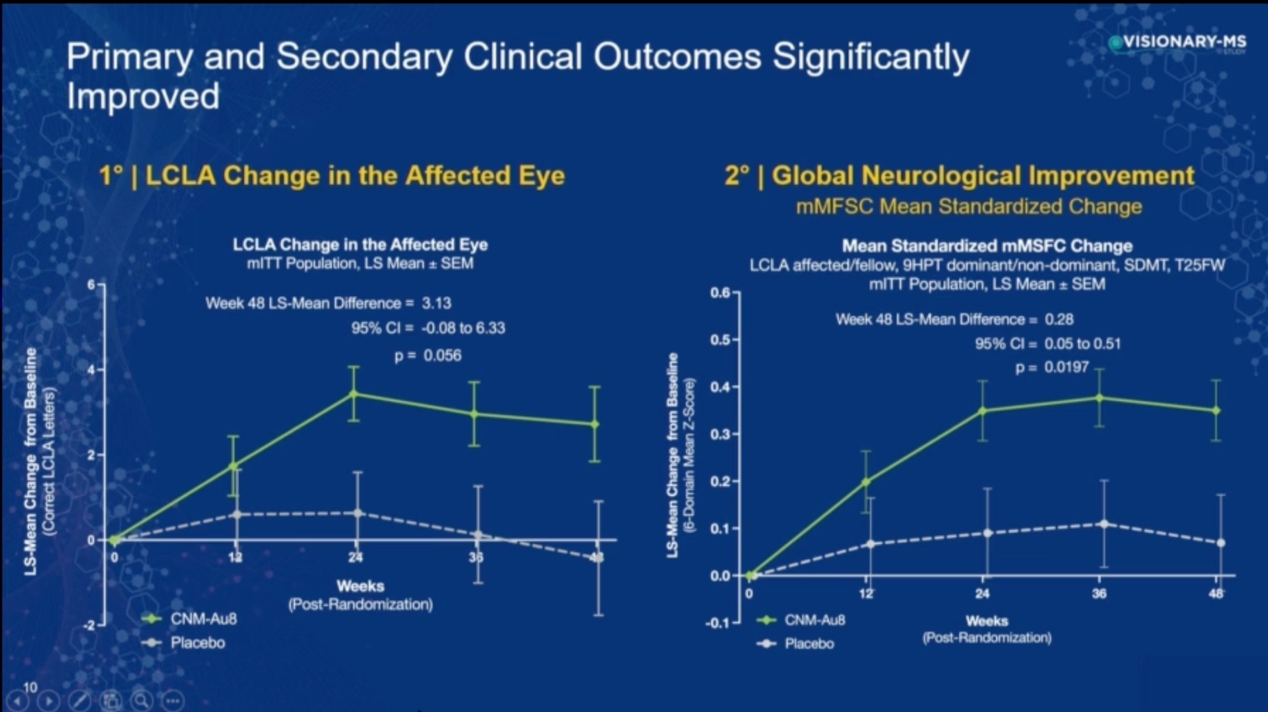
研究结论:研究证明CNM-Au8使MS患者的神经轴在结构性和功能性上均得到改善,其作为疾病修饰治疗(DMT)药物的辅助疗法可安全有效地改善稳定复发性MS患者的神经系统功能。
查看更多