查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





消化道肿瘤包括食管癌、胃癌以及结肠癌,是肿瘤相关死亡的重要原因。2021年,消化道早癌领域在筛查策略、内镜下治疗新技术等方面有诸多进展,《中国医学论坛报》特别邀请首都医科大学附属北京友谊医院张澍田教授团队对研究进展进行总结,以飨读者。
作者:首都医科大学附属北京友谊医院 秦达 何振 程芮 张澍田

张澍田教授
早期消化道肿瘤症状不明显, 具有起病隐匿的特点,预后较好,而晚期消化道肿瘤预后极差。提高人群中的早癌诊断率是降低消化道肿瘤相关死亡的重要手段。2021年消化道早癌的早期诊断领域出现了很多新方法、新技术,以下将从筛查方面对其中的显著成果进行总结。
1
筛查的人群选择
肿瘤高风险人群的界定对于早癌筛查工作来说非常重要,过宽的筛查范围常常导致不必要的人力、物力的浪费,而过窄的筛查范围会导致早期肿瘤病例的漏诊。因此,合理认识癌前疾病,针对不同的人群制定筛查策略是必要的。针对这一问题,《消化道》(Gut)杂志发表了一篇来自新加坡的前瞻性、多中心的研究,该研究纳入了从2004年1月至2010年12月接受过胃镜检查和标准化活检的2980名受试者,并进行间隔3年或5年的胃镜监测,其中21名受试者被诊断为早期胃癌。经过统计,研究者发现肠化是胃早癌的重要风险因素(HR 5.36;95% CI 1.51-19.0;P<0.01)。根据可操作的与胃癌风险联系的肠化生评估(OLGIM),OLGIM Ⅲ-Ⅳ期的患者进展为胃癌的风险最大[风险比(HR) 20.7; 95% CI 5.04 - 85.6; P<0.01]。超过半数的早期胃癌是从OLGIM Ⅲ-Ⅳ期的基础上在2年内(12.7-44.8月)发展而来的。而OLGIM Ⅱ期的受试者也同样面临着早期胃癌的风险(HR 7.34;95%CI 1.60 - 33.7;P=0.02),吸烟史使风险进一步增加。基于以上数据,作者建议采用风险分层的方法,建议在非胃癌高发地区的患者中,高风险患者(OLGIM Ⅲ-Ⅳ期)在2年内进行内镜检测,对中风险患者(OLGIM Ⅱ期)在5年内进行内镜监测。
同样来自Gut杂志的一项研究将目光聚焦到了消化道肿瘤的高风险地区。该研究共纳入中国的六个上消化道肿瘤高发地区且年龄位于40~69岁之间的637500名受试者作为研究对象,将受到邀请并行内镜检查的受试者归于筛查组,未被邀请的受试者作为对照组。最终,有113 340人接受了内镜检查,结果提示,与对照组相比,筛查组的上消化道肿瘤发病率、死亡率分别下降了23% [危险比(RR) = 0.77, 95% CI 0.74 - 0.81]和57% (RR=0.43, 95% CI 0.40 - 0.47)。研究者根据这些数据得出结论,在上消化道癌高风险地区,40~69岁的人群进行内镜筛查可以显著下降上消化道癌发病率与死亡率。
2
筛查的方法创新
消化道的肿瘤筛查旨在发现早期消化道肿瘤,从而降低其发病率与死亡率,方法包括肿瘤标记物、粪便免疫化学测试(FIT)、内镜检查等。其中,使用内镜作为初步筛查手段可以检测出大部分消化道肿瘤,但对于医保系统来说过于昂贵,替代的筛查方法例如FIT是很好的初筛手段。但目前大部分的FIT实验对所有的参与者使用相同的临界值,影响其准确性,为解决这一问题,发表在《消化内镜》(Gastrointest Endosc)中的一项研究找到了针对特定年龄、性别的临界值,以改善FIT的准确性。该研究共纳入531828名参与者,数据显示,降低老年人的临界值、提高年轻人的临界值可以提高FIT整体的敏感性与特异性,减少7%的结肠镜检查的需求,增加1.1%的肿瘤发现率,增加5%的腺瘤发现率,对提高临床筛查的准确性有较大帮助。研究者同时指出,不同的临界值选择会增加不同组间敏感性、特异性的不平等,存在一定的风险。
除了传统的肿瘤标记物、FIT、常规内镜检查外,研究者们创新性地研发出了多种新型早期肿瘤筛查的方法,这些方法以血浆中的游离遗传物质作为基础,具有无创、易行的特点,极具临床转化潜能,被称为“液体活检”技术。细胞外囊泡(EV)作为血浆中遗传物质的一种载体,是一种良好的生物标记物。在2021年,发表在《先进科学》(Adv Sci)杂志上的一篇来自首都医科大学附属北京友谊医院消化科团队的EV相关综述详细的介绍了各类分离、检测EV的纳米技术,针对EV的不同理化性质制定了各种不同的分离策略,重点探讨了EV在液体活检领域所面临的挑战,并提出了基于EV的液体活检与材料学交叉学科解决问题的可行性,这些工作为EV的进一步临床转化提供了思路。另外,发表在《血液与肿瘤学杂志》(J Hematol Oncol)中的一项研究使用血浆cell-free DNA(cfDNA)构建诊断模型,可以准确地检测早期结直肠癌(CRC)和进展期腺瘤。研究者招募了 149 例早期结直肠腺癌患者、46 例进展期腺瘤患者和 115 名健康志愿者作为训练队列,使用五个机器学习模型和五种cfDNA片段特征进行建模。该模型随后使用测试组(N = 311;包括149个早期结直肠癌、46个进展期腺瘤和116个健康对照组)进行了验证,结果显示,该模型可以很好的区分早期结直肠癌和(或)进展期腺瘤与正常个体,曲线下面积为0.988。与识别进展期腺瘤(AUC 0.982)相比,该模型在识别早期结直肠癌(AUC 0.990)方面表现更好。结果表明,cfDNA是一种有潜力的早期肿瘤标记物,具有很高的敏感性与特异性,但该研究结论仍需更大样本量外部验证的支持。
除液体活检技术外,计算机辅助诊断技术也是肿瘤筛查技术革新的重要组成内容。发表在Gastrointest Endosc杂志中的一项研究创新性地开发了一种新的计算机辅助诊断(CAD)系统,用于Barrett's食管(BE)窄带成像(NBI)图像的识别与表征。研究者先使用494,364个普通内镜图像训练CAD系统;再使用690张肿瘤BE图像与577张非肿瘤BE图像进行精细训练;然后使用了122张肿瘤BE的放大图像与70张非肿瘤BE的放大内镜图像进一步对模型进行训练;最后,使用59个肿瘤BE与98个非肿瘤BE的NBI放大内镜视频对模型进行训练和评估。结果显示,CAD系统诊断BE的准确性、灵敏度和特异性分别为84%、88%和78%。CAD系统共分析了30,021个单独的视频帧。基于视频的CAD系统准确性、灵敏度和特异性分别为83%(95%CI:78%-89%)、85%(95%CI:76%-94%)和83%(95%CI:76%-90%)。平均评估速度为每秒38帧。最终,研究者得出结论,CAD系统可以准确地判断NBI放大视频中的BE病变,并具有快速的评估速度。
内镜下治疗技术的发展
随着消化内镜技术的发展,微创技术如内镜黏膜下剥离术(ESD)以及内镜下全层切除术已经被广泛应用于治疗消化系统疾病。大量研究表明,ESD的术后伤口闭合有助于防止延迟出血。发表在Gastrointest Endosc杂志中的一项研究创新性地开发了一种新型的内镜下夹子,称为新型的内镜双夹(TTS-TC)系统。TTS-TC可以直接通过3.2mm的内镜活检孔道来发挥作用,不必安装在内镜上,也不需其他任何内镜配件的辅助。该装置的使用方法如图1所示,首先,将TTS-TC通过内镜活检通道送入消化道腔,使用其一侧的金属夹夹住伤口一侧的黏膜(图1A)。再通过移动TTS-TC将夹住的黏膜拉到伤口的另一侧(图1B)。接着使用其另外一个夹子夹住另一侧的黏膜(图1C)。两侧的粘膜均被夹住后,夹子被锁定,TTS-TC的头端被释放并保留在体内(图1D)。研究者在动物试验层面验证了TTS-TC的安全性与有效性。经过统计,研究者发现使用TTS-TC来拉合伤口的两侧,可以完成的最大跨度胃、肠分别为3.6 cm和3.9 cm。每次创面闭合时,TTS-TC和组织夹的平均使用数量分别为2.9个和4.2个。TTS-TC闭合创面的平均操作时间为3.9分钟,每个TTS-TC的平均操作时间为1.2 min。5只活猪身上的13处伤口均成功闭合,创面闭合的过程中无出血及黏膜损伤。经过为期1个月的随访,无出血、穿孔、死亡等不良事件发生。在术后1个月的内镜检查中,均观察到了创面愈合及瘢痕形成,所有的TTS-TC均自行脱落。该研究提示,TTS-TC具有良好的安全性与有效性,是具有潜力的内镜下闭合装置,并且相对于于Over-The-Scope-Clip(OTSC)与荷包缝合,具有操作上的简便性。
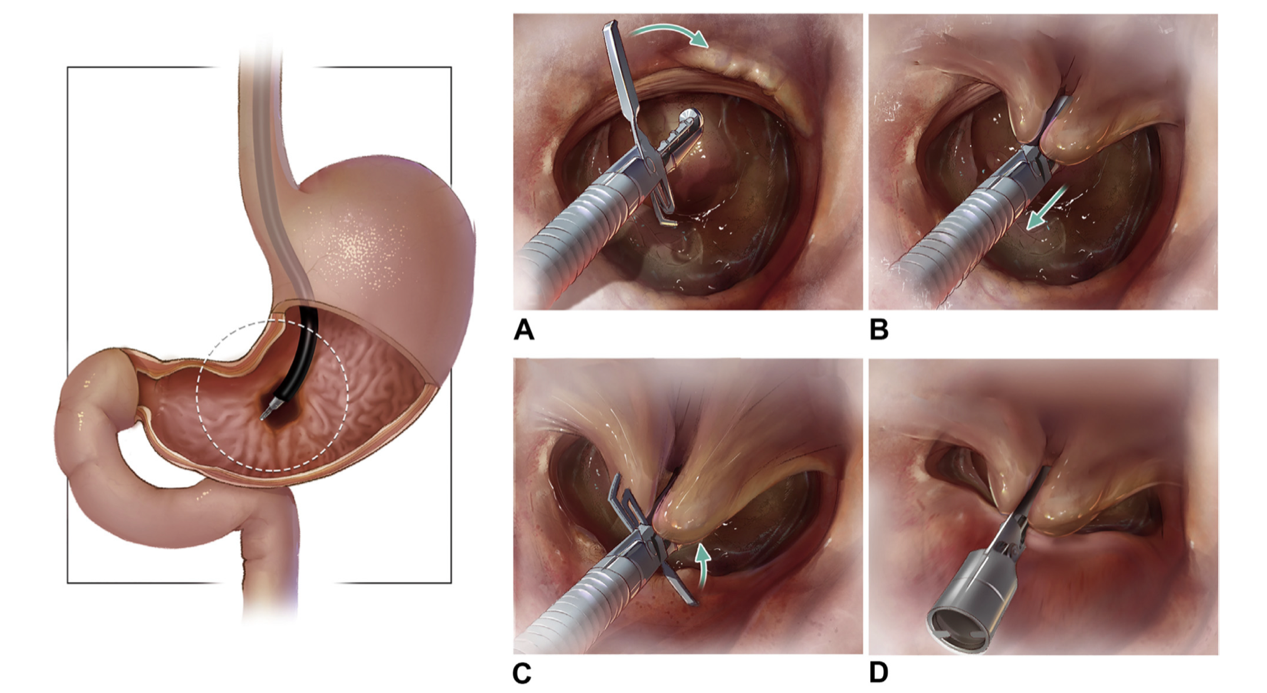
图1 TTS-TC系统使用方法图示
ESD术后出血是ESD术后常见的并发症,发表在Gut杂志的一项研究开发并外部验证了一个临床实用的胃早癌ESD术后出血预测模型:BEST-J 评分。这项研究回顾性的招募了进行过胃早癌ESD的患者,来自25个医疗机构的8291例患者作为训练集来建立模型,另外来自8个其他区域的医疗机构的2029例患者作为外部验证。经过统计,10个变量(包括华法林、直接口服抗凝剂、血液透析的慢性肾脏疾病、P2Y12受体拮抗剂、阿司匹林、西洛他唑、肿瘤大小>30 mm、肿瘤位置位于下三分之一、多个肿瘤存在和抗血小板药物的中断)被纳入预测模型中。低风险(0-1分)、中度风险(2分)、高风险(3至4分)和极高风险(≥5分)的ESD后的出血率分别为2.8%、6.1%、11.4%和29.7%。在外部验证队列中,该模型表现出良好的准确性,C统计量为0.70(95%CI:0.64 - 0.76)。
小结
本文从筛查策略、内镜下治疗新技术等角度对2021年消化道肿瘤领域的研究进展进行总结。其中,早期胃癌的风险因素研究将为更科学地筛选高风险人群提供依据,高风险地区适龄人群的内镜检查可以显著降低上消化道癌发病率与死亡率。FIT的临界值管理、血浆外泌体、cfDNA的应用以及人工智能技术为早期消化系统肿瘤的诊断提供了新的思路。新型的内镜双夹系统提供了闭合较大创口的新的解决方案,在便捷性上优于OTSC或荷包缝合的方法。最后,BEST-J评分系统也很好地预测了ESD术后出血的风险,值得临床推广。
本文版权属于《中国医学论坛报》,转载请注明出处
查看更多