查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






由欧洲肿瘤内科学会(ESMO)主办的2023 ESMO年会将于2023年10月20-24日在西班牙马德里召开。目前,大会常规摘要内容已全部更新,“2023ESMO年会中国医学论坛报学术联播”将持续整理大会重点研究,与大家一起E览盛会!
大会“Gastrointestinal tumours, lower digestive”领域共设2个优选论文专场与1个简短口头报告专场,汇集下消化道肿瘤方面的最新进展,其中包括多项中国研究,本文筛选优选论文专场1中的重点研究进行编译整理,共瞻前沿。
Neoadjuvant short-course radiotherapy followed by camrelizumab plus chemotherapy versus long-course chemoradiotherapy followed by chemotherapy in locally advanced rectal cancer: a randomized phase Ⅲ trial (UNION)
中文标题:局部晚期直肠癌新辅助短程放疗后卡瑞利珠单抗联合化疗与长程化放疗后化疗的对比:随机Ⅲ期试验(UNION)
讲者:林振宇(华中科技大学同济医学院附属协和医院)
报告时间:10月21日 14:45-14:55,CEST
研究背景
根据临床前研究和 II 期研究的结果,我们开展了一项随机、多中心、开放标签 Ⅲ 期研究,比较短程放疗(SCRT)后免疫化疗与长程化放疗(LCRT)后化疗在局部晚期直肠癌(LARC)围手术期治疗中的疗效和安全性。
研究方法
T3~4或N+直肠腺癌患者(pts)的肿瘤下缘距离肛门边缘≤10厘米,按1:1的比例随机分配到A组或B组。根据临床T分期(≤ T3对T4)和N分期(N0对N+)进行分层,患者接受SCRT或LCRT治疗,然后分别接受2个周期的卡瑞利珠单抗(CAM)+ CAPOX或单纯CAPOX治疗。随后进行全直肠系膜切除术(TME),术后A组患者接受6个周期的CAM+CAPOX治疗以及后续长达1年的CAM治疗,B组患者接受6个周期的CAPOX治疗。主要终点是独立审查委员会(IRC)评估的pCR率(ypT0N0)。分层检测的次要终点是3年EFS率和OS。
研究结果
2021年7月至2023年3月期间,231例患者被随机分配到A组(113例)和B组(118例)。在A组中,112例患者接受了SCRT治疗,107例患者完成了新辅助治疗,104例患者接受了TME治疗。在B组中,115例患者接受了LCRT治疗,109例患者完成了新辅助治疗,99例患者接受了TME治疗。A组[39.8%(95%CI 30.7%~49.5%)]与B组[15.3%(95%CI 9.3%~23.0%)]相比,ITT例群中IRC评估的pCR率显著提高,风险比为3.7[(95%CI 2.0~6.9),P<0.001],达到了主要终点。亚组分析显示,所有亚组的结果均一致为阳性。在手术例群中,A组和B组的R0切除率分别为96.2%和97.0%。在整个治疗过程中,A组和B组分别有38.1%和40.8%的患者出现术后并发症。目前正在监测长期生存结果。
研究结论
与 LCRT 后再进行化疗的 LARC 相比,SCRT 后再进行 CAM 和化疗的 pCR 率更高、耐受性更好。
Neoadjuvant Chemotherapy with CAPOX versus Chemoradiation for Locally Advanced Rectal Cancer with Uninvolved Mesorectal Fascia (CONVERT): Final Results of a Phase Ⅲ Trial
中文标题:未累及直肠筋膜局部晚期直肠癌的新辅助CAPOX化疗对比化放疗(CONVERT研究):Ⅲ期试验的最终结果
讲者:丁培荣(中山大学肿瘤防治中心)
报告时间:10月21日 14:55-15:05,CEST
研究背景
新辅助化放疗(nCRT)是治疗局部晚期直肠癌(LARC)的重要组成部分。然而,对所有直肠癌患者不加区分地进行盆腔放疗并不能带来明显的长期生存益处,反而会加重手术并发症和毒性。相比之下,对于直肠系膜筋膜(MRF)未受累的局部晚期直肠癌,单纯新辅助化疗(nCT)有望成为一种替代治疗方法。本试验旨在评估在有未受累的MRF的LARC中,使用CAPOX的新辅助化疗与使用卡培他滨的新辅助化疗的非劣效性。
研究方法
2014年6月至2020年10月期间,距肛门边缘12厘米以内、MRF未受累的LARC患者被随机分配接受4个周期的CAPOX单独化疗(nCT组)或卡培他滨CRT(nCRT组)。主要终点是3年无局部或区域复发生存(LRRFS)率,即从随机分配之日到任何局部或区域进展/复发之间的时间间隔。如果LRRFS率风险比(HR)的双侧95%置信区间(CI)上限不超过1.6(NI边界),则可确定nCT的NI。此外,还报告了次要终点,如3年无病生存(DFS)率、3年总生存(OS)率和长期毒性。
研究结果
共有663例患者入组,589例患者接受了分配的治疗(nCT,n=300;nCRT,n=289)。中位随访48个月后,对LRFFA进行了分析。nCRT治疗组的3年LRRFS率为97.4%(95%CI,95.5%~99.3%),nCT治疗组为96.3%(95%CI,94.0%~98.6%),HR为1.08(95%CI,0.46~2.54)。
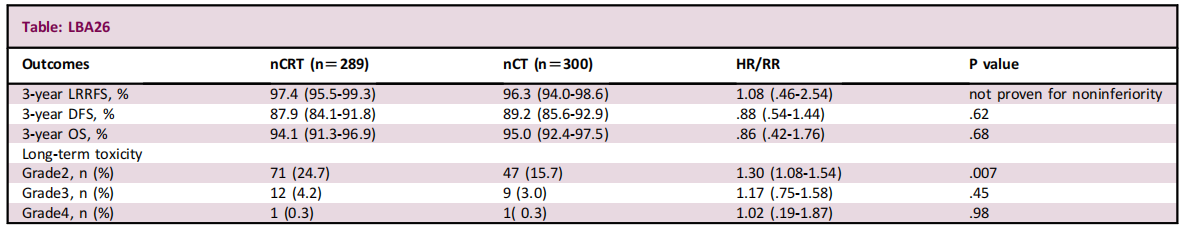
研究结论
nCT的非劣效性未得到证实,主要原因是两组患者的局部复发率都非常低。但与nCRT相比,nCT可提供相当的DFS和OS,同时减轻毒性负担。这些发现揭示了治疗未累及MRF的LARC的潜在模式转变。
Adagrasib with or without cetuximab in patients with KRASG12C-mutated colorectal cancer (CRC): Analysis of tumor biomarkers and genomic alterations
中文标题:Adagrasib±西妥昔单抗治疗KRASG12C突变的结直肠癌(CRC):肿瘤生物标志物和基因组变化分析
讲者:Meredith S. Pelster (美国)
报告时间:10月21日 15:25-15:35,CEST
研究背景
Adagrasib(ada)是一种KRASG12C抑制剂,具有23小时半衰期、剂量依赖性药代动力学(PK)特征和中枢神经系统渗透等良好特性。KRASG12C抑制剂的耐药性可能会通过EGFR再活化发生在CRC中,因此可能需要 EGFR/KRASG12C双阻断剂才能有效治疗KRASG12C突变的CRC。在KRYSTAL-1(NCT03785249)的Ⅰ/Ⅱ期队列中,对于既往接受过化疗的KRASG12C突变CRC患者,ada单药治疗(mono)和与西妥昔单抗(cetux)联合治疗的耐受性良好,ada+cetux的缓解率更高(46%),中位无进展生存期更长(6.9个月)。
研究方法
既往接受过治疗的KRASG12C突变CRC患者接受ada单药(600 mg,每日两次)或ada(600 mg,每日两次)+cetux(400 mg/m3,然后250 mg/m3 每周一次或500 mg/m3 每两周一次)治疗。两组患者的探索性分析包括获得性KRASG12C耐药性的机制以及血浆ctDNA清除率和基线肿瘤IHC评估的EGFR表达与缓解的相关性。在基线、C2D1(周期2的第1天)、C4D1和治疗结束(EOT)时收集血浆。对获得性基因组改变进行致病性鉴定,并将其定义为基线时不存在和EOT时存在。
研究结果
至数据截止日(2022年6月16日),44例患者接受了ada治疗,32例患者接受了ada+cetux治疗。ada队列中的27例患者和ada+cetux队列中的11例患者在基线和EOT时获得了配对血浆样本。在接受ada治疗和ada+cetux治疗的患者中,分别有81%(22/27)和73%(8/11)观察到获得性基因组改变,包括突变、拷贝数变化和融合。在使用ada和ada+cetux治疗的患者中,周期2时分别有55%(16/29)和88%(14/16)的患者清除了>95%的突变等位基因。初步数据表明,肿瘤EGFR表达与对ada+cetux治疗的反应之间存在关系。
研究结论
探索性分析表明,ada单药治疗和与cetux联合治疗的患者获得性耐药的机制各不相同,ada+cetux治疗的患者ctDNA反应程度更高。Ⅲ期试验KRYSTAL-10(NCT04793958)正在对ada+cetux二线治疗CRC的效果进行研究。
Safety and efficacy of D-1553 in combination with cetuximab in KRAS G12C mutated colorectal cancer (CRC): A phase II study
中文标题:D-1553联合西妥昔单抗治疗KRASG12C突变结直肠癌(CRC)的安全性和有效性:Ⅱ期研究
讲者:徐瑞华(中山大学肿瘤防治中心)
报告时间:10月21日 15:35-15:45,CEST
研究背景
作为一种高选择性、强效的KRASG12C抑制剂,D-1553 在KRASG12C突变的CRC患者中显示出令人鼓舞的抗肿瘤活性。同时靶向KRAS和EGFR途径可能会增强D-1553的抗肿瘤活性。一项正在进行的多国Ⅱ期研究(NCT04585035)正在评估D-1553联合西妥昔单抗(一种EGFR抗体)治疗KRASG12C突变的CRC的安全性和有效性。
研究方法
本研究纳入了标准治疗后病情进展的转移性CRC患者。患者必须有KRASG12C突变,且之前未接受过针对 KRASG12C的治疗。入组患者接受每天两次的D-1553 600 mg联合西妥昔单抗(标准剂量)治疗。研究终点包括疗效(RECIST, v1.1)、安全性和药代动力学(PK)。
研究结果
截至2023年4月17日,共纳入29例患者[37.9%为女性,中位年龄为56.0(范围32~76)岁,65.5%既往接受过≥3次治疗(中位数3;范围1~6),100%基线时为Ⅳ期疾病,24.1%/75.9%为ECOG PS 0/1]。数据截止时,20例患者(69.0%)仍在接受治疗。中位治疗时间为5.95个月(1.35个月~9.13个月),中位随访时间为6.24个月(2.33个月~9.13个月)。初步观察到的总体缓解率为 51.7%(15/29),15例缓解者中有9例已确认有缓解,其中5例仍在接受治疗,其缓解程度有待确认。疾病控制率为93.1%(27/29)。中位无进展生存(PFS)期为7.56个月(95%CI:5.49个月~不详)。29例患者(100%)发生了任何级别的治疗相关不良事件(TRAEs),其中最常见(≥20%)的不良事件为皮疹、AST升高、ALT升高和甲沟炎,主要为≤2级。3例(10.3%)患者发生了3~4级TRAE,均与西妥昔单抗有关。未报告5级TRAE。2/29(6.9%)例患者因TRAE导致D-1553剂量中断,1/29(3.4%)例和5/29(17.2%)例患者因TRAE导致西妥昔单抗剂量减少和中断,1/29(3.4%)例患者因TRAE导致西妥昔单抗停药。
研究结论
D-1553 和西妥昔单抗的联合治疗显示了可接受的安全性,与D-1553单药治疗相比,获得了更高的缓解率,在重度预处理的KRASG12C突变CRC患者中,PFS期很有潜力。更多数据将在会议上公布。
Impact of baseline molecular alterations on the efficacy of tucatinib (TUC) plus trastuzumab (Tras) for HER2+, RAS WT metastatic CRC (mCRC) in MOUNTAINEER
中文标题:MOUNTAINEER研究中基线分子改变对图卡替尼(TUC)联合曲妥珠单抗(Tras)治疗HER2+、RAS WT转移性癌症(mCRC)疗效的影响
讲者:John H. Strickler (美国)
报告时间:10月21日 15:45-15:55,CEST
研究背景
HER2是mCRC的可操作生物标志物,但同时发生的基因组改变的影响尚不清楚。在MOUNTAINEER研究的基础上,TUC+Tras被美国食品药品监督管理局(FDA)批准用于化疗难治性HER2+、RAS-WT的mCRC患者。在此,我们将介绍伴随基线基因组改变对TUC+Tras临床活性的影响。
研究方法
MOUNTAINEER纳入了通过组织免疫组化(IHC)、原位杂交(ISH)和/或新一代测序(NGS)进行局部评估的 HER2+的mCRC患者。通过IHC/FISH、PGDx组织NGS和Guardant 360血液NGS对基线组织和血液样本进行回顾性分析。针对在接受TUC+Tras治疗的患者中发生超过5例的特定基因组改变(SNV和CNV),计算了cORRs[根据BICR的RECIST v1.1标准,获得完全缓解(CR)或部分缓解(PR)的患者比例]和缓解持续时间(DoR)。该分析为描述性分析,未进行统计比较。
研究结果
在84例接受TUC+Tras治疗的患者中,有65例样本可用于 FISH检测。根据HER2/CEP17比值[>5,n=50:cORR (95%CI)=44.0%(30.0,58.7);≤5,n=15:cORR (95%CI)=26.7%(7.8,55.1)]或HER2拷贝数[>9.45,n=57:cORR(95%CI)=42.1%(29.1,55.9);≤9.45,n=8:cORR(95%CI)=25.0% (3.2,65.1)]。对中心HER2+检测结果为阳性的患者的组织(n=45)和血液(n=66)样本进行NGS检测,发现了ERBB2、PIK3CA、APC和TP53等关键基因的伴随突变和/或基因组扩增。在这些患者中,cORR和DOR与总体观察结果基本相似(表)。
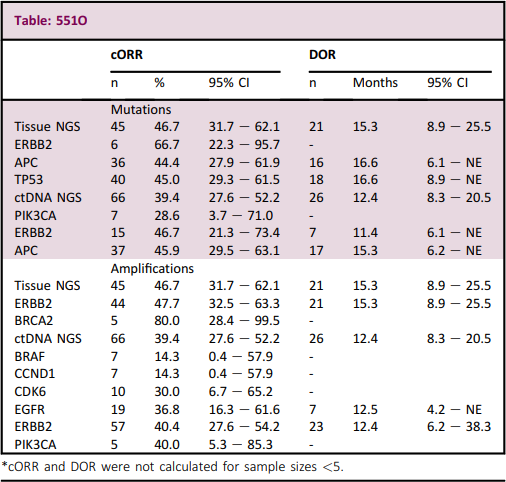
研究结论
这项对MOUNTAINEER试验的探索性分析发现,在HER2+RAS-WT的mCRC和其他临床相关基因组改变的患者亚群中,TUC+Tras的临床疗效与主要分析结果基本一致。

读前沿进展,听中国强音,享国际视野。“2023ESMO年会中国医学论坛报学术联播”将持续关注大会动态,为大家带来大会最新内容,敬请期待!
查看更多