查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





2019年11月26日,国家药品监督管理局(NMPA)药品评审中心(CDE)官网显示默沙东公司旗下帕博利珠单抗(俗称“K药”)的又一适应证完成审评审批。
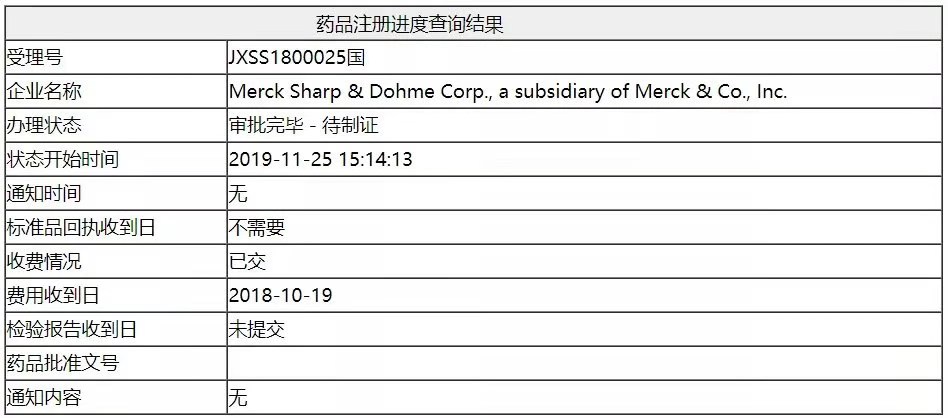
据查,该适应证于2018年10月22日,在CDE被正式受理(受理号:JXSS1800025)。此次获批的适应证为免疫检查点抑制剂帕博利珠单抗联合化疗(卡铂和紫杉醇)方案,无论PD-L1表达情况,一线治疗转移性鳞状非小细胞肺癌(NSCLC)。
本次获批基于一项大型的全球III期临床研究(KEYNOTE-407)的结果。该研究结果于同年刊登在《新英格兰医学杂志》。
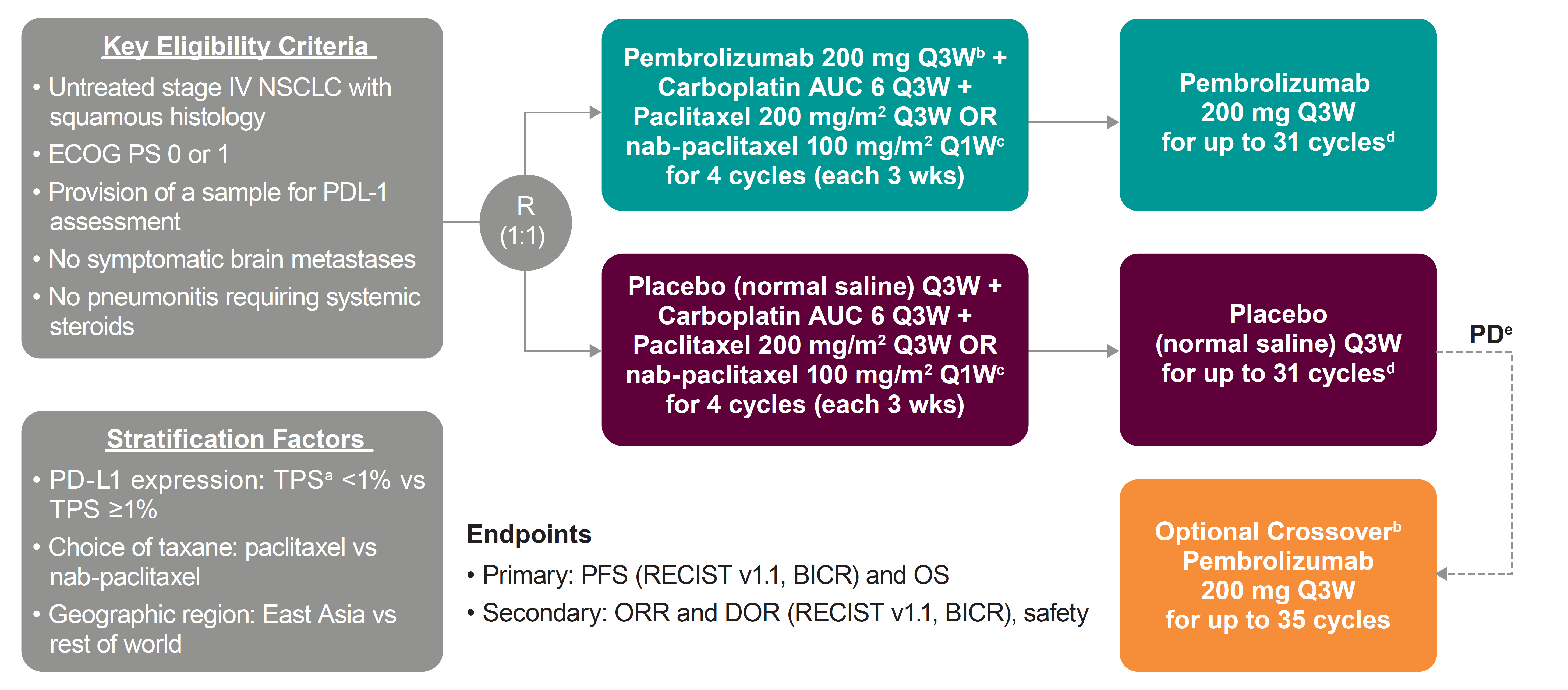
在今年的欧洲内科肿瘤学(ESMO)年会上公布了更新的KEYNOTE-407研究OS数据,并首次公布了PFS2数据。结果显示,在所有的意向性治疗(ITT)人群中,帕博利珠单抗联合化疗组的中位OS达17.1个月(14.4~19.9个月),而单纯化疗组仅11.6个月(10.1~13.7个月);帕博利珠单抗联合化疗降低29%的死亡风险(HR=0.71, 95%CI 0.58~0.88);
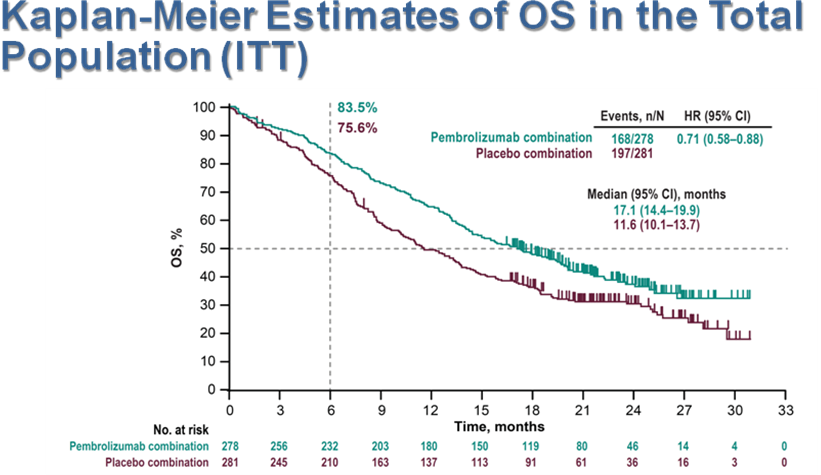
在单纯化疗组中有49.1%的患者接受后续抗PD-1/PD-L1治疗的情况下, 帕博利珠单抗联合化疗组仍然为患者带来持续的OS获益。两组的中位PFS2分别为13.8个月和9.1个月(HR=0.59;95%CI 0.49~0.72)。
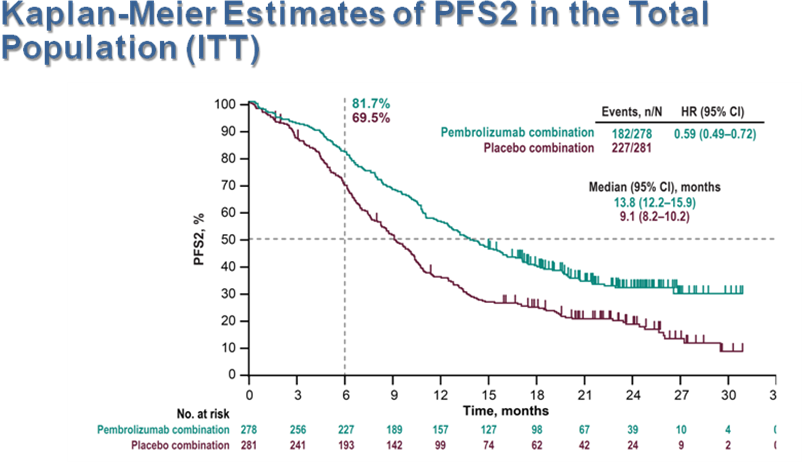
据国家癌症中心今年发布的最新统计数据,我国2015年新增肺癌患者约78.7万肺癌,其中NSCLC约占肺癌总数的80%~85%, 其中已经发展为晚期或转移性肺癌患者约占60%,鳞状NSCLC约占30%。
目前中国晚期鳞状NSCLC的一线治疗主要仍以含铂化疗方案为主,缓解率约为30%,中位生存时间仅一年左右,因此,中国晚期肺鳞癌的一线治疗仍面临极大困境,亟待解决。KEYNOTE-407研究中国牵头人、吉林省肿瘤医院程颖教授指出,帕博利珠单抗联合化疗一线治疗鳞状NSCLC的客观缓解率(ORR)达到62.6%,且显著延长患者总生存获益,有望彻底改变针对鳞状NSCLC的临床实践,让这部分患者有机会得到长期生存获益。
帕博利珠单抗已分别于2018年7月、2019年3月及2019年9月在国内获批单药治疗不可切除转移性黑色素瘤、联合化疗一线治疗非鳞NSCLC以及单药一线治疗PD-L1表达阳性(TPS≥1%)NSCLC(包括鳞和非鳞NSCLC)的适应证,此次获批的“无论PD-L1表达情况,一线治疗转移性鳞状NSCLC”为帕博利珠单抗在华获批的第四个适应证,也是其获批的第三个一线治疗NSCLC适应证。这使帕博利珠单抗成为了国内及晚期肺癌治疗领域,获批适应证最多的PD-1单抗。
此次适应证的获批,也标志着帕博利珠单抗在国内已完成一线治疗无驱动基因突变NSCLC的最后一块"拼图“, 堪称这一治疗领域的“免疫之王”。同时,此适应证的获批也必将进一步推动免疫治疗成为晚期NSCLC一线治疗的基石,从而彻底改变国内晚期NSCLC一线治疗的临床实践,让中国所有无驱动基因突变的晚期NSCLC患者都有机会获得免疫治疗可能带来的长期生存“红利”,并助力提升我国晚期肺癌的五年生存率。
查看更多