查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





6月8~10日,由中国老年医学学会消化病分会主办,北京大学人民医院协办的2018年第九届免疫介导消化系统疾病论坛暨2018北京第十届肠黏膜屏障与相关疾病论坛在京召开。此次会议针对肠黏膜屏障相关疾病和免疫介导消化系统疾病2项热点议题,旨在更好地提高老年消化系统疾病的防治水平,增进国内消化同道们的交流。
终末期肝病----细胞移植治疗的前世、今生与未来

第二军医大学附属长征医院消化内科 谢渭芬
终末期肝病的细胞移植治疗是一个既古老又热门的话题,本次讲座谢教授从以下三个方面对细胞移植治疗的前世、今生与未来进行讲述:
肝细胞移植
肝脏组织学目前已经阐释已十分清楚,肝脏主要细胞分为实质细胞和非实质细胞,其中实质细胞即肝细胞,占肝脏细胞总数的65%,肝总体积的80%,而非实质细胞则包括胆管上皮细胞、肝星状细胞、窦内皮细胞、Kupffer细胞和自然杀伤细胞。在肝脏再生中的关键是肝细胞再生。正常情况下肝脏是一个非常安静的器官,肝细胞的平均生命周期为200-300天,肝脏每1-2年才更新一次。而在病理情况下,肝脏具有强大的再生能力。
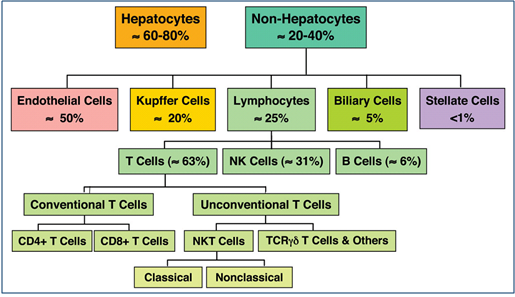
终末期肝病的肝脏病理改变包括肝细胞损伤和坏死,纤维组织大量增生,其细胞总数和功能均显著下降。目前,原位肝移植是终末期肝病唯一根治方法,但由于供肝缺乏、费用昂贵、免疫抑制等问题应用受限。因此细胞移植,包括肝细胞移植、干细胞移植和肝干细胞移植等,成为未来治疗终末期肝病的希望。
肝细胞移植自1976年起进入学者的视线,其最初应用于代谢障碍性疾病,随后逐渐用于急性肝衰竭等疾病的治疗中。目前,肝细胞移植的主要适应症包括以下疾病:急性肝衰竭(药物、病毒、特发性、毒物、妊娠期急性脂肪肝),α1抗胰蛋白酶缺乏症,家族性高胆固醇血症,VII因子缺乏症,糖原累积病等。肝细胞移植与肝移植相比存在以下优势:1)一个供者可以提供肝细胞给多个受者,从而使多名患者受益;2)创伤性小;3)肝细胞可长期冷藏保存;4)若一次移植失败,患者仍可进行再次移植;5)原始的肝脏仍然在体内,有潜在的康复能力;6)仍然保留基因治疗的可能,不需长期应用免疫抑制剂。但肝细胞移植也仍然有很多问题,包括:1)缺乏足够数量的高质量的肝细胞来源;2)定植率低,长期疗效有限;3)在体外冻融后可能失去功能;4)异体细胞移植比完整的肝脏移植更易出现排斥反应。人诱导型肝细胞 (hiHeps) 治疗小鼠代谢性肝病和急性肝功能衰竭已取得较好疗效,但其病毒性载体的安全性问题限制其临床应用。
目前有研究显示多种肝细胞核因子(HNFs)组合可在体内促使星状细胞转化为肝细胞,显著减轻肝纤维化、逆转早期肝硬化。但星状细胞转化的比例仅1%左右。
(非肝)干细胞移植
干细胞移植是治疗终末期肝病的另一方法,包括自体干细胞移植和异体干细胞移植。其中间充质干细胞(Mesenchymal stem cells,MSC)是目前临床中应用最为广泛的干细胞种类,其有强大的分化能力。早期II期临床研究结果显示自体骨髓MSCs可用于治疗终末期肝病,患者肝功能明显改善,MELD评分显著下降,未发现明显不良反应。在应用自体骨髓MSCs治疗乙肝相关肝衰竭的研究中发现其短期疗效改善明显,但长期疗效无显著差别(192周)。在酒精性肝硬化的II期临床研究中,治疗组较对照组纤维化程度明显改善,Child-Pugh评分明显下降。MSCs治疗可提高失代偿肝硬化和ACLF生存率。在异体骨髓MSCs治疗慢加急性肝功能衰竭的研究中,治疗组总体生存率及各时间点生存率均高于对照组。
在间充质干细胞治疗终末期肝病的治疗机制研究中,2012年Hepatology发表的研究显示给予暴发性肝衰竭的猪hBMSC治疗,对照组4天全部死亡,而治疗组有87.6%生存6个月以上,10周时人源性肝细胞约占30%,因此该研究认为人源性肝细胞定植在猪肝脏上起到治疗作用。但在2017年Gut上发表的试验结果显示在7天和14天时,人源性肝细胞仅占4.5%和4.7%,因此该研究团队认为MSCs治疗肝衰竭的机制主要是抑制炎症因子风暴,稳定机体内环境。间充质干细胞治疗同样存在一定的优势与劣势,其优势在于无伦理问题、取材方便、短期疗效较好,而劣势在于长期疗效不佳、数量少、准备时间长等。
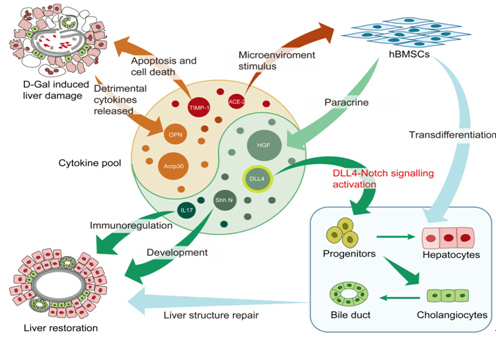
除此以外,诱导成熟肝细胞去分化为干细胞也是重要的方法之一。最新研究显示可利用Y-27632、A-83-01、CHIR99021三个小分子鸡尾酒组合诱导成熟肝细胞去分化,所诱导出的干细胞可再分化为肝细胞及胆管细胞,体内定植率超过70%,促进肝脏再生。
自体肝干细胞移植
肝细胞再生和肝干细胞的来源问题是目前研究热点。现已发现肝脏内一类具有多向分化潜能的原始细胞,可称为肝前体细胞(Hepatic Progenitor Cells,HPCs)。既往认为骨髓干细胞、肝星状细胞是肝干细胞的主要来源,但这两种说法已被推翻,目前认为肝细胞是肝干细胞的主要来源。
2015年Cell发表的一篇研究显示正常肝脏汇管区周围存在一群杂合肝细胞,其既表达干细胞标志物Sox9,同时也表达肝细胞标志物,而在慢性肝损伤后这些细胞会大量增生,促进肝脏再生。同年另一项研究发现肝脏中还有一类Lgr5+干细胞存在,其可分化成肝细胞和胆管细胞,但在肝脏中的定植率较低。同时Nature也发表了一项研究,结果显示中央静脉周围存在一群Axin2(+)的干细胞,其从中央静脉向外扩增,逐渐向肝细胞分化,一年内可更换肝脏内约40%的肝细胞。以上研究说明肝脏不仅可以从汇管区开始再生,也可从中央静脉区再生。2018年Nature上的一项研究进一步证实散在分布于肝组织中的TERThigh肝细胞无论在生理还是病理状态下均可引起肝细胞的再生。
由于终末期肝硬化时肝细胞受损严重,那么已经发展为终末期肝病的肝脏是否还具有再生能力呢?近日,谢教授和中科院惠利健课题组合作在Cell Stem Cell杂志发表有关肝再生研究论文,发现严重肝损伤时非肝细胞参与肝细胞的修复和再生。这一群非肝细胞经研究证实部分来源于胆管细胞,而且这些胆管细胞在转化过程中并非经过干细胞再生为肝细胞,而是经过具有胆管细胞和肝细胞属性和形态特征的“双相细胞”(bi-phenotypic cells)转化为肝细胞。这些胆管来源的“双相细胞”具有活跃的分裂增殖能力,其增殖能力远高于其他未发生转化的胆管细胞。这一发现解释了虽然发生转化的胆管细胞亚群所占总体胆管细胞比例较小,却具有强大修复肝实质能力的原因,也凸显了该类细胞在肝脏损伤修复中的重要性。近期来自UCSF再生医学研究中心Holger Willenbring教授实验室报道了肝细胞可转分化为胆管细胞。
这些研究充分证明,肝脏内的细胞具有高度的可塑性,在生理状态、急性损伤、慢性损伤、重度损伤等不同状态下,肝脏多种细胞均可通过去分化或转分化,为再生肝脏细胞提供了多种来源,使肝细胞得到修复和再生。这是肝脏具有强大再生能力的基础。
自体肝干细胞治疗存在明显的优势,包括无伦理问题、无免疫源性、可培养扩增等,但其肝脏定植率低仍然是限制其临床应用的主要问题。
综上所述,细胞移植的前世是指传统肝细胞移植方法,其对遗传性疾病和急性肝衰竭有一定疗效,同时诱导型肝细胞具有一定的潜力。而目前,间充质干细胞展现出了一定的短期疗效,小分子诱导的干细胞有望应用于临床。未来,自体肝干细胞移植很可能成为治疗终末期肝病的有效手段。
(北京大学人民医院消化科 刘心怡 整理 谢谓芬 审阅)
查看更多